Orale biofilmmodeller – nye muligheter for plakkstudier
Forfatter
professor, dr.odont. Institutt for klinisk odontologi, Avdeling for kariologi og gerodontologi, Det odontologiske fakultet, Universitetet i Oslo
Artikkelen er basert på oversiktsartikkelen Guggenheim B, Guggenheim M, Gmür R, Giertsen E, Thurnheer T. Application of the Zürich biofilm model to problems of cariology. Caries Res 2004; 38: 212-22 og på et foredrag ved NTFs landsmøte i Stavanger 14. oktober 2006.
Dentalt plakk er en biofilm hvor ca. 700 ulike bakteriearter kan påvises. Begrepet biofilm brukes stadig oftere i litteraturen om plakk. Biofilmer er naturlig forekommende, tredimensjonale samfunn av mikroorganismer som vokser på overflater i en matriks. Vår kunnskap om plakkets fysiologi og patogenisitet bygger i vesentlig grad på laboratorieforsøk med planktoniske (frittflytende) bakterier. Det er imidlertid velkjent at bakterier i biofilmer viser andre egenskaper enn planktoniske bakterier. Modeller av orale biofilmer kombinert med moderne molekylærbiologiske metoder og mikroskopiske teknikker, gir nye muligheter for å studere disse komplekse bakteriesamfunnene. Slike studier gir bl.a. håp om nye strategier for å forebygge plakkrelaterte sykdommer.
Denne artikkelen omhandler en nylig utviklet in vitro multispecies biofilmmodell som etterligner supragingivalt plakk. Modellen beskrives, og det gis eksempler der den brukes til å studere biofilmens struktur og funksjoner. Funn fra klinisk relevante forsøk med modellen samt effekt av profylaktiske tiltak belyses.
Modeller av orale biofilmer er forholdsvis nylig tatt i bruk innen odontologisk forskning. Mens plakkbakterier i mer enn hundre år er blitt studert i flytende kulturer, ofte renkulturer som vokste i rikt vekstmedium, er modeller i løpet av de siste tiår utviklet for å etterligne forholdene i munnen bedre (1, 2). I slike modeller adhererer mikroorganismer til en overflate og vokser deretter festet til overflaten. Orale biofilmstudier, særlig med multispecies-modeller, antas å gi nye muligheter for forebyggelse av sykdom ved bedre forståelse for interaksjoner i plakk, dets struktur, økologi, diffusjonsegenskaper, metabolisme og effekt av antimikrobielle stoffer på disse komplekse mikrobiologiske samfunnene.
Det er velkjent at bakterier i biofilmer viser andre egenskaper enn planktoniske (frittflytende) bakterier som vokser i suspensjon uten å feste seg til en overflate (3). Biofilmer er naturlig forekommende, strukturerte samfunn av mikroorganismer, f.eks. alger, bakterier og sopp. Mikroorganismene vokser på overflater innesluttet i en matriks. Matriksen produseres for det meste av organismene og består hovedsakelig av polysakkarider, men også av proteiner og DNA. De aller fleste bakterier i naturen lever i biofilmer. De dannes på livløse og levende overflater og forårsaker infeksjoner hos mennesker og dyr som kan være vanskelige å behandle. Biofilmer er blitt sammenlignet med høyere flercellete organismer (4). De viser komplekse intercellulære interaksjoner, inkludert kommunikasjon ved hjelp av signalmolekyler (5). Bakterier i biofilmer er mer resistente mot antimikrobielle stoffer enn planktoniske bakterier, noe som forklarer at antimikrobielle midler har dårligere effekt klinisk enn forventet fra laboratorieforsøk (6).
Karies, gingivitt og periodontitt er multifaktorielle sykdommer der den normale bakteriefloraen koloniserer som dentalt plakk og er nødvendig for sykdomsutvikling. Plakk er en typisk biofilm som består av mikrobielle mikrokolonier omgitt av en ekstracellulær matriks. Supra- og subgingivalt plakk er blant de best studerte biofilmer når det gjelder dannelse og sammensetning. Sammensetningen av plakk, både med hensyn til arter og antall organismer, avhenger i siste instans av vekstbetingelsene. Disse synes å være avgjørende for interaksjoner med verten, og resulterer i helse eller sykdom. P.D. Marsh, en pionér innen oral biofilmforskning, har beskrevet dette forholdet som «den økologiske plakkhypotesen» (7).
Igangværende oral biofilmforskning fører til at flere paradigmer, basert på forsøk med planktoniske bakterier, er i ferd med å endres. Denne artikkelen omhandler en nylig utviklet supragingival biofilmmodell og dens anvendelse for å belyse basale og klinisk relevante problemstillinger med direkte eller indirekte betydning for forebyggende tannpleie.
Beskrivelse av modellen
Biofilmene vokser på skiver av hydroksylapatitt eller bovin emalje (fra storfe) dekket med en salivær pellikel. Denne dannes på skivene fordi bakterier i dentalt plakk fester seg til pellikeldekkete tannoverflater. Pellikelen er et tynt, strukturert lag som består av proteiner og glykoproteiner fra saliva. Vi bruker fem orale bakterier, tre grampositive (Actinomyces naeslundii, Streptococcus oralis, Streptococcus sobrinus eller Streptococcus mutans) og to gramnegative (Veillonella dispar, Fusobacterium nucleatum) samt en sopp (Candida albicans).
Et biofilmforsøk som varer fra mandag til fredag, vises skjematisk i Figur 1. Mikroorganismene overføres fra agarplater til flytende medium og dyrkes anaerobt over natten ved 37 °C. Kulturene standardiseres og blandes. Skivene dekkes med saliva i 4 timer for å danne en pellikel (adsorberte proteiner og glykoproteiner) før de overføres til mediet, og blandingen av mikroorganismer tilsettes. Biofilmene dyrkes anaerobt ved 37 °C. I standardmodellen fôres biofilmene med en blanding av 70 % saliva og 30 % medium som inneholder 0,3 % glukose i de første 16,5 timer, deretter 0,15 % glukose + 0,15 % sukrose. I noen tilfelle bruker vi den såkalte «Feast and Famine»-modellen som etterligner vekstbetingelsene i munnen bedre. Da vokser biofilmene i saliva og blir tilført «måltider» med glukose og sukrose tre ganger daglig i 45 minutter, første gang (tid 0 minutter) et «måltid» med bare glukose. Mediet eller saliva skiftes etter 16,5 og 40,5 timer, og biofilmene høstes etter 64,5 timer (Figur 1). Antallet mikroorganismer bestemmes ved dyrking på uspesifikke og spesifikke agarmedier og ved bruk av fluorescerende DNA-fargestoffer.
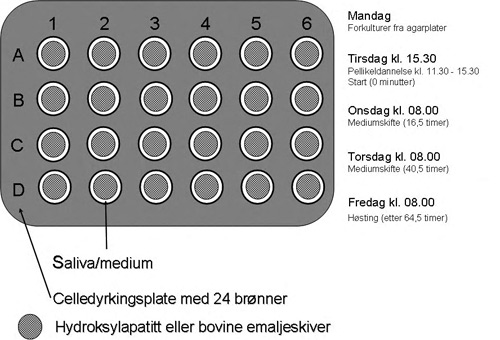
Figur 1. Skjematisk fremstilling av biofilmforsøk med standardmodellen. Biofilmene vokser på pellikeldekkete skiver av hydroksylapatitt eller bovin emalje og «mates» med en blanding av 70 % saliva og 30 % medium som inneholder 0,3 % glukose i de første 16,5 timer, deretter 0,15 % glukose + 0,15 % sukrose.
Biofilmene undersøkes på forskjellige tidspunkt ved hjelp av diverse teknikker, bl. a. immunfluorescens og fluorescerende in situ hybridisering (FISH). Ved FISH brukes fluorescerende DNA-prober som binder spesifikt til 16S rRNA-sekvenser hos bakteriene (8). Biofilmenes struktur og funksjoner undersøkes ved hjelp av konfokal-laser-skanningmikroskopi (KLSM). Denne teknikken tillater å visualisere biofilmers egenskaper tredimensjonalt uten å forstyrre oppbygningen.
Gjentatte forsøk har vist at det totale antallet bakterier i biofilmen etter 40,5 og 64,5 timers vekst er reproduserbart, også antallet for hver enkelt bakterie. Det totale antallet «colony-forming units» (CFU) ved bruk av standardmodellen ble gjennomsnittlig funnet å være 1,2 x 109 etter 64,5 timer (9). Gjennomsnittlig andel levende bakterier etter 40,5 timer er 85 % (9). Bakterietallet i biofilmen per mm2 hydroksylapatittoverflate stemmer godt overens med antallet bakterier per mm2 emaljeoverflate i biofilmer som ble dannet på bovine emaljeskiver båret i akrylplater i munnen (9, 10).
Adhesjon og samspill mellom species i biofilmen
Biofilmers motstand mot antimikrobielle stoffer, diffusjon og metabolske interaksjoner i biofilmer knyttes til deres arkitektur (1, 2, 6). Kunnskap om plakkets dannelse og struktur, både med hensyn til mikrobenes vekstmønstre, romlig fordeling av mikrober samt mikrobielle interaksjoner er vesentlig for å forstå dets patogenisitet og for å kunne utvikle nye strategier for å forebygge sykdom.
Plakkdannelse er en trinnvis prosess hvor bakterier først adhererer til pellikeldekket tannoverflate og deretter vokser. Det antas at adhesjon av bakterier til pellikel er en høyst selektiv prosess der primære plakkdannere har gjenkjennelsessystemer på overflaten (adhesiner) som binder spesifikt til reseptorer i pellikelen (11). Sekundære kolonisatorer antas å være helt avhengige av koadhesjon til pionérbakteriene via adhesin-reseptor interaksjoner, og spesifikke mikrokolonier dannes (12). Disse oppfatningene stammer i vesentlig grad fra forsøk med ikke-voksende bakterier blandet i suspensjon (13) og har derfor liten relevans til den kliniske situasjonen.
Ved bruk av fluorescens-merkete species-spesifikke antistoffer sammen med KLSM ble bakteriell adhesjon, romlig fordeling av bakteriene, mikrokoloniers morfologi og interspecies-sammenheng mellom de fem bakteriene studert i løpet av biofilmdannelsen (14). Alle parvise kombinasjoner ble visualisert ved merking med monoklonale antistoffer etter 15 minutter, 16,5, 40,5 og 64,5 timer. Parallelt ble biofilmene analysert kvantitativt ved dyrking (14).
Det viste seg at samtlige bakterier, både antatt tidlige plakkdannere (S. oralis, A. naeslundii) og antatt sekundære kolonisatorer (S. sobrinus, V. dispar, F. nucleatum), hadde sterk adhesjon til pellikelen etter 15 minutter som vist i Figur 2a til venstre. Antallet bakterier påvist ved bildeanalyse stemte godt overens med CFU ved dyrking. Koadhesjon spilte liten rolle i tidlig fase av biofilmdannelsen som illustrert for F. nucleatum og A. naeslundii i Figur 2a til høyre. Selv bakteriepar som koaggregerer i flytende medier, koloniserte initialt i 96 % av tilfellene som enkle celler etter 15 minutter (14). Disse funn stiller spørsmål ved den allment aksepterte oppfatningen at spesifikke adhesjonsmekanismer og koaggregering som vist i ikke-voksende planktoniske cellekulturer, er viktige mekanismer for å forklare rekkefølgen av bakteriers kolonisering i plakk.
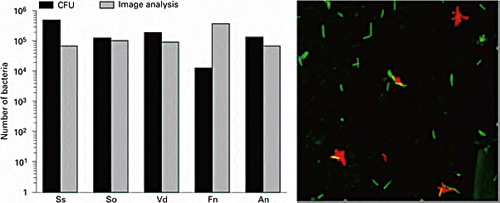
Figur 2a. Antall bakterier etter 15 minutter adhesjon til pellikel på hydroksylapatittskiver. Dyrking (CFU) eller bildeanalyser av bakterier farget med fluorescerende species-spesifikke monoklonale antistoffer: S. sobrinus (Ss), S. oralis (So), V. dispar (Vd), F. nucleatum (Fn), A. naeslundii (An). Bakteriene adhererte hovedsakelig som enkeltceller etter 15 minutter som vist på bildet til høyre hvor F. nucleatum er farget grønn og A. naeslundii rød. (Fra referanse 1)
Spesielle vekstformer for de enkelte bakteriene ble karakterisert og interspecies-vekstmønstre ble observert og klassifisert som fem hovedtyper. Disse er beskrevet utførlig i originalpublikasjonen (14). Eksempler på interspecies-relasjoner i biofilmen etter 64,5 timer vises i Figur 2b. Funn fra disse undersøkelsene og nylige biofilmforsøk med subgingivale, potensielt periodontopatogene bakterier viste at koadhesjon spiller liten rolle i tidlig fase av biofilmdannelsen, og bekrefter at bakteriers vekstbetingelser er av vesentlig betydning for biofilmers dannelse og struktur (14, 15).
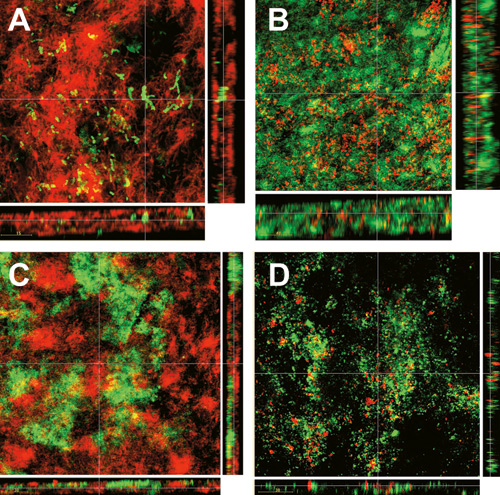
Figur 2b. KLSM-bilder (KLSM = konfokal-laser-skanningmikroskopi) av 64,5 timers biofilmer farget med fluorescerende species-spesifikke monoklonale antistoffer. A: Streptococcus sobrinus (grønn) og Fusobacterium nucleatum (rød). B: Fusobacterium nucleatum (grønn) og Actinomyces naeslundii (rød). C: Streptococcus oralis (grønn) og Fusobacterium nucleatum (rød). D: Veillonella dispar (grønn) og Streptococcus sobrinus (rød). De gule linjene nederst til venstre på hvert bilde angir avstand i mikrometer. (Fra referanse 1)
Massetransport av makromolekyler i biofilmen
Kunnskap om massetransport i biofilmer er vesentlig for å forstå deres oppbygning, egenskaper og patogene potensial og for å kunne utvikle strategier for forebyggelse av sykdom. Det har vært antatt at biofilmer inneholder et nettverk av kanaler som er av betydning for biofilmenes diffusjonsegenskaper (16, 17). Funn fra våre biofilmforsøk har stilt spørsmål ved forekomsten av kanaler i orale biofilmer.
Diffusjon av fluorescens-merkete makromolekyler med molekylvekt som varierte fra 3 til 900 kilodalton (kD) ble undersøkt med hensyn til tid og molekylstørrelse i standardmodellen (18). Bl. a. ble det brukt dextraner (3, 10, 40, 70 kD), IgG (150 kD), IgG-fragmenter (100 kD), R-phycoerythrin (240 kD) og IgM (900 kD). Biofilmer ble inkubert med fluorescerende prober i 2, 60, 120, 300 og 600 sekunder. Noen eksempler på KLSM-bilder av diffusjon i biofilmen vises i Figur 3a. Det fremgår tydelig at 240-kD phycoerythrin penetrerte dårlig inn i biofilmen (Figur 3a), mens 900-kD IgM samlet seg på overflaten og trengte nesten ikke gjennom. Basert på molekylstørrelsene kunne vi slutte at porene i biofilmen har en diameter såvidt over 11 nm. Videre analyser av diffusjonen viste at «tortuositet» er den mest sannsynlige forklaringen på sterkt retardert diffusjon i biofilmen (18) som beskrevet mer utførlig senere.
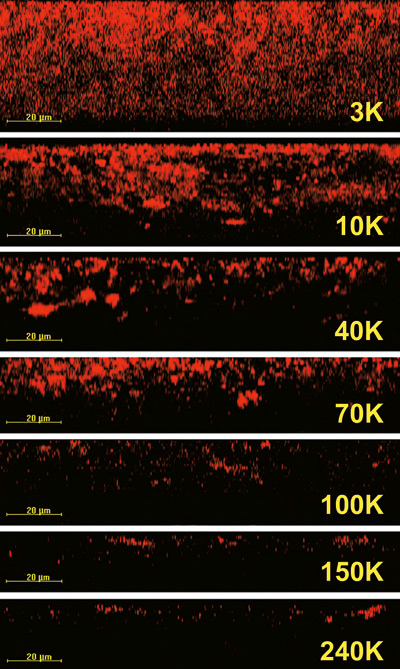
Figur 3a. KLSM-bilder av tverrsnitt av 64,5 timers biofilmer viser diffusjon av fluorescens-merkete makromolekyler med forskjellig molekylvekt etter 120 sekunder (3-kD dextran) eller etter 600 sekunder (10- til 240-kD dextran). K = Kilodalton, mål for molekylvekt. (Fra referanse 1)
Retardert diffusjon av molekyler med radius < 10 nm og den generelle antakelsen at biofilmer har kanaler i størrelsesorden mikrometer (19) er motstridende oppfatninger. De velkjente «sorte hull» som antas å være kanaler gjennom biofilmer, finnes også i orale biofilmer når mikroorganismene farges grønne med Syto 13 eller i trippel-FISH fargete biofilmer som vist i Figur 3b; A og B. Det viste seg imidlertid at når biofilmer i tillegg ble farget med Calcofluor (18) som binder til ekstracellulære polysakkarider (EPS), fremkom at multispecies-biofilmer som inneholder streptokokker og sukrose består av mikrobielle mikrokolonier omgitt av en kompakt polysakkarid-hydrogel uten kanaler (Figur 3b; C). Diffusjonsforsøk med slike dobbeltfargete biofilmer viste at dextraner ³ 10 kD ikke kan diffundere gjennom den ekstracellulære matriksen, men må diffundere gjennom mikrokolonier (Figur 3b; D). Tortuositet vil si at molekylene snirkler seg sakte gjennom de mikrobielle masser og har lang diffusjonsvei med uttalt buktning, forgrening og tilstedeværelse av flaskehalser. 3-kD-molekyler kan derimot diffundere gjennom porer med diameter 2,8 – 4,6 nm i den ekstracellulære matriksen. Dette forklarer den høyere diffusjonshastigheten og mindre tortuositet for 3-kD-molekyler (Figur 3a). Disse funn kan også delvis forklare lavere kariesfremmende evne av stivelse sammenlignet med lavmolekylære sakkarider som beskrevet senere.
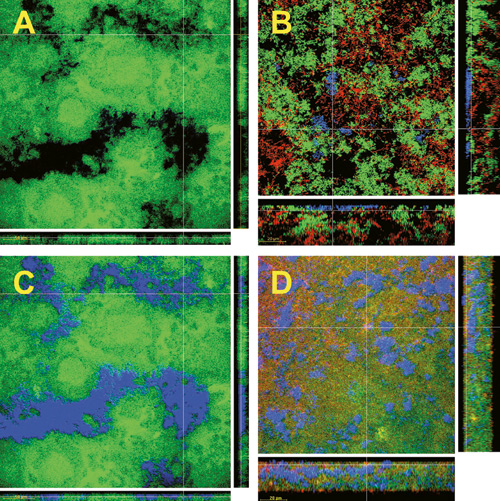
Figur 3b. KLSM-bilder av 64,5 timers biofilmer. A: Alle mikro-organismer (grønne) farget med Syto 13. B: Trippel-FISH (fluorescerende in situ hybridisering) farget biofilm: F. nucleatum (rød), S. oralis (grønn) og V. dispar (blå). C: Mikroorganismer (grønne) farget med Syto 13 og EPS (blå) farget med Calcofluor. D: Mikroorganismer (grønne, Syto 13), 10-kD dextran (rød), EPS (blå, Calcofluor). Bildene A og C viser samme sted på biofilmen. EPS = Ekstracellulære polysakkarider. (Fra referanse 1)
Betydningen av ekstracellulære polysakkarider
S. mutans og S. sobrinus regnes for å være av stor betydning ved utvikling av karies. Den kariesfremmende evnen knyttes til bakterienes syredannelse og produksjon av vannuløselige EPS fra sukrose som i svært liten grad brytes ned av enzymer (20). Hos S. mutans katalyseres syntesen av EPS av tre glukosyltransferaser (GTF). GTF B syntetiserer bare vannuløselig glukan (mutan), GTF C produserer både vannuløselig og løselig glukan (dextran), mens GTF D syntetiserer bare vannløselig glukan. GTF og glukan, spesielt det uløselige mutan, antas å være av vesentlig betydning for initial adhesjon og videre kolonisering av organismen i plakk og for koadhesjon av andre supragingivale plakkbakterier (21, 22). Dessuten virker EPS beskyttende mot antibakterielle og toksiske stoffer (22). EPS antas også å være av vesentlig betydning for plakkets struktur, diffusjon av molekyler i plakk og kariesutvikling (1, 2, 6, 21).
«Feast and Famine»-modellen ble brukt til å undersøke biofilmer som inneholdt mutanter (genmuterte bakterier) av S. mutans som mangler ulike GTF og derved har redusert glukanproduksjon (23, 24). Biofilmer med mutanter ble sammenlignet med biofilmer som inneholdt den opphavlige, uforandrete S. mutans. Adhesjon og vekst av organismene, biofilmenes mikrobielle sammensetning, struktur og diffusjonsegenskaper samt utvikling av karies i bovine emaljeskiver under biofilmen ble undersøkt (23, 24).
Motsatt vanlig oppfatning fremmet ikke GTF og mutan (uløselig glukan) initial adhesjon av S. mutans eller dens evne til videre kolonisering (23). Mutan påvirket heller ikke den mikrobielle sammensetningen i biofilmene (23). Inkorporering av en gtfC knock-out mutant av S. mutans (OMZ 937) i biofilmer økte derimot volumandelen celler og reduserte volumandelen EPS dramatisk sammenlignet med biofilmer som inneholdt S. mutans (UA 159) som illustrert i Figur 4a (24). Volumandelen celler og EPS i biofilmer som inneholdt S. mutans var i gjennomsnitt henholdsvis 29 % ( 6,7 %) og 48 % ( 12 %), mens i biofilmer med gtfC-negativ S. mutans var gjennomsnittlig cellevolum 51 % ( 13 %) og EPS-volumet 33 % ( 6,0 %). Forskjellene i volumandel celler og EPS var statistisk signifikante (N = 10; uparet t-test; p £ 0,002). Tykkelsen på biofilmene var for øvrig den samme. Dette førte til en kraftig økning av diffusjonshastigheten i biofilmer som inneholdt mutanten som vist i Figur 4b (24). Sammenlignet med biofilmer som inneholdt S. mutans var diffusjonskoeffisienten for 70-kD dextran 16x høyere i biofilmer som inneholdt gtfC-negativ S. mutans, i gjennomsnitt henholdsvis 0,46 m2 per sekund og 7,2 m2 per sekund. Disse funn støtter at mutan fungerer som en diffusjonsbarriere i plakk (21). Motsatt vanlig oppfatning var den kariogene evnen til mutanten ikke redusert (23).
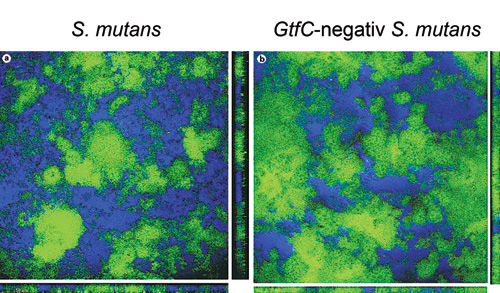
Figur 4a. Volumfordeling av celler og EPS i 6-species biofilmer som inneholdt enten S. mutans (a) eller gtfC-negativ S. mutans (b). Mikroorganismer (grønne) farget med Syto 13 og EPS (blå) farget med Calcofluor. (Fra referanse 24)
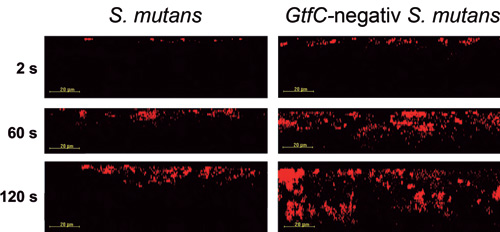
Figur 4b. Diffusjon av 70-kD dextran i 6-species biofilmer som inneholdt enten S. mutans (til venstre) eller gtfC-negativ S. mutans (til høyre) etter 2, 60 og 120 sekunder inkubasjonstid. (Fra referanse 24)
Det synes som om betydningen av streptokokk-glukaner for plakkdannelse basert på forsøk med planktoniske streptokokker i renkulturer er overvurdert. Våre funn tyder også på at vår kunnskap om betydningen av EPS for kariesutvikling fremdeles er begrenset. Fremtidige biofilmstudier vil gjøre det mulig å undersøke nærmere betydningen av EPS for plakkets patogenisitet. Likeledes vil fremtidige studier belyse effekten av EPS på biofilmenes følsomhet for antimikrobielle stoffer.
Modellen som pålitelig mål for effekten av antimikrobielle midler
I mange tiår er effekten av antimikrobielle midler for oral bruk blitt undersøkt ved klassiske tester med renkulturer av planktoniske bakterier. I slike tester, hvor midlet er kontinuerlig til stede i vekstmediet, hemmes bakterievekst av konsentrasjoner som er 100 -1 000x lavere enn de som kreves for å redusere plakkdannelse. Disse testene kan brukes for å sammenligne effekten av ulike stoffer, men egner seg ikke til å forutsi klinisk effekt. Det er flere grunner til dette, bl. a. at den korte eksponeringstiden til plakk av munnpleiemidler (< 3 minutter/dag) fører til gjenvekst av bakterier mellom bruk og om natten. I tillegg er bakterier som vokser i biofilmer mindre følsomme overfor antimikrobielle stoffer enn planktoniske bakterier (6). I biofilmmodellen etterligner vi bruk av munnskyllevæsker ved å dyppe biofilmene i antimikrobielt middel tre ganger daglig i ett minutt. Langtidseffekten evalueres ved at vi undersøker biofilmene 16 timer etter siste dypp i midlet. Dette er viktig fordi små forskjeller i antallet overlevende bakterier som formerer seg, kan føre til store variasjoner i bakterietallet mellom munnskyllinger.
Biofilmers følsomhet for antimikrobielle midler avhenger bl. a. av bakterienes veksthastighet (6). Standardmodellen med 70 % saliva i vekstmediet ble funnet velegnet til å skille mellom effekten av klorheksidinløsninger i konsentrasjoner som brukes i klinikken (Figur 5a) (25). Det er veldokumentert at 0,2 % klorheksidin hemmer effektivt plakkdannelse og at 0,1 % klorheksidin har en litt svakere effekt, men ikke alltid statistisk signifikant forskjellig. Munnskyllevæsken Corsodyl (SmithKline Beecham) som inneholder 0,2 % klorheksidin hemmet biofilmvekst tilsvarende den rene klorheksidinløsningen.
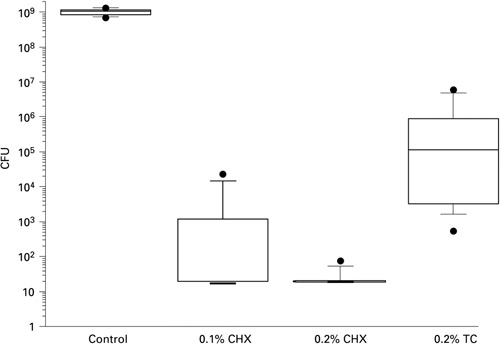
Figur 5a. «Box plots» viser effekten av 0,1 % og 0,2 % klorheksidin (CHX) samt 0,2 % triklosan (TC) på biofilmdannelse sammenlignet med vann (kontroll; N = 9). Biofilmene ble eksponert for testløsning eller vann 3 x daglig i 1 minutt og høstet etter 64,5 timer. Hver boks angir nedre og øvre kvartil (25 % til 75 % av verdiene), den horisontale linjen i boksen medianverdien, de horisontale linjene utenfor boksen 10 % og 90 % percentiler, sirklene antyder utenforliggende verdier. I de tilfellene hvor bokser ikke har «medianstrek» faller medianverdien sammen med nedre kvartil. Forskjellene mellom kontroll og alle testløsninger var statistisk signifikante på 99,9 % nivå. Forskjellene mellom testløsningene var ikke statistisk signifikante. CFU = Colony-forming units. (Fra referanse 1)
Effekten av 12 munnskyllevæsker på markedet i Europa ble testet i standardmodellen (25). Samtlige reduserte biofilmvekst statistisk signifikant sammenlignet med vann. Et utsnitt av resultatene vises i Figur 5b. Munnskyllevæskene inneholdt triklosan (Colgate total), naturlige oljer (Listerine), tinnfluorid og aminfluorid (Meridol), klorheksidin (Clorhexamed), hexetidin (Hexoral) og octenidin (Octenisept). Resultatene stemte med plakkhemmende effekt rapportert i tidligere kliniske forsøk (25). Dette er for tiden den eneste in vitro-modellen som er egnet til å vurdere effekten av antimikrobielle stoffer i klinisk relevante konsentrasjoner. Modellen er således et verdifullt og økonomisk redskap for preklinisk utprøving av nye produkter.
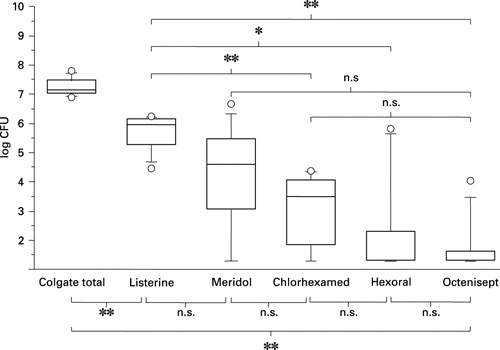
Figur 5b. «Box plots» viser log10 totale CFU (N = 9) fra biofilmer som ble eksponert for kommersielle munnskyllevæsker 3 x daglig i 1 minutt og høstet etter 64,5 timer. Forskjellen mellom behandlinger var statistisk signifikant ved parvis sammenligning på 99 % (**) eller på 95 % nivå (*). n.s. = ikke statistisk signifikant. (Fra referanse 1)
Effekt av xylitol på biofilmdannelse
Xylitol og sorbitol er begge tannvennlige sukkersubstitutter, men xylitol er også blitt tillagt anti-kariogene, altså terapeutiske, egenskaper. Denne effekten har vært omstridt helt siden de velkjente «Turku sugar studies» i 1975. Xylitol metaboliseres ikke av plakkbakterier og gir ikke syreproduksjon i plakk. Det er blitt hevdet at bruk av xylitol har flere kliniske fordeler fremfor bruk av sorbitol, bl. a. at xylitol reduserer adhesjon av mutans-streptokokker og syreproduksjon i plakk, bakterievekst og plakkmengde, samt karies ved å stimulere salivasekresjonen (26). Biofilmmodellen syntes velegnet til å vurdere om den energikrevende prosessen som kalles «futile xylitol cycle» – opptak, akkumulering og utskillelse av xylitol uten at bakteriene kan nyttiggjøre seg det – kan forklare den påståtte reduksjonen av mutans-streptokokker (S. mutans eller S. sobrinus) i plakk.
«Feast and Famine»-modellen ble her brukt, dvs. biofilmene vokste i saliva og ble tilført «måltider» med glukose og sukrose tre ganger daglig i 45 minutter. Før eller etter «måltidene» ble biofilmene eksponert for enten xylitol, sorbitol eller saliva (kontroll) i 20 minutter. Vi undersøkte til sammen åtte xylitol-sensitive mutans-streptokokker med normal «futile cycle»-aktivitet eller xylitol-resistente mutans-streptokokker med lav eller ingen slik aktivitet. Biofilmene ble eksponert til sammen seks ganger i løpet av to dager og dyrket på uspesifikke og spesifikke agarmedier etter 64,5 timer, hvoretter det totale antallet mikroorganismer, streptokokker, mutans-streptokokker og S. oralis ble telt (27).
Xylitol reduserte ikke antallet levende bakterier i biofilmene enten det ble tilført før eller etter «måltider» som vist i Figur 6 for en av de undersøkte S. mutans med normal «futile cycle»- aktivitet. Resultatene var de samme for xylitol-sensitive og xylitol-resistente mutans-streptokokker (27). Våre funn støtter ikke påstanden om at xylitol reduserer eller eliminerer mutans-streptokokker i plakk ved «futile cycles». Dette er vist under ufysiologiske betingelser hvor planktoniske renkulturer av S. mutans først vokste med høye konsentrasjoner av xylitol som eneste energikilde og deretter ble tilført glukose i lave konsentrasjoner (28). Mangel på samsvar med tidligere publiserte in vitro data kan derfor lett forklares med at vi eksponerte multispecies-biofilmer og ikke planktoniske bakterier for xylitol under realistiske betingelser, dvs. for begrensete tidsrom og i rimelige konsentrasjoner.
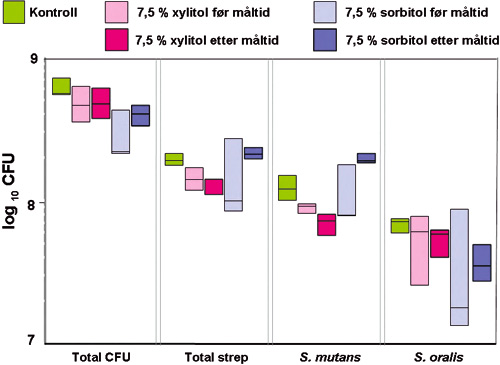
Figur 6. Effekten av 7,5 % xylitol eller 7,5 % sorbitol sammenlignet med saliva (kontroll) gitt før eller etter «måltider» på vekst av 6-species biofilmer som inneholdt S. mutans OMZ 918. «Box plots» (N = 3) viser det totale antallet mikroorganismer (Total CFU), streptokokker (Total strep), S. mutans og S. oralis som log10 CFU. Merk at y-aksen dekker kun to log-trinn.
De- og remineralisering av bovin emalje under biofilm
Modellen er også brukt til å studere de- og remineralisering av bovine emaljeskiver under biofilmen. De- og remineralisering måles ved «Quantitative Light-induced Fluorescence» (QLF). Denne teknikken ble opprinnelig utviklet til bruk for målinger på tannoverflater i munnen, men ble tilpasset til bruk in vitro (29). QLF er en sensitiv, ikke-destruktiv, optisk metode som bruker tennenes (spesielt dentinets) naturlige fluorescens til å skille mellom karies og frisk emalje, og til å måle lesjonens grad og utbredelse. Ved demineralisering reduseres fluorescensen, og ved remineralisering øker den. Bildeanalyser gir et kvantitativt mål for endring i mineralinnholdet. Differansen i fluorescens uttrykkes i % som delta F.
I demineraliseringsstudier kan vi studere effekten av regimer som reduserer kariesutvikling, kariesfremmende evne av ulike mikrobielle samfunn, patogenisiteten til enkle bakteriearter og ulike karbohydraters kariesfremmende evne som omtalt senere for stivelse.
For å studere remineralisering demineraliseres emaljeskivene først in vitro ved bruk av syregel. Figur 7 viser remineralisering av emaljeskiver under biofilm i standardmodellen. Her ble skivene behandlet med CaCl2 (29). Slike studier tillater å undersøke effekten av behandlinger som kan fremme remineralisering, f. eks. fluorforbindelser eller kostfaktorer.
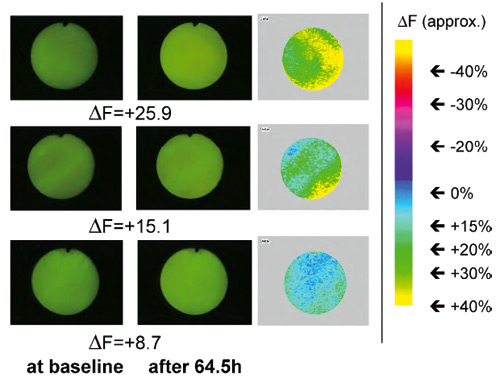
Figur 7. Remineralisering av bovine emaljeskiver under biofilmer etter 64,5 timer. Kolonnen til venstre viser QLF-bilder (QLF = quantitative light-induced fluorescence) av tre emaljeskiver demineralisert med syregel in vitro til delta F ca. - 30 %. QLF-bildene i midten viser skivene etter remineralisering under biofilm. Skivene ble behandlet med 15 mM (øverst), 10 mM (i midten) eller 5 mM CaCl2 (nederst). D F angir i prosent økningen i mineralinnhold i forhold til utgangspunktet. Til høyre sees bildeanalyser som angir nøyaktig sted på emaljeskivene med remineralisering i forhold til fargeskalaen. (Fra referanse 29)
Bruk av in vitro-QLF er også velegnet til å studere de- og remineralisering av bovin emalje under biofilmer dannet in situ. Figur 8a viser en intraoral kariesmodell som bæres av forsøkspersoner dag og natt i 10-døgns perioder (10). I demineraliseringsstudier eksponeres emaljeskivene for sukkerløsning ekstraoralt, og i remineraliseringsstudier benyttes emaljeskiver pre-demineralisert in situ eller med syregel in vitro. Figur 8b viser emaljeskiver eksponert for sukkerløsning åtte ganger daglig i 10 minutter og for enten vann eller 0,1 % NaF to ganger daglig i ett minutt. Som ventet hemmet fluorid signifikant utvikling av demineralisering sammenlignet med vann. Gjennomsnittlig delta F ble -11 % ( 6,6 %) for vann og -3,1 % ( 2,5 %) for NaF (N = 6; p = 0,02) (29).
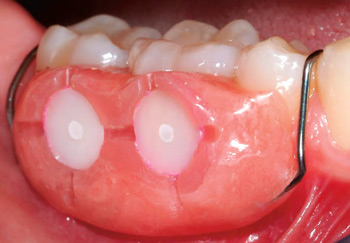
Figur 8a. Intraoral kariesmodell hvor bovine emaljeskiver festes i akrylplater. De hvite områdene sentralt er neglelakk som dekker et referanseområde for kontroll. Hver forsøksperson bærer to plater i munnen dag og natt i de- og remineraliseringsstudier. (Foto: Jørgen Barth)
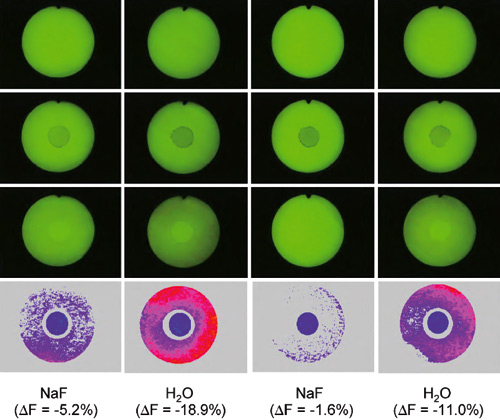
Figur 8b. QLF-bilder av demineralisering utviklet under biofilmer in situ etter 10 døgn. Emaljeskivene ble eksponert for sukkerløsning ekstraoralt 8 x daglig og for testløsning (0,1 % NaF) eller kontroll (vann) morgen og kveld. De to øverste rekkene viser 4 tannbiter målt med QLF før (øverst) og etter påføring av neglelakk (under). Den tredje rekken viser de samme tannbitene etter in situ eksperimentet. Nederst vises bildeanalyser med blått referanseområde i midten og farget ytre testområde. Fiolette områder er minst demineralisert; røde områder mest demineralisert. (Fra referanse 29)
Fordi QLF tillater å lokalisere nøyaktig demineraliserte og remineraliserte områder på eksperimentelle emaljeskiver, kan vi nå kombinere QLF med immunfluorescens eller FISH og identifisere og analysere mikrofloraen i direkte relasjon til disse områdene in vitro og in situ. Dette åpner mulighet for å utvikle nye strategier som kan interferere spesifikt med mikrofloraen assosiert med initial kariesutvikling.
Stivelse og kariogenisitet
Helt siden Miller lanserte den kjemo-parasittære teorien på slutten av 1800-tallet, har den kariesfremmende evnen til stivelse vært et debattert tema. Stivelse var mindre kariogent enn glukose, fruktose og sukrose (30). Dette forklares ved at streptokokker, spesielt mutans-streptokokker, ikke produserer EPS fra stivelse. Det er postulert at stivelse fører til redusert kolonisering av mutans-streptokokker i plakk og derved mindre syrepotensial (31). Vår hypotese var at redusert kariesutvikling av stivelse sammenlignet med sukrose ikke skyldes forandring i plakkets mikroflora, men at stivelse påvirker biofilmenes struktur og derved deres diffusjonsegenskaper. Dette ble studert i biofilmmodellen (32, 33).
I disse forsøkene vokste biofilmer med glukose+sukrose (0,5 %+0,5 %), glukose+sukrose+stivelse (0,25 %+0,25 %+0,5 %) eller med stivelse alene i vekstmediet i en total konsentrasjon på 1 % (32, 33). Ved dette høye karbohydratinnholdet, og følgelig lave pH-verdier i vekstmediet, ble antallet CFU lavere enn i standardmodellen, men ikke antallet S. sobrinus som er syretolerant og V. dispar som fermenterer laktat. Det var bemerkelsesverdig at antallet streptokokker og S. sobrinus viste stor variasjon i biofilmer som vokste bare med stivelse som karbohydratkilde sammenlignet med de andre kombinasjonene av karbohydrater (32).
Emaljen ble mindre demineralisert under biofilmer som vokste bare med stivelse sammenlignet med de andre kombinasjonene av karbohydrater (32). Gjennomsnittlig delta F ble -27 % ( 5,5 %) ved glukose+sukrose, ved glukose+sukrose+stivelse -19 % ( 2,6 %) og ved stivelse alene -13 % ( 3,3 %). Forskjellene i demineralisering var statistisk signifikante (N = 9; paret t-test; p £ 0,002). Dette kunne ikke forklares med endret sammensetning av mikrofloraen ved de ulike karbohydratkildene. Innholdet av amylase og pH i vekstmediene ble også målt. pH i vekstmediet varierte mellom 4,6 ved glukose+sukrose, ved glukose+sukrose+stivelse 4,7 og 4,8 ved kun stivelse. Lavere syreproduksjon ved stivelse er av betydning, men kunne neppe forklare den svake demineraliseringen. Forskjellene kunne heller ikke forklares med lavt innhold av enzymet amylase (32).
Biofilmenes struktur ble derimot vesentlig endret ved stivelse sammenlignet med glukose+sukrose. Volumandelen celler i biofilmer som vokste med glukose+sukrose var i gjennomsnitt 61 % og med stivelse alene 73 % (33). Volumandelen EPS minket dramatisk ved stivelse alene i vekstmediet. Biofilmene inneholdt gjennomsnittlig 20 % EPS ved glukose+sukrose, 9,3 % ved glukose+sukrose+stivelse og bare 3,8 % ved stivelse (33). Forskjellene i EPS-innholdet påvirket diffusjonshastigheten av makromolekyler i betydelig grad. 70-kD dextraner diffunderte dobbelt så hurtig gjennom biofilmene ved bare stivelse som ved glukose+sukrose. Gjennomsnittlig diffusjonskoeffisient for 70-kD dextran var 3,2 m2 per sekund ved glukose+sukrose og 6,5 m2 per sekund ved stivelse (33). Mindre kariesutvikling av stivelse i forhold til glukose+sukrose skyldes sannsynligvis flere faktorer, men biofilmenes ulike struktur og diffusjonsegenskaper synes å spille en vesentlig rolle.
Avsluttende bemerkninger
Vår in vitro multispecies-biofilmmodell er reproduserbar og pålitelig. Den kan brukes til å studere basale og praktiske problemer som ikke kunne studeres tidligere. Bruk av orale biofilmmodeller kombinert med moderne analytiske teknikker gjør det mulig å studere biofilmers struktur og funksjoner på en måte som ikke var mulig med organismer i planktonisk tilstand. Orale biofilmmodeller har selvfølgelig begrensninger sammenlignet med «in vivo-situasjoner», og forskjellige biofilmmodeller som brukes til plakkstudier har sine fordeler og svakheter. Slike modeller er likevel den beste tilnærming til dentalt plakk in vivo. Oral biofilmforskning åpner en ny dimensjon innen oral biologi med fremtidig betydning for forebyggende tannpleie.
Vi har hovedsakelig stilt spørsmål ved konsepter som stammer fra studier av monospecies-biofilmer innen generell medisin eller fra studier med planktoniske orale bakterier under ufysiologiske betingelser. Våre studier har vist at orale biofilmer har egenskaper som er helt forskjellig fra monospecies-biofilmer studert i generell medisin. Flere funn som er gjort der kan ikke overføres til orale biofilmer, f. eks. er kanaler ikke til stede i multispecies orale biofilmer.
Det er i dag allment akseptert at biofilmer med svært forskjellige egenskaper dannes i ulike omgivelser, og at vekstbetingelsene er av avgjørende betydning (34). Prinsipielt kan alle bakterier, ikke bare de orale, adherere til pellikelen. Ikke-orale bakterier kan imidlertid ikke konkurrere og vokse i munnen. Vår hypotese er at bakterier som finnes i plakket senere, f. eks. subgingivale bakterier, «går i dvale» (overlever i lavt antall) og vokser bare hvis deres vekstbetingelser oppfylles. Fremtidige in vitro multispecies-biofilmstudier og kliniske studier av dentalt plakk må utføres for å kunne bekrefte denne hypotesen.
English summary
Giertsen E.
Oral biofilm models – a new approach for plaque studies
794-802.
The term oral biofilm is increasingly replacing "plaque" in the literature, but concepts and existing paradigms are changing much more slowly. There is little doubt that biofilm research will lead to more realistic perception and interpretation of the physiology and pathogenicity of microorganisms colonizing plaques in the oral cavity. There is clear evidence that the genotypic and phenotypic expression profiles of bacteria growing in biofilms are different from those of planktonic bacteria. Several techniques are available today to study multispecies biofilms of oral bacteria, each having its particular advantages and weaknesses. This paper describes a biofilm model and demonstrates a number of applications with direct or indirect impact on prophylactic dentistry: spatial arrangement and associative behavior of various species in biofilms; multiplex fluorescent in situ hybridization analysis of oral bacteria in biofilms; mass transport in biofilms and importance of extracellular polysaccharides; use of the biofilm model to predict reliably in vivo efficacy of antimicrobials; effects of xylitol on mutans streptococci in biofilms; de- and remineralization of enamel exposed to biofilms in vitro or in situ; cariogenicity of starch. The potential of biofilm experimentation in oral biology has certainly not yet been fully exploited and dozens of possible interesting applications could be investigated. The overall physiological parameters of multispecies biofilms can be measured quite accurately, but it is still impossible to assess in toto the multitude of interactions taking place in such complex systems. What can and should be done is to test hypotheses stemming from experiments with planktonic cells in monospecies cultures. In particular, it will be interesting to investigate further the relevance to biofilm composition and metabolism of specific gene products by using appropriate bacterial mutants.
Takk
Figurene som tidligere er publisert i Caries Research, er trykket med tillatelse av S. Karger AG, Basel. Figurene som tidligere er publisert i Clinical Oral Investigations, er trykket med tillatelse av Springer Science and Business Media. Takk til Knut Erik Buanes ved Det odontologiske fakultet, Universitetet i Bergen for redigering av figurene.
Hovedbudskap | |
|---|---|
Hva vår biofilmforskning har ført til så langt: |
|
• |
Den har stilt spørsmål ved mange teorier som stammer fra eksperimenter med planktoniske bakterier |
• |
Den har vist redusert betydning av spesifikk mikrobiell adhesjon og at vekstbetingelser har vesentlig betydning for plakkdannelse |
• |
Den har satt spørsmålstegn ved den betydning glukosyltransferase og glukaner fra streptokokker har for plakkdannelse og kariesutvikling |
• |
Den har understreket at diffusjonsegenskaper i biofilmer har stor betydning for utvikling av karies |
Referanser
1. Guggenheim B, Guggenheim M, Gmür R, Giertsen E, Thurnheer T. Application of the Zürich biofilm model to problems of cariology. Caries Res 2004; 38: 212–22.
2. ten Cate JM. Biofilms, a new approach to the microbiology of dental plaque. Odontology 2006; 94: 1–9.
3. Costerton JW, Lewandowski Z, deBeer D, Caldwell D, Korber D, James G. Biofilms, the customized microniche. J Bacteriol 1994; 176: 2137–42.
4. Costerton JW, Lewandowski Z, Caldwell DE, Korber DR, Lappin-Scott HM. Microbial biofilms. Annu Rev Microbiol 1995; 49: 711–45.
5. Davies DG, Parsek MR, Pearson JP, Iglewski BH, Costerton JW, Greenberg EP. The involvement of cell-to-cell signals in the development of a bacterial biofilm. Science 1998; 280: 295–8.
6. Gilbert P, Das J, Foley I. Biofilm susceptibility to antimicrobials. Adv Dent Res 1997; 11: 160–7.
7. Marsh PD. Microbial ecology of dental plaque and its significance in health and disease. Adv Dent Res 1994; 8: 263–71.
8. Thurnheer T, Gmür R, Guggenheim B. Multiplex FISH analysis of a six-species bacterial biofilm. J Microbiol Methods 2004; 56: 37–47.
9. Guggenheim B, Giertsen E, Schüpbach P, Shapiro S. Validation of an in vitro biofilm model of supragingival plaque. J Dent Res 2001; 80: 363–70.
10. Giertsen E, Guggenheim B, Thurnheer T, Gmür R. Microbiological aspects of an in situ model to study effects of antimicrobial agents on dental plaque ecology. Eur J Oral Sci 2000; 108: 403–11.
11. Liljemark WF, Bloomquist C. Human oral microbial ecology and dental caries and periodontal diseases. Crit Rev Oral Biol Med 1996; 7: 180–98.
12. Kolenbrander PE, Andersen RN, Kazmerak KM. Coaggregation and coadhesion in oral biofilms. In: Allison DG, Gilbert P, Lappin-Scott HM, editors. Community structure and co-operation in biofilms. Cambridge: Cambridge University Press; 2000. p. 65–85.
13. Kolenbrander PE, London J. Adhere today, here tomorrow: Oral bacterial adherence. J Bacteriol 1993; 175: 3247–52.
14. Guggenheim M, Shapiro S, Gmür R, Guggenheim B. Spatial arrangements and associative behavior of species in an in vitro oral biofilm model. Appl Environ Microbiol 2001; 67: 1343–50.
15. Guggenheim B, Wyss C, Gmür R. The Zürich biofilm model extended to subgingival microbiota. J Dent Res 2007; 86 (Spec Iss A): Abstract 1303.
16. Davey ME, O"Toole GA. Microbial biofilms: from ecology to molecular genetics. Microbiol Mol Biol Rev 2000; 64: 847–67.
17. Donlan RM, Costerton JW. Biofilms: survival mechanisms of clinically relevant microorganisms. Clin Microbiol Rev 2002; 15: 167–93.
18. Thurnheer T, Gmür R, Shapiro S, Guggenheim B. Mass transport of macromolecules within an in vitro model of supragingival plaque. Appl Environ Microbiol 2003; 69: 1702–9.
19. Hall-Stoodley L, Stoodley P. Developmental regulation of microbial biofilms. Curr Opin Biotechnol 2002; 13: 228–33.
20. Guggenheim B. Extracellular polysaccharides and microbial plaque. Int Dent J 1970; 20: 657–78.
21. Ooshima T, Matsumura M, Hoshino T, Kawabata S, Sobue S, Fujiwara T. Contributions of three glucosyltransferases to sucrose-dependent adherence of Streptococcus mutans. J Dent Res 2001; 80: 1672–7.
22. Banas JA, Vickerman MM. Glucan-binding proteins of the oral streptococci. Crit Rev Oral Biol Med 2003; 14: 89–99.
23. van der Ploeg JR, Guggenheim B. Deletion of gtfC of Streptococcus mutans has no influence on the composition of a mixed-species in vitro biofilm model of supragingival plaque. Eur J Oral Sci 2004; 112: 433–8.
24. Thurnheer T, van der Ploeg JR, Giertsen E, Guggenheim B. Effects of Streptococcus mutans gtfC deficiency on mixed oral biofilms in vitro. Caries Res 2006; 40: 163–71.
25. Shapiro S, Giertsen E, Guggenheim B. An in vitro oral biofilm model for comparing the efficacy of antimicrobial mouthrinses. Caries Res 2002; 36: 93–9.
26. Twetman S, Holgersen PL. Xylitol für die Kariesprävention – einige praktische Aspekte und Richtlinien. ZWR 2004; 113: 265–8.
27. Giertsen E, Guggenheim B. Effect of xylitol on survival of mutans streptococci in biofilms. J Dent Res 2005; 84 (Spec Iss A): Abstract 1506.
28. Assev S, Rølla G. Further studies on the growth inhibition of Streptococcus mutans OMZ 176 by xylitol. APMIS 1986; 94: 97–102.
29. Gmür R, Giertsen E, van der Veen MH, de Josselin de Jong E, ten Cate JM, Guggenheim B. In vitro quantitative light-induced fluorescence to measure changes in enamel mineralization. Clin Oral Invest 2006; 10: 187–95.
30. Rugg-Gunn AJ, Nunn JH. Nutrition, diet and oral health. Oxford: Oxford University Press; 1999.
31. Newbrun E, Finzen F, Sharma M. Inhibition of adherence of Streptococcus mutans to glass surfaces. Caries Res 1977; 11: 153–9.
32. Guggenheim B, Gmür R, Giertsen E. Starch: Effect on microbial composition and demineralization potential of biofilms. J Dent Res 2005; 84 (Spec Iss A): Abstract 1509.
33. Thurnheer T, Guggenheim B. Influence of starch on structure and diffusion properties of biofilms. J Dent Res 2005; 84 (Spec Iss A): Abstract 1510.
34. Klausen M, Heydorn A, Ragas P, Lambertsen L, Aaes-Jørgensen A, Molin S, et al. Biofilm formation by Pseudomonas aeruginosa wild type, flagella and type IV pili mutants. Mol Microbiol 2003; 48: 1511–24.
Adresse: Elin Giertsen, postboks 1109, Blindern, 0317 Oslo. E-postadresse: Elin.Giertsen@odont.uio.no
Artikkelen har gjennomgått ekstern faglig vurdering.