Implantatens livslängd beroende av stödbehandlingen
Författare
dr odont, specialtandläkare i klinisk tandvård (parodontologi), seniorforskare. Institutionen för odontologi, Helsingfors universitet
lic odont, specialtandläkare i klinisk tandvård (protetik och bettfysiologi), privattandläkare, utbildare
professor i oral biologi. Institutionen för odontologi, Kliniken för mun- och käksjukdomar, HUCS, Helsingfors universitet
Trots att korrekt installerade tandimplantat förväntas bevara sin funktion länge, visar uppföljningsstudier att olika biologiska och/eller mekaniska komplikationer förekommer hos nästan 40 procent av patienterna redan under de fem första åren efter installationen. Den bakteriella kolonisationen av implantaten kan leda till peri-implantära inflammationer, peri-implantär mukosit och peri-implantit. Vid peri-implantär mukosit begränsas inflammationen till angränsande mjukvävnad, medan peri-implantit också orsakar benförlust runt implantaten. På senare tid har man börjat inse att implantatens överlevnad är i hög grad beroende av god munhygien och regelbunden stödbehandling. Enligt ny forskning förekommer biologiska, inflammatoriska komplikationer i mindre utsträckning hos sådana patienter som årligen gått på kontroll än hos sådana, som uppsökt vård först när komplikationer har uppstått. Det primära målet för stödbehandlingen av implantat är att förebygga peri-implantära sjukdomar, eller att behandla dem på ett tidigt stadium, samt att reparera tekniska fel, som uppstått i implantatkonstruktionerna. Trots att forskningen inte har presenterat data för hur optimal stödbehandling vid implantat ska genomföras, kan man förmoda att samma principer som gäller för stödbehandling vid parodontit också gäller här. Vid varje besök för stödbehandling av tandimplantat mäts djupet på implantatfickorna och förekomsten av blödning och/eller pus vid mätningen av fickdjupen registreras. Om fickorna har blivit djupare jämfört med föregående besök, är radiologisk verifiering av diagnosen indicerad. Beroende på vävnadsskadans stadium, behandlas peri-implantatsjukdomarna med mekanisk rengöring och lokal desinfektion, som vid behov kombineras med systemisk antibiotika och/eller kirurgiska åtgärder.
Redan när ett implantatingrepp planeras och genomförs, bör alla riskfaktorer som gäller patienten beaktas med syfte att bevara vävnadernas hälsa och för att undvika komplikationer. För att garantera en god långtidsprognos för implantatkonstruktionerna, bör alla implantatpatienter få ett individuellt, långsiktigt behandlingsprogram som betonar patientens eget ansvar för munhygien, rökvanor och stödbehandling.
Stödbehandling betyder i detta sammanhang professionell vård av tandläkare och/eller tandhygienist i syfte att bevara tänder eller tandimplantat och att befrämja frisk stödjevävnad kring dem. När det gjelder naturliga tänder är målet att bevara det resultat som uppnåtts med aktiv vård och att förhindra recidiverande inflammationer och progressiv vävnadsnedbrytning. Stödbehandling utgör en viktig del av den parodontologiska behandlingen, och dess betydelse har påvisats i flera kliniska studier (1, 2, 3). Frekvensen för stödbehandling är individuell och beror på patientens sjukdomsstatus, benägenhet för parodontit, kooperation och risknivån (4, 5). Vid tandläkarbesöken kontrolleras nivån på patientens munhygien och förbättras vid behov. Om inflammationen recidiverat eller om vävnadsnedbrytningen progredierat, används icke-kirurgiska och/eller kirurgiska metoder för att stabilisera den orala situationen. Dessa principer följs också för stödbehandling av tandimplantat tills nya forskningsresultat eventuellt gör andra behandlingsscheman mer befogade.
Sedan den första kliniska rapporten om osseointegrerade implantat presenterades i slutet av 1970-talet (6) har implantaten blivit en väsentlig del av den rekonstruktiva odontologin. Framgång vid implantatbehandling har traditionellt mätts med lyckandefrekvens: hur länge implantatet överlever (survival). Ett implantat som är integrerat i benet och är kliniskt orörligt har ansetts utgöra ett lyckat behandlingsresultat. Enligt dessa kriterier har en överlevnadsfrekvens på 5–10 års uppföljning rapporterats vara utmärkt och överskrida 90 procent (7, 8). Kriterierna för lyckad implantatbehandling fastslogs första gången år 1986 (9). Då ansågs att benresorption på 1–1,5 mm under det första året efter belastning (early crestal bone loss, remodeing) och därefter mindre än 0,2 mm årligen är acceptabelt när det är fråga om traditionella maskinbearbetade (turned) tvåstegsinstallerade Brånemarkimplantat, med slät yta. Dessa kriterier för acceptabel benresorption runt implantatet kan dock inte tillämpas på moderna implantatkonstruktioner (10, 11), eftersom det marginala benet inte reagerar på samma sätt under det första året och någon benresorption knappast förekommer senare, om mjukvävnaden kring implantaten hålls fri från inflammation. Vid rapportering av lyckandefrekvens på lång sikt, har man knappast alls uppmärksammat hur vävnadsbarriären eller det estetiska resultatet har bevarats.
Med åren har marknaden översvämmats av olika slags implantat och implantatkomponenter från olika tillverkare. Alla moderna implantat har en ojämn yta. Implantatytans topografi och kemiska egenskaper varierar med implantatmärke. En ojämn titanyta främjar visserligen osseointegrationen, men är mer mottaglig för bakterieangrepp då den exponeras för munhålans mikroflora, än en slät yta (12, 13). När det gäller kontaktytan (interfasen) mellan implantatet och mjukvävnaden har inget implantatfabrikat visat sig vara bättre än något annat. Det förefaller inte heller ha någon betydelse om implantatet består av en eller två delar, om det installerats i ett eller två steg (submerged, non-submerged) eller om suprakonstruktionen är cementerad eller förankrad med skruv (14). För långtidsuppföljning är dessa uppgifter dock viktiga med tanke på utredning och behandling av eventuella sena komplikationer.
Trots att frekvensen för framgångsrik implantation enligt stabilitetskriteriet för implantat är hög, drabbas cirka 40 procent av patienterna av olika biologiska (inflammatoriska peri-implantatsjukdomar) och/eller mekaniska komplikationer (late failures) inom fem år (15, 16). Tidiga implantatförluster eller komplikationer (early loss/failures) inträffar redan innan de protetiska konstruktionerna utsätts för någon betydande mekanisk belastning, eller under implantatets första användningsår. Orsaken till de sena biologiska komplikationerna är oftast en inflammationsprocess i marginalområdena, som obehandlad kan leda till implantatförlust. De mekaniska komplikationerna utgörs av tekniska problem med implantatburna protetiska konstruktionerna. Man har till exempel konstaterat att till exempel överbelastning av bettet kan leda till fraktur av implantatets suprakonstruktioner eller till att skruven som fäster distansen eller kronan blir lös eller bryts av (17). Också själva implantatfixturen kan fraktureras, men detta är ovanligt. Forskningsdata om bitkraftens inverkan på osseointegrationen är motstridiga (18). I en del djurförsök har överbelastning av bettet lett till benresorption i marginalområdena (19) eller till större vävnadsnedbrytning, särskilt då överbelastningen är kombinerad med inflammation i peri-implantatvävnaden (20).
I takt med ökad klinisk erfarenhet har betydelsen av stödbehandling av implantaten för mjukvävnadens tillstånd och osseointegrationen framstått allt klarare. Det finns en del forskningsresultat om stödbehandlingens långtidseffekter, men forskningsdata saknas ännu, bland annat om stödbehandlingsfrekvens och om de munhygieniska åtgärder som är lämpliga för implantatburna konstruktioner (21). Enligt två nyligen publicerade svenska studier är inflammatoriska, plackrelaterade komplikationer mer sällsynta hos de implantatpatienter som regelbundet går på årliga kontroller än hos dem som uppsöker vård först då komplikationer uppkommer (22, 23, 24, 25).
Stödbehandlingsfasen anses börja först när implantatet har belastats i ett år. Målet är att bevara
1. frisk mjukvävnad runt implantatet
2. osseointegrationen, det vill säga intakt benstöd kring implantatet
3. balansen mellan munhålans bakterieflora och värdens immunrespons på den
4. en estetisk mjukvävnadskontur.
Det primära syftet med stödbehandlingen är att förhindra sena biologiska och mekaniska komplikationer eller att behandla dem i tid (26).
Mjukvävnaden kring implantat
Mjukvävnadsbarriär
Mjukvävnadsbarriären kring implant är särskilt betydelsefull när det gäller att skydda det osseointegrerade implantatets benfäste mot påverkan av munhålans mikrober, mot mekaniskt trauma vid restorativ vård, samt mot trauma förknippad med ocklusion, bitkrafter och munhygieniska åtgärder. Forskningsresultat visar att mjukvävnadsbarriären kring implantatet, den så kallade biologiska vidden (biological width), består av ett kontaktepitel (2 mm) och av en bindvävszon (1–1,5 mm). Histologiska undersökningar visar att den biologiska vidden i koronoapikal riktning i allmänhet är 3–4 mm. Den bevaras rätt konstant om de omgivande vävnaderna förblir friska (27, 28, 29). Denna sammanfogande epitelzon påminner om motsvarande vävnad hos naturliga tänder, medan bindvävsstrukturerna kring implantat inte är likadana som de som omger tänderna (figurerna 1 och 2). Avsaknad av parodontalligamentet och det supraalveolära fiberfästet, vertikalt förlopp av bindvävsfibrerna, relativt få fibroblaster och – i jämförelse med tänder – mindre cirkulerande blodmängd, kan försvaga mjukvävnadsbarriärens existens under en inflammationsprocess (30).
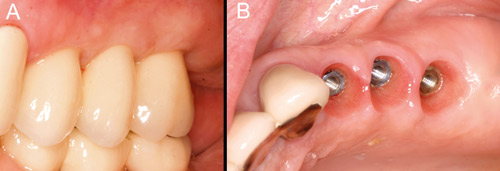
Figur 1. Kliniskt frisk mjukvävnad kring implantatkronor (A). Efter frisättning av suprakonstruktionerna ser man epitelzon kring varje implantat (B). (Foto: Marjatta Jokela).
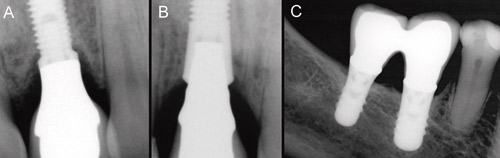
Figur 2. Röntgenbilder tagna efter det första belastningsåret. När den biologiska vidden och mjukvävnaderna stabiliseras, formas det alveolära benet enligt implantattypen och de anatomiska förhållandena. Under det aktuella tidsintervallet sker ofta för Brånemarkimplantat en remodellering av benet ända till skruvens första spiralvarv (A). Vid användingen av Astra- (B) och Straumann-implantat (C) kan någon marginell benremodellering knappt ses. Den marginala benkantens förlopp mellan den naturliga tanden och implantatet ger lätt ett intryck av en vertikal benficka, men det är fråga om helt normala omständigheter. (Foto: Marjatta Jokela).
Keratiniserad mukosa
Den keratiniserade slemhinnan som omger implantatet består av en lös marginal del och en vid benet fäst del. Den kan jämföras med det tandkött som normalt omger tänderna. Trots att en keratiniserad vävnadszon kan vara mindre känslig för mikrobiella angrepp, visar kliniska uppföljningsstudier att avsaknad eller förminskning (< 2 mm) av denna zon inte påverkar prognosen för implantatet om mjukvävnaderna är friska (31). Enligt en retrospektiv treårsstudie korrelerade en smal keratiniserad mukosazon inte med förlust av det alveolära benet, men jämfört med en bredare keratiniserad mukosazon (> 2 mm) var en smalare zon förenad med rikligare retention av plack samt mjukvävnadsinflammation, speciellt kring implantat i bakre delen av käken (32). Enligt sakkunniga och erfarna kliniker är det önskvärt att det finns keratiniserad mukosa runt implantatet, trots att inga tillgängliga forskningsdata påvisar dess betydelse (33). Vid implantatkirurgi används olika tekniker för att bevara och skapa en keratiniserad, fast mukosa (34).
Peri-implantatsjukdomar
Implantat, liksom naturliga tänder, är mottagliga för bakteriebiofilmens påvärkan. Bakteriebeläggningar utgör med tiden en stor risk inte endast för de peri-implantära mjukvävnaderna utan också för hela implantatbehandlingens prognos.
Peri-implantatsjukdomarna utgörs av de plackrelaterade tillstånden peri-implantär mukosit och peri-implantit. Vid peri-implantär mukosit begränsas inflammationen till mjukvävnaderna kring implantatet och kan jämställas med gingivit. Vid peri-implantit, som motsvarar parodontit, ses mjukvävnadsinflammation runt implantatet, men också resorption av det alveolära benet, det vill säga förlust av osseointegrationen (35). Vid peri-implantit ses ofta en skålformad benresorption runt hela implantatet, utom då en facial och/eller oral benlamell, som ursprungligen varit tunn, har resorberats helt (36). I båda fallen kan man röntgenologiskt se motsvarande angulära bendefekter i approximalytorna.
På ytan av ett nyligen installerat implantat är bakteriefloran till stor del densamma som den som koloniserar slemhinnan kring implantatet. Hos tandlösa patienter förekommer parodontitpatogener endast sällan på implantatytan och den mikrobiella floran består huvudsakligen av så kallad frisk bakterieflora. Om det finns naturliga tänder i munnen och om patienten tidigare har behandlats för parodontit och/eller har benägenhet för parodontit, är det sannolikt att bakterierna från tandköttsfickorna och tungans yta flyttar till implantatets yta (37). Plackmängden korrelerar positivt med peri-implantär mukosit och djupa implantatfickor (38). Patientens munhygien är alltså av avgörande betydelse för uppkomsten av peri-implantatinflammationer (39).
Enligt flera studier löper parodontitpatienter en något större risk för peri-implantatinflammation än de som inte har haft parodontit (40). På grund av rökning och/eller genetiska faktorer reagerar ett litet antal patienter otillfredsställande på adekvat parodontitbehandling. Dessa individer löper också en större risk för peri-implantit (41).
Floran i en frisk implantatficka är begränsad och består i huvudsak av aeroba bakterier. I peri-implantitfickorna däremot finns det rikligt med anaeroba parodontitpatogener, bland annat spirocheter, fusobakterier, Porphyromonas gingivalis och Prevotella intermedia. Ibland kan den dominerande floran vid peri-implantit bestå av andra bakterier än de som associeras med parodontit, till exempel tarmbakterier, Pseudomonas spp. och Staphylococcus aureus (42).
Främmande föremål i området runt implantatet (till exempel cementrester och upprispad tandtrådsfiber) kan också orsaka inflammatoriska reaktioner, antingen genom direkt vävnadsirritation eller genom ökad bakterieretention.
Förekomsten av peri-implantatsjukdomar
Peri-implantit uppfattades länge som en ganska ovanlig komplikation, eftersom prevalensen under 5–10 år av uppföljning uppgick till 0–14,4 procent av implantaten (8). Enligt nyligen publicerade studier är prevalensen för peri-implantit dock betydligt högre och uppgår till 28–56 procent bland implantatpatienterna. Resultaten beror på de kriterier som har använts för omfattningen av peri-implantär benförlust och förekomsten av infektionskännetecken samt implantatets funktionstid. Peri-implantär mukosit är rätt vanligt och har påvisats hos cirka 80 procent av implantatpatienterna (24, 25).
Peri-implantär mukosit är ett reversibelt tillstånd som kan behandlas. Däremot är osseointegrationsförlust i samband med peri-implantit så gott som irreversibelt. När osseointegrationen har förlorats helt blir implantatet rörligt och måste avlägsnas.
Kontroll av vävnaden runt implantat
När en patient kommer på stödbehandlingbesök, ber tandläkaren patienten bedöma hur implantatet fungerat. Klinisk undersökning utförs av såväl vävnaderna runt implantaten som för alla tänder, särskilt om patienten tidigare har haft parodontit. För denna kliniska bedömning bör nedan angivna omständigheter beaktas och registreras (41, 43, 44, 45).
Symtom och implantatrörlighet
Smärta förekommer sällan vid kronisk inflammation. Om patienten känner obehag i munnen eller misstänker att ett implantat är rörligt, är detta i första hand ett mekaniskt problem. Den vanligaste orsaken till rörligheten är att distans- och/eller broskruven, lossnat eller gått av. Ett vanligt kliniskt fynd vid skruvproblem är förändringar i mjukvävnaden, till exempel en fistel på samma höjd som skarven mellan implantatet och suprakonstruktionen. Det är viktigt att göra rätt differentialdiagnos mellan å ena sidan plackrelaterade inflammationsförändringar och å andra sidan lösa eller lossnade skruvar, cementrester, inkompatibilitet mellan implantatkomponenterna eller främmandekroppsreaktion (figur 3). Orsaken kan utredas bättre om konstruktionerna lösgörs och vid behov friläggs kirurgiskt. Också vid fasta broar kan det vara lättare att separat identifiera mobila implantat om suprakonstruktionen kan avlägsnas och tillståndet undersökas på fixturnivån. Avtagbara konstruktioner bör alltid noggrant rengöras och desinficeras innan de fästs på nytt. Man bör dock undvika att i onödan avlägsna konstruktioner och komponenter. Rörligheten är inget tidigt diagnostiskt tecken, eftersom implantat blir rörligt först då hela osseointegrationen gått förlorad.
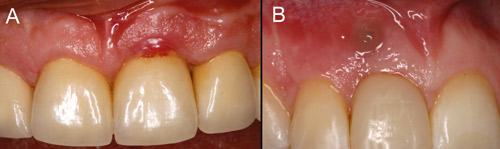
Figur 3. Inflammation i vävnaden runt implantat förorsakade av cementrester i marginalen till cementerad krona (A) och av lös skruv (B). (Foto: Marjatta Jokela).
Munhygien
Vid varje stödbehandlingsbesök kontrolleras funktion och nivå på patientens egenvård. Tandläkaren registrerar var det finns plack och tandsten samt i vilken omfattning. Supragingival tandsten förekommer oftast i underkäkens främre region. Om munhygienen är bristfällig, bör patienten informeras och instrueras i bättre munhygien och dess betydelse för implantatets långtidsprognos betonas (46). När implantatkonstruktionernas ytor är släta och glansiga, kan bakterier och tandsten lättare avlägsnas.
Hälsotillståndet hos peri-implantatvävnaderna
Den viktigaste metoden för en bedömning av vävnadernas tillstånd kring ett implantat är visuell granskning av mjukvävnaderna. Den friska peri-implantära slemhinnan är ljus till färgen och sluter tätt till implantatytan (figur 1). Om marginala inflammationsförändringar syns i de peri-implantära mjukvävnaderna (rodnad, svullnad, ödem) är detta ett tecken på en peri-implantatsjukdom (figur 4). Om patienten röker, kan det hindra upptäckten av sådana förändringar. Färgförändringar av slemhinnan kan vara följden av en patologisk process i käkbenet och detsamma gäller om slemhinnekanten drar sig tillbaka.
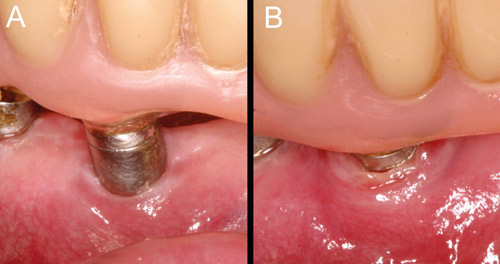
Figur 4. Frisk zon av mjukvävnad kring distansen till en implantatburen bro, med uppenbar avsaknad av fast keratiniserad mukosa (A). Uppföljning sju år efter installation: svullen mjukvävnad täcker distansen helt (B). Förmodligen har den anatomiska situationen med tiden försvårat patientens munhygien och bidragit till inflammationen. (Foto: Marjatta Jokela).
Mätning av implantatfickan
För bedömning och registrering av peri-implantatvävnadernas hälsa krävs mätning av fickdjupen vid varje stödbehandlingbesök. Djupen på implantatfickorna mäts på fyra eller sex ytor runt implantatet. Mätningen av dessa fickor är känsligare för den kraft som används än mätningen av naturliga tandköttsfickor. På basis av djurförsök rekommenderas en kraft på 20–30 g (0,2–0,3N) (47, 48). Om implantatfickans djup mäts från en fast referensnivå på suprakonstruktionen, blir det lättare att identifiera eventuella benförändringar under uppföljningen. Mätning med en sedvanlig fickdjupssond skadar inte kontaktepitelet och inte heller implantatets titanyta (49). Däremot finns det inga studier om eventuella skillnader i mätresultaten mellan sonder tillverkade av olika material.
Normalt är implantatfickans djup < 4 mm. Friska 4–5 mm djupa fickor, så kallade pseudofickor, är också möjliga. De kan uppkomma antingen av fixturens och suprakonstruktionernas anpassning till submukosan, mjukdelsplastik som gjorts av estetiska skäl eller av vävnadshyperplasi. Om fickan är 5 mm djup, skapas gynnsamma förhållanden för bakteriekolonisation, och om blödning uppstår när fickan sonderas, kan det vara ett tecken på begynnande peri-implantit. Redan ett avvikande mätningsresultat från en enda implantatyta kräver alltid en radiologisk bekräftelse på benkantens position. Utformningen av suprakonstruktionen, tjockleken på den omgivande slemhinnan, modellen på fixturen eller skruvens spiralvarv kan försvåra mätningen av implantatfickor med en rak sond. Då kan en furkationssond utgöra ett bra alternativ.
Blödning vid mätning av implantatficka (BOP)
För naturliga tänder är BOP (bleeding on probing) ett tecken på inflammation, men inte nödvändigtvis ett tecken på progredierande parodontitrelaterad vävnadsskada (50). Avsaknaden av blödning å andra sidan tyder på att läget är stabilt (51). I samband med implantat är BOP dock ett tecken på inflammation (52) (figur 5). BOP har också ett stort prognostiskt värde då det gäller progressionen av vävnadsdestruktion, särskilt samtidigt med någon patogen mikroorganism (53).
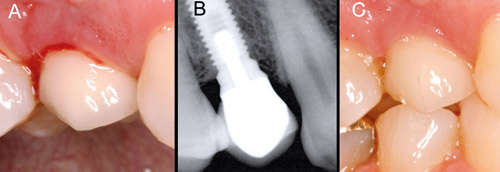
Figur 5. I samband med mätning av peri-implantatfickan ses blödning (A), men inga förändringar syns i bennivån (B). Diagnosen av denna förändring är således peri-implantär mukosit. Efter mekanisk rengöring och två veckors munsköljning med klorhexidin är inflammationen borta (C). (Foto: Marjatta Jokela).
Pusflöde
Pusflöde i samband med sondering av en implantatficka eller vid lätt tryck på slemhinnan, är alltid ett tecken på aktiv vävnadsdestruktion och på vårdbehov (figur 6). Pusflöde tycks förekomma i synnerhet hos rökare.
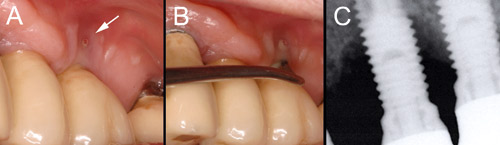
Figur 6. Uppföljning sex år efter installering av implantat för att ersätta d. 26 en fistel ses kliniskt vid implantatet (A). Fickdjupet mättes med en furkationssond, då den prominerande kronan begränsade användningen av en rak sond. Efter mätningen ses suppration från fickan och fisteln (B). I röntgenbilden ses en skålformad bendefekt som sträcker sig ända till skruvens nionde spiralvarv (C). Diagnosen är långt framskriden peri-implantit. (Foto: Marjatta Jokela).
Mikrobiologisk undersökning
Mikrobiologisk undersökning rekommenderas om kliniska och radiologiska tecken på peri-implantit har konstaterats. Odlingsresultatet kan utnyttjas vid vårdplaneringen (54).
Röntgenologisk undersökning
Röntgenologisk undersökning behövs för identifiering av förändringar i käkbenet. Begynnande benförändringar syns inte på konventionella röntgenbilder. Därför är det viktigt att man vid diagnostisering av begynnande peri-implantit utför en klinisk undersökning dvs. inspektion samt sondering och mätning av implantatsfickans djup. När det finns flera implantat eller implantatburna konstruktioner i munnen gär panoramaröntgen en helhetsbild. För att säkerställa diagnosen behövs standardiserade intraoralbilder med parallellteknik. För undersökning av bentillståndet i marginalområdet, behöver apikalregionerna inte nödvändigtvis synas på röntgenbilderna. Vid behov, till exempel vid så kallade sinuslyft (sinus lift), inspekteras de apikala delerna separat med andra lämpliga bildtekniker. I uppföljningsbilderna mäts benhöjden alltid från samma referenspunkt, till exempel implantatets skuldra. För att kunna identifiera förändringar i bennivån kan man även räkna antalet frilagda spiralvarv på skruven i det aktuella implantatet (figur 7). Om det inte förekommer synliga, kliniskt relevanta problem, rekommenderas röntgenfotografering av implantatet efter ett, tre och fem år och enligt kliniskt behov. I konventionella röntgenbilder syns endast de approximala ytornas eventuella benresorption. I särskilda fall är det möjligt att med hjälp av volymdatortomografi avbilda implantatets position i benet i tre dimensioner och att få information om benet också på de faciala/orala ytorna.
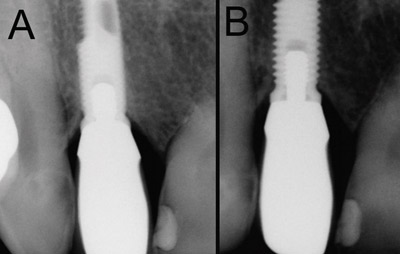
Figur 7. Röntgenbilder av samma implantat i olika projektioner. På bilden som tagits i sned projektion urskiljs spiralvarven inte ordentligt. Detta försvårar tolkningen av bilden, och en jämförelse mellan röntgenbilder tagna vid olika besök blir osäker (A). Vid användning av parallellprojektion framträder benkanten och implantatets spiralvarv tydligt (B). (Foto: Marjatta Jokela).
Bettundersökning
Bettundersökning hos implantatpatienter fokuserar på ocklusala och funktionella kontaktytor och eventuellt förändrade belastningsförhållanden i implantatkonstruktionerna. Belastningsförhållandena kan förändras, till exempel på grund av tandextraktioner och/eller framställning av nya protetiska konstruktioner. Eventuella prekontakter eller interferenser bör diagnostiseras och elimineras. Om slitfacetter förekommer eller tilltar, tyder detta på bruxism eller någon annan parafunktion som eventuellt kan kräva behandling med bettskena (figur 8).
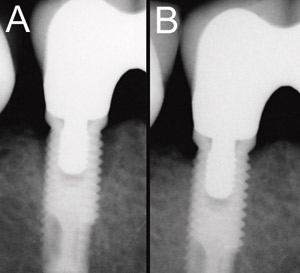
Figur 8. Efter tre års uppföljning ses benresorption kring det mest distala implantatet (reg. d. 45) av implantatburna bro, det vill säga förlust av osseointegration (A). Någon mätbar fördjupning av fickan konstaterades dock inte. Bettet som belastade implantatet balanserades genom att d. 47 försågs med en krona, och en ny delprotes samt en bettskena tillverkades för övre käken. Kontrollbilden ett år senare visar att bensituationen runt implantatet normaliserats (B). (Foto: Marjatta Jokela).
Behandling av peri-implantatsjukdomar
Det finns endast några få kontrollerade eller jämförande kliniska studier som behandlar upprätthållande av god vävnadshälsa runt implantat och behandling av sjukdomar i dessa vävnader (55). Några evidensbaserade behandlingsmetoder finns för närvarande inte beskrivna (56). Peri-implantit har behandlats med olika kända parodontologiska metoder, men det finns inga klara anvisningar om indikationerna för de olika metoderna (57, 58). Doktor Niklaus P Langs kumulativa behandlingsschema, Cumulative Interceptive Supportive Therapy (CIST), är en i litteraturen ofta presenterad modell för genomförande av stödbehandling (59, 60, 61, 62) (figur 9). Med hjälp av den kan man i det praktiska arbetet välja olika behandlingsformer beroende på peri-implantatsjukdomens diagnos.
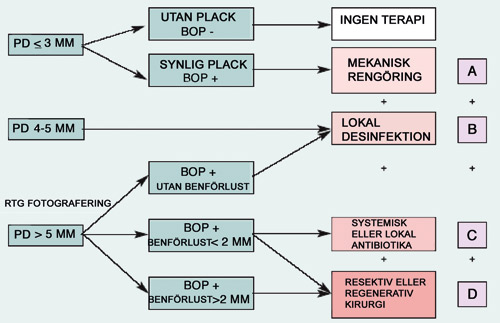
Figur 9. Schema för kumulativ underhållsbehandling av implantat (CIST). I situation (A) strävar man efter att förbättra patientens egenvård. Implantatets yta rengörs mekaniskt, till exempel med icke-metalliska kyretter och gummikoppar + implantatpasta. I situation (B) förenar man mekanisk rengöring med kemisk plackkontroll, som omfattar desinficering av fickorna med klorhexidingel och sköljning av munnen med klorhexidinlösning två gånger dagligen i 3–4 veckor. Efter de föregående åtgärderna inleds i situation (C) behandling med antibiotika på basis av en radiologisk undersökning och bakterieodlingssvar. Om behandlingarna (A), (B) och (C) inte leder till förbättring, övervägs kirurgisk behandling. Se artikeltexten för närmare beskrivning. (Bilden och bildtexten är en bearbetning av konsensusrapporten från år 2004 (61).)
PD = Implantatfickans djup. BOP = Blödning i samband med mätning av peri-implantatfickan
Behandling av peri-implantär mukosit
Om en patient inte har tecken på inflammatorisk sjukdom, om fickorna är < 4 mm djupa och om det finns bara lite plack, räcker det vid stödbehandlingsbesöket med mekanisk rengöring med gummikopp och implantatpasta. Användning av sodarengöring (air powder system) är också ett tryggt och effektivt sätt att bryta ner bakteriebiofilmen på tand- och implantatytor. För borttagning av plack och särskilt tandsten passar plast-, teflon- eller kolfiberkyretter, eftersom dessa inte skadar den känsliga titanytan. Till följd av deras tjocklek är de dock klumpiga. Ultraljudsapparaternas implantatspetsar är också säkra och effektiva (63) (figur 9 A). Användning av sedvanliga stålkyretter eller ultraljudsapparatspetsar rekommenderas inte. Antiseptiska ämnen, till exempel klorhexidin, förbättrar resultatet av den mekaniska instrumenteringen (64) (figur 9 B). När tecken på inflammation föreligger, är det av största vikt att patienten förbättrar sin munhygien. För den dagliga plackkontrollen kan man använda en vanlig tandborste eller en eltandborste. För rengöring av ytor, som är svåra att rengöra, finns specialborstar för de approximala mellanrummen mjuka plastbeklädda mellanrumsborstar. Böjliga tandstickor fungerar väl i trånga mellanrum. Implantattrådar lämpar sig särskilt väl för borttagning av plack från submukotiska implantatytor (65, 66). Daglig användning av munsköljmedel (Listerine®) som tillägg till den mekaniska rengöringen kan vara till nytta för att reducera plack hos en del patienter (67, 68). Om man vid kontrollbesöket konstaterar att fickorna kring ett implantat har blivit grundare och mjukvävnaderna fastare samt att blödningen och pusflöde upphör, är detta tecken på en lyckad behandling av patientens peri-implantatsjukdom (figur 5).
Icke-kirurgisk behandling av peri-implantit
Behandlingen av begynnande peri-implantit följer till en börja med samma principer som behandlingen av peri-implantär mukosit (59, 61). Vid måttligt framskriden (fickdjup 4–6 mm och benförlust < 30 procent av implantatets längd) eller långt framskriden peri-implantit (fickdjup > 6 mm och benförlust > 30 procent) är icke-kirurgisk behandling inte tillräckligt effektiv. Bruk av klorhexidin har inte påverkat de kliniska och mikrobiologiska parametrarna i nämnvärd grad. Då patienten utöver den mekaniska behandlingen har fått upprepad, lokal eller systemisk antibiotikabehandling, har blödningarna minskat och implantatfickorna blivit grundare vid ettårskontrollen (64, 69, 70) (figur 9 C). Alla peri-implantitlesioner har dock inte läkts. För en del patienter med peri-implantit medför mikrobiell odling och riktad, systemisk antimikrobiell läkemedelsbehandling, som baserar sig på odlingssvaret, som tillägg till den mekaniska behandlingen, ett förbättrat slutresultat (54, 71). Laserbehandling av peri-implantit har inte visat sig ge någon tilläggsnytta jämfört med icke-kirurgisk behandling (64).
Kirurgisk behandling av peri-implantit
Vid behandlingen av peri-implantit har den kirurgiska behandlingen (konservativ lambåoperation, regenerativ eller resektiv kirurgi) visat sig vara effektivare än icke-kirurgisk behandling (72) (figur 9 d). Enligt en femårig uppföljningsstudie medförde konservativ kirurgi att 58 procent av implantaten med svår peri-implantit tillfrisknade (73). En förutsättning för framgångsrik kirurgisk behandling är att man – förutom noggrann borttagning av granulationsvävnad – också får den kontaminerade och blottade implantatytan fri från bakterier och celler. Några uppenbara skillnader har inte konstaterats mellan olika metoder för dekontaminering av implantatytan (mekanisk rengöring eller kemiska ämnen såsom klorhexidin, väteperoxid, koksalt, citronsyra och luftabrasion eller laser) (74). Däremot är rökare uppenbara riskpatienter inte bara när det gäller att drabbas av peri-implantit utan också när det gäller att tillfriskna. I studierna har man i allmänhet använt antibiotika systemiskt i samband med de kirurgiska ingreppen för behandling av peri-implantit, men vetenskapligt belägg för effekten av denna behandling finns inte (71). Enligt en tremånaders uppföljningsstudie är konservativ kirurgi utan systemisk antibiotika också effektiv (75).
Många patientfall och patientserier har visat att peri-implantit i vissa fall kan behandlas framgångsrikt med regenerativ kirurgi (membraner, autologa benstransplantat eller ersättande benmaterial med eller utan membran). Resultaten av regenerativ kirurgi har dock varierat och är svåra att förutse. Verklig re-osseointegration kan inte förväntas, men lesionerna kan i någon mån få utfyllnad av regenererande benvävnad beroende på storleken av defekten, dess morfologi och patientens rökvanor. Trots bentillväxt kan inflammationen inte alltid elimineras och vävnadsskadan progredierar med tiden (72, 76).
Inflammationen kan även kontrolleras genom att påverka de anatomiska förhållandena med resektiv kirurgi. I samband med lambåkirurgisk åtgärd reduceras kanterna av bendefekten kring implantatet och lambån lägges antingen på den ursprungliga höjden eller flyttas apikalt. När fickorna blir grundare elimineras de anaerobiska omständigheterna. Ingen entydig nytta har påvisats av en slipning av implantatskruvens spiralvarv (implantoplasty) i samband med morfologisk hårdvävnadsreparation (77, 78).
För att underlätta plackkontrollen kan ett plastikingrepp utföras på den hyperplastiska slemhinna som ofta uppstår kring implantatburna täckproteser, men endast om det finns tillräckligt med fast keratiniserad mukosa. Om vävnaderna är friska (ingen blödning), är en morfologisk reparation av mjukvävnaderna inte alltid nödvändig.
Om ett lambåkirurgiskt ingrepp utförs i ett område där fast keratiniserad mukosa saknas, bör man i samband med ingreppet sträva till att skapa sådan på det aktuella området (34).
Alla kirurgiska åtgärder är alltid förenade med en risk för att slemhinnan drar sig tillbaka, vilket särskilt bör beaktas i den estetiskt krävande överkäksfronten. Patienten måste informeras väl om denna risk innan åtgärden utförs. Hos patienten med en tunn vävnadsbiotyp, kan mjukvävnaden lätt dra sig tillbaka.
Viktiga punkter för att förhindra komplikationer
Patienten spelar en aktiv roll i vårdteamet och deltar i teamets arbete. Patienten har på förhand informerats om hur de implantatprotetiska konstruktionerna som skal installeras skiljer sig från naturliga tänder eller traditionella proteser i fråga om funktion och behov av stödbehandling.
Alla patientrelaterade riskfaktorer som påverkar framgångsrik implantatbehandling har förklarats för patienten. Patienten har fått information om betydelsen av god munhygien för implantatet och för hela tanduppsättningen. Även rökningens skadeverkningar har framhållits, och patienten är beredd att sluta röka om omständigheterna kräver det (till exempel vid användning av bentransplantat). Eventuell parodontit har behandlats och patienten är fri från inflammationer innan implantatbehandlingen påbörjas.
Implantaten har installerats så att de omges av tillräckligt med benmängd. Det måste också finnas tillräckligt med mjukvävnad antingen från början eller genom plastisk rekonstruktion; målet är att implantatet omges av en zon av fast keratiniserad slemhinna. Implantatet är stabilt och uppfyller estetiska och funktionella krav (balanserat bett, inga interferenser, ingen skadlig lateral belastning, tuggytorna är rätt dimensionerade och antalet implantat är tillräckligt).
De protetiska konstruktionerna har utformats så att det är enkelt att rengöra alla ytor dagligen, särskilt approximalmellanrummen. Patienten har instruerats i användningen av individuellt anpassade rengöringsredskap.
Det kliniska och radiologiska läget har registrerats vid det ögonblick då de protetetiska konstruktionerna har satts på plats och implantatet har belastats. För att kunna konstatera förändringar i mjukvävnader- och bennivå bör dokumentationen vid belastningsögonblicket innehålla följande uppgifter:
a) Implantatfickornas djup mätt från en fast referanspunkt.
b) Intraorala röntgenbilder tagna med parallellteknik vid belastning och vid behov ett halvt eller ett år.
c) Eventuella fotografier av slemhinnestatus och mjukvävnadskontur.
Det bør finnas tillräckliga journalanteckningar för alla åtgärder, både kirurgiska och protetiska.
Patienten har informerats om betydelsen av fortgående stödbehandling med tanke på bevarat implantat. Patienten kommer på regelbundna kontrollbesök enligt individanpassat schema, antingen på eget initiativ eller på kallelse av tandvårdspersonalen.
Slutord
För på lång sikt framgångsrika implantatburna konstruktioner är det lika viktigt att upprätthålla en frisk mjukvävnadsbarriär som att garantera osseointegrationen. Preventiv vård inleds redan före fixturoperation med en bedömning av patientens munhygiennivå. Patientens motivation och förmåga till daglig plackkontroll bör beaktas redan vid planeringen av implantatburna konstruktioner och givetvis när implantatet har placerats. Patientens eget ansvar betonas inte bara i fråga om munhygien utan också när det gäller rökvanor och effekten av stödbehandling.
För att mjukvävnaderna skal förbli friska är det viktigt att skapa ett effektivt program för stödbehandlingen. Vid stödbehandlingsbesöken mäts fickorna, registreras eventuell blödning och pusflöde vid sonderingen. Mätresultaten jämförs med tidigare resultat. Förutom klinisk granskning tas röntgenbilder för att kontrollera eventuell förekomst av peri-implantatsjukdom. Långtidsprognosen för implantat är beroende av regelbunden professionell uppföljning och effektiv förebyggande vård.
Det finns ännu inga vetenskapliga data om den optimala frekvensen för stödbehandlingsbesöken, men de normala rutinerna för parodontologisk stödbehandling har ett besöksintervall på 6–12 månader beroende på patientens samlade riskfaktorer och tändernas allmänna situation. Stödbehandlingsintervallet för patienter med dålig behandlingsföljsamhet och för riskpatienter kan vara 3–6 månader. Samma intervall gäller för patienter som under det första året haft komplikationer eller som förlorat ett eller flera implantat.
För behandlingen av komplikationer som uppstår under stödbehandlingstiden är det synnerligen viktigt att diagnosen är rätt. Eftersom behandlingsresultaten för peri-implantit är osäkra, är de primära målen för stödbehandling att förebygga och behandla peri-implantatsjukdomarna på ett tidigt stadium. För att dessa mål ska uppfyllas är en individuellt anpassad, regelbunden stödbehandling nödvändig för alla patienter med implantat.
English summary
Nieminen A, Jokela-Hietamäki M, Uitto V-J.
Supportive implant treatment and peri-implant diseases
116–24.
Properly placed tooth implants can be expected to last functionally for a long time. However, research has shown that nearly 40 percent of implant patients have some sort of biological or mechanical complications already during the first five years. Inflammatory peri-implant diseases, peri-implant mucositis and peri-implantitis, result from the formation of bacterial deposits on implant structures. In peri-implant mucositis inflammation is restricted to soft tissues, while in peri-implantitis also the surrounding bone has been lost. Only recently we have learned that the preservation of implants depends greatly on both the appropriate oral hygiene of the patient and on regular maintenance care. According to recent studies patients that have yearly control appointments have less inflammatory complications than those who have undergone treatment only after the occurrence of complications.
The primary goals of maintenance treatment are prevention of the formation of peri-implant diseases or their treatment at early stages, as well as the correction of technical flaws in the implants. Even though there is no scientific evidence for optimal peri-implant maintenance care, it can be assumed that the same principles that have been obtained from studies on periodontal maintenance care apply to implant maintenance as well. During each maintenance care appointment the depth of peri-implant pockets and bleeding/suppuration on probing are measured and registered. If the pocket depth is increased compared to the earlier appointment, the diagnosis has to be verified by radiographs. Depending on the extension of tissue destruction, peri-implant diseases are treated by mechanical cleaning and local disinfection, and when required, by systemic antibiotic treatment or surgical therapy or both. In order to maintain peri-implant health and to prevent complications, the individual risk factors connected to implant therapy should be considered already when planning the treatment. To guarantee a long-term positive outcome for implant structures, an individual maintenance program should be planned for all implant patients. This should stress the responsibility of the patient to keep up proper oral hygiene, attend maintenance appointments, and to limit smoking.
Referenser
3. Ramfjord SP. Maintenance care for treated periodontitis patients. J Clin Periodontol. 1987; 14: 433–7. Review article.
4. Cohen RE. Academy Report. Position paper – periodontal maintenance. Research, science and therapy committee of the American Academy of Periodontology. J Periodontol. 2003; 74: 1395–401.
8. Berglundh T, Person L, Klinge B. A systematic review of the incidence of biological and technical complications in implant dentistry reported in prospective longitudinal studies of at least 5 years. J Clin Periodontol. 2002; 29(Suppl.3): 197–212.
9. Albrektsson T, Zarb G, Worthington P, Eriksson AR. The long-term efficacy of currently used dental implants: a review and proposed criteria of success. Int J Oral Maxillofac Implants. 1986; 1(1): 11–25.
11. Schwartz-Arad D, Herzberg R, Levin L. Evaluation of long-term implant success. J Periodontol 2005; 76: 1623–8.
13. Quirynen M, Bollen CML. The influence of surface roughness and surface-free energy on supra- and subgingival plaque formation in man. A review of the literature. J Clin Periodontol. 1995; 22(1): 1–14.
14. Esposito M, Murray-Curtis L, Grusovin MG, Coulthard P, Worthington HV. Interventions for replacing missing teeth: different types of dental implants. Cochrane Database Syst Rev. 2007; Issue 4.
15. Pjetursson BE, Tan K, Lang NP, Brägger U, Egger M, Zwahlen M. A systematic review of the survival and complication rates of fixed partial dentures (FPDs) after an observation period of at least 5 years. I. Implant-supported FPDs. Clin Oral Impl Res. 2004; 15: 625–42.
18. Isidor F. Influence of forces on peri-implant bone. Clin Oral Impl Res. 2006; 17(Suppl.2): 8–18.
20. Kozlovsky A, Tal H, Laufer BZ, Leshem R, Rohrer MD, Weinreb M, Artzi Z. Impact of implant overloading on the peri-implant bone in inflamed and non-inflamed peri-implant mucosa. Clin Oral Impl Res. 2007; 18(5): 601–10.
21. Hultin M, Komiyama Ai, Klinge B. Supportive therapy and the longevity of dental implants: a systematic review of the literature. Clin Oral Impl. Res 2007; 18(Suppl.3): 50–62.
25. Zitzmann NU, Berglundh T. Definition and prevalence of peri-implant diseases. J Clin Periodontol. 2008; 35(Suppl. 8): 286–91.
26. Iacono VJ. Academy Report. Position Paper – Dental implants in periodontal therapy. J Periodontol. 2000; 71: 1934–42.
29. Hermann JS, Buser D, Schenk RK, Higginbottom FL, Cochran DL. Biologic width around titanium implants. A physiologically formed and stable dimension over time. Clin Oral Impl Res. 2000; 11(1): 1–11.
33. Esposito M, Grusovin MG, Maghaireh H, Coulthard P, Worthington HV. Interventions for replacing teeth: Management of soft tissues for dental implants. Cochrane Database Syst Rev. 2007 Jul 18(3).
34. Cairo F, Pagliaro U, Nieri M. Soft tissue management at implant sites. J Clin Periodontol. 2008; 35 (Suppl.8): 163–7.
35. Albrektsson T, Isidor F. Consensus report of session IV. In : Lang NP, Karring T. (eds.) Proceedings of the 1st European Workshop on Periodontology. Quintessence Publishing Co., Ltd., London 1994; pp. 365–9.
37. Quirynen M, De Soete M, van Steenberghe D. Infectious risks for oral implants: a review of the literature. Clin Oral Impl Res. 2002; 13: 1–19.
39. Ferreira SD, Silva GLM, Cortelli JR, Costa JE, Costa FO. Prevalence and risk variables for peri-implant disease in Brazilian subjects. J Clin Periodontol. 2006; 33: 929–35.
40. Renvert S, Persson GR. Periodontitis as a potential risk factor for peri-implantitis. J Clin Periodontol. 2009; 36(Suppl.10): 9–14.
41. Heitz-Mayfield LJA. Peri-implant diseases: diagnosis and risk indicators. J Clin Periodontol. 2008; 35(Suppl.8): 292–304.
42. Mombelli A. Microbiology of the dental implant. Adv Dent Res. 1993; 7(2): 202–6.
43. Salvi GE, Lang NP. Diagnostic parameters for monitoring peri-implant conditions. Int J Oral Maxillofac Implants. 2004; 19(Suppl.): 116–27.
44. Humphrey S. Implant maintenance. Dent Clin North Am. 2006; 50: 463–78.
45. Heitz-Mayfield LJA. Diagnosis and management of peri-implant diseases. Aust Dent J. 2008; 53(Suppl.1): 43–8. Review.
53. Luterbacher S, Mayfield L, Brägger U, Lang NP. Diagnostic characteristics of clinical and microbiological tests for monitoring periodontal and peri-implant mucosal tissue conditions during supportive periodontal therapy (SPT). Clin Oral Impl Res. 2000; 11: 521–9.
54. Mombelli A. Microbiology and antimicrobial therapy of peri-implantitis. Periodontol. 2000 2002; 28: 177–89.
55. Esposito M, Worthington HV, Coulthard P, Thomsen P. Maintaining and re-establishing health around osseointegrated oral implants. A Cochrane systematic review comparing the efficacy of various treatments. Periodontol. 2000 2003; 33: 204–12.
56. Lindhe J, Meyle J. Peri-implant diseases: Consensus Report of the 6th European Workshop on Periodontology. J Clin Periodontol. 2008; 35(Suppl.8): 282–5.
57. Roos-Jansåker A-M, Renvert S, Egelberg J. Treatment of peri-implant infections: a literature review. J Clin Periodontol. 2003; 30: 467–85.
58. Esposito M, Grusovin MG, Kakisis I, Coulthard P, Worthington HV. Interventions for replacing teeth: treatment of peri-implantitis. Cochrane Database Syst Rev. 2008 Apr 16(2).
59. Mombelli A, Lang NP. The diagnosis and treatment of peri-implantitis. Periodontol. 2000 1998; 17: 63–76.
61. Lang NP, Berglundh T, Heitz-Mayfield LJ, Pjetursson BE, Salvi GE, Sanz M. Consensus statements and recommended clinical procedures regarding implant survival and complications. Int J Oral Maxillofac Implants. 2004; 19 (Suppl.): 150–4.
62. Berglundh T, Lang NP, Lindhe J. Treatment of peri-implant lesions. In: Lang NP, Lindhe J. (eds.) Clinical Periodontology and Implant Dentistry. Fifth Edition. Blackwell Munksgaard 2008; pp. 875–81.
64. Renvert S, Roos-Jansåker A-M, Claffey N. Non-surgical treatment of peri-implant mucositis and peri-implantitis: a literature review. J Clin Periodontol. 2008; 35(Suppl.8): 305–15.
65. Silverstein LH, Kurtzman GM. Oral hygiene and maintenance of dental implants. Dent Today 2006; 25(3): 70–5.
68. Grusovin MG, Coulthard P, Jourabchian E, Worthington HV, Esposito M. Interventions for replacing missing teeth: maintaining and recovering soft tissue health around dental implants. Cochrane Database of Syst Rev. 2008, Issue 1.
69. Renvert S, Lessem J, Dahlén G, Lindahl C, Svensson M. Topical minocycline microphores versus topical chlorhexidine gel as an adjunct to mechanical debridement of incipient peri-implant infections: a randomized clinical trial. J Clin Periodontol. 2006; 33: 362–9.
70. Renvert S, Lessem J, Dahlén G, Renvert H, Lindahl C. Mechanical and repeated antimicrobial therapy using a local drug delivery system in the treatment of peri-implantitis: a randomized clinical trial. J Periodontol. 2008; 79: 836–44.
71. Heitz-Mayfield LJA, Lang NP. Antimicrobial treatment of peri-implant diseases. Int J Oral Maxillofac Implants. 2004; 19(Suppl.): 128–39.
72. Claffey N, Clarke E, Polyzois I, Renvert S. Surgical treatment of peri-implantitis. J Clin Periodontol. 2008; 35(Suppl.8): 316–32
73. Leonhardt Å, Dahlén G, Renvert S. Five-year clinical, microbiological, and radiological outcome following treatment of peri-implantitis in man. J Periodontol. 2003; 74: 1415–22.
76. Roos-Jansåker A-M, Renvert H, Lindahl C, Renvert S. Surgical treatment of peri-implantitis using a bone substitute with or without a resorbable membrane: a prospective cohort study. J Clin Periodontol. 2007; 34: 625–32.
Fullständig referenslista kan rekvireras från Anja Nieminen (anja.nieminen@helsinki.fi)
Adress: Anja Nieminen, dr odont, specialtandläkare i klinisk tandvård (parodontologi), seniorforskare. Institutionen för odontologi, Helsingfors universitet. E-post: anja.nieminen@helsinki.fi