Non-operativ vs operativ behandling av karies blant barn og unge
Målsetningen med artikkelen er å presentere og diskutere dagens forskningsbaserte kunnskap om metoder for å behandle karies på barn og ungdom, spesielt om det er grunnlag for å legge større vekt på non-operativ terapi og derved redusere behovet for fyllingsterapi (operativ terapi). Til tross for en viss vitenskapelig usikkerhet hevder internasjonalt ledende forskere at det er forskningsbasert grunnlag for non-operativ kariesterapi, hvilket innebærer å reversere, stanse eller forsinke progresjonen av initiale kariesangrep ved hjelp av profylaktiske og non-operative metoder. Dette forutsetter at man anvender diagnostiske rutiner som oppdager tidlige stadier i kariesutviklingen og bedømmer risikoen for at de videreutvikler seg.
Tannhelsetjenesten for barn og ungdom bør derfor legge til rette for at prinsippene for non-operativ kariesterapi innføres. Det forutsetter sannsynligvis en del strukturelle forandringer i forhold til innkallingsrutiner, bemanning og insentiver for de ansatte i tjenesten. Non-operativ terapi krever mange behandlingssekvenser og korte innkallingsintervaller for pasienter med kariesaktivitet, og en forutsetning for kostnadseffektivitet vil være at man har tilstrekkelig tilgang på rimeligere personell som tannpleiere og tannhelsesekretærer med spesiell opplæring. Økonomiske og andre insentiver, både for de ansatte og for tannhelsetjenesten, må dessuten tilpasses strategien. Bonusordninger som favoriserer operativ terapi vil således være et hinder.
Karies er en multifaktoriell sykdom (1). Patogenesen er godt kjent og akseptert i den forstand at det dreier seg om normalfloraens bakterier i biofilm på tannoverflaten som produserer svake organiske syrer som resultat av metabolisering av karbohydrater. Hvilke bakterier som produserer de organiske syrene som er avgjørende for initiering og utvikling av karies, er i dag omdiskutert. Tradisjonelt har tidigere litteratur fokusert på mutans streptococcer og laktobaciller, men nyere forskning med molekylærbiologiske metoder har vist et mangfold av bakterier som kan spille en rolle (2, 3). Men kunnskapen om at det foreligger en rekke risikofaktorer utover dette, gjør at man ikke lenger bare kan betrakte denne sykdommen som betinget av de tre velkjente sirklene i Keyes’ triade; tann, substrat og mikroorganismer, eventuelt med tillegg av tid som den fjerde sirkel. En rekke personlige faktorer som påvirker det intraorale miljøet spiller en så stor rolle for forståelsen av sykdommen at modellen med de 3–4 sirklene er blitt utvidet til å inkludere andre risikofaktorer og derved karakterisere karies som en multifaktoriell sykdom. Figur 1 er et eksempel på en slik modell basert på publikasjoner av Fejerskov (4) og Selwitz og medarbeidere (1). Det er dessuten en økende erkjennelse av at også arv spiller en betydelig rolle for kariesforekomsten (5).
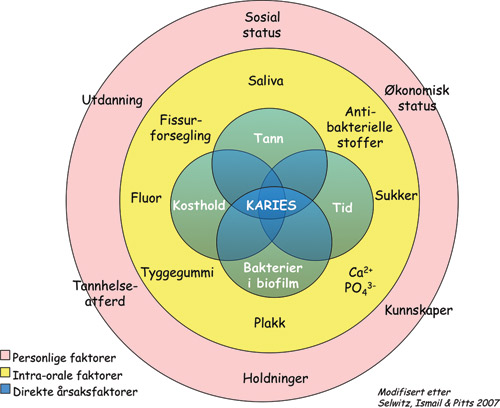
Fig. 1: Faktorer som er involvert i utviklingen av karies.
Karies betraktes som en kronisk sykdom der symptomene varierer fra subklinisk, subsurface demineralisering til infeksjon og destruksjon av dentin, med og uten kavitetsdannelse (6). Hos de fleste mennesker veksler prosessen mellom demineralisering og remineralisering i perioder hver eneste dag. Hvorvidt sykdommen progredierer, stopper eller reverserer er avhengig av balansen mellom de- og remineralisering. Det er når plakket (biofilmen) får anledning til å modnes over lang tid, at kariesprosessen progredierer. Initiale stadier av sykdommen er derfor reversible dersom sukkerinntaket reduseres, biofilmen fjernes og overflaten holdes ren.
Diagnostikk
Nigel Pitts (7) har illustrert kariesforekomsten som et isfjell basert på hvilket diagnostisk nivå man anvender, her illustrert som en pyramide (figur 2). Forekomsten av alvorlige karieslesjoner, som lesjoner til pulpa og kaviteter inn i dentin, er alltid forbundet med forekomst av mange mindre alvorlige lesjoner. Dersom vi bare behandler de alvorlige symptomene på toppen av isfjellet med operativ terapi, som fyllings- og endodontisk terapi, behandler vi ikke sykdommen kausalt.
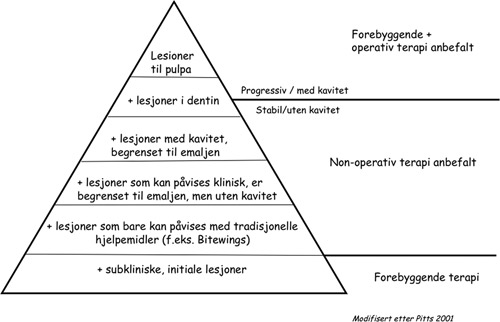
Fig. 2: Foreslåtte terapiformer basert på karies diagnostisk nivå (Pitts 2001 (7))
Når man skal behandle sykdommen er det nødvendig å fastsette et diagnostisk nivå, et «cut-off» for hvor i symptomutviklingen man setter grensen for å registrere at en tann, en flate eller et individ har behandlingskrevende karies (8–10). Dette kan være problematisk i de tidlige stadier av sykdommen, som i internasjonal litteratur benevnes «initial», «incipient» og «non-cavitated lesions», der denne grensen er svært avhengig av hvilken diagnostisk metode man benytter (11). Sensitiviteten og spesifisiteten av de vanlige diagnostiske teknikkene som visuell, taktil og røntgenologisk undersøkelse er svært varierende på forskjellige tenner og flater, og spesielt vanskelig på approksimale flater og i fissurer. Selv om noen av de nyere teknikkene som fiberoptisk transilluminasjon (FOTI og DiFOTI), laser fluorosens (DIAGNOdent™, KaVo Dental GmbH, Biberach/Riß), kvantitativ lysindusert fluorosens (QLF™, Inspektor Research Systems BV, Nederland) og elektrisk konduktans kan ha sin berettigelse på visse tenner og flater, representerer de ikke noe gjennombrudd med tanke på entydig diagnostikk av tidlige stadier av karies. Flere metoder innebærer fare for overregistrering, men dette har ingen negative konsekvenser for flatene dersom det er snakk om non-operativ terapi (12).
Det er imidlertid enighet om viktigheten av å skille mellom det å påvise en karieslesjon (caries detection) og å bedømme den (caries assessment) (9, 13). I det første begrepet (caries detection) ligger det at man på en objektiv måte påviser at det foreligger en karieslesjon, mens det i det andre (caries assessment) ligger en karakterisering av kariesangrepets alvorlighetsgrad og aktivitet. Med alvorlighetsgrad menes hvor langt inn i tannen man kan se symptomer på sykdommen og hvorvidt det foreligger en kavitet eller ikke, mens det med aktivitet menes med hvilken hastighet den progredierer eller går tilbake. Aktiviteten kan være vanskelig å avgjøre, men bedømmes gjerne på basis av lesjonens overflatestruktur (porøs eller glatt, matt eller blank) samt progresjon over tid.
For at en individuell kariesdiagnose skal være fullstendig må den inneholde en risikoanalyse med tanke på hvorvidt den(de) aktuelle lesjonen(e) vil utvikle seg videre, samt om pasienten skal utvikle nye lesjoner. Dette baserer man på det kliniske bildet i munnhulen i kombinasjon med de andre risikofaktorene som er illustrert i figur 1.
Fyllingsterapi (operativ terapi)
Mye av økonomien i klinisk odontologi, både offentlig og privat, er knyttet til reparasjon av alvorlige kariesskader, og således i behandling av symptomer og ikke i kausal behandling av sykdommen. Men det er mange ulemper med fyllingsterapien:
– Det er en «kirurgisk» metode som skjærer/kutter bort både sykt og friskt tannvev.
– Fyllinger har begrenset levetid og resulterer i ytterligere behov for behandling, og ofte mer komplisert behandling (14).
– Pasientene oppfatter ofte behandlingen som ubehagelig og smertefull, og blant barn er den hyppigste enkeltfaktor til utvikling av angst, fobi og unngåelse av tannbehandling (15).
I barnetannpleien er det spesielt problematisk at kvaliteten på fyllingsterapien er relativt dårlig pga. de tekniske vanskelighetene man ofte har på små melketenner og små barn med dårlig mestringsevne. I en svensk studie (16) fant man at 33 % av fyllingene som var lagt i primære tenner før barnet var 5 år var mislykket ved at de enten var lagt om igjen eller at tennene var ekstrahert før barna var blitt 8 år. I en annen svensk studie (17) ble det funnet at 31 % av alle fyllinger som ble lagt på barn mellom 7 og 12 år var omgjøringer, og de fleste av disse omgjøringene (81 %) ble foretatt da barna var mellom 7 og 9 år.
Det er nå en økende trend i den vitenskapelige litteraturen om at man bør bevege seg bort fra denne tradisjonelle «kirurgiske» behandlingsmetoden som innebærer å kutte vekk tannvev og erstatte det med et fyllingsmateriale, og i stedet satse på å kontrollere progresjonen når det oppstår karieslesjoner (18, 19).
Non-operativ terapi
Begrepet anvendes for metoder som søker å reversere, stanse eller redusere progresjonen av en karieslesjon som er under utvikling (20). I praksis handler dette først og fremst om metoder som tar sikte på remineralisering av emalje i lesjoner uten kavitetsdannelse, dvs. aktiv, initial karies (figur 3) (21–23). Det er også mulig å remineralisere lesjoner med kavitet, men det forutsetter at lesjonen ligger slik til at pasienten kan holde den ren for plakk, hvilket kan være tilfelle på bukkal- og lingualflater, men svært vanskelig eller umulig på approksimalflater. I fissurer og pits er det mulig å stanse progresjonen med fissurforsegling (24).
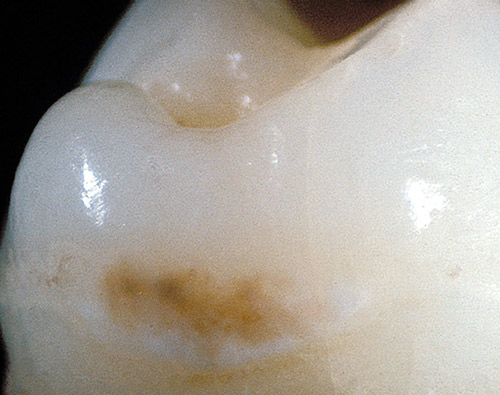
Fig. 3: Initialt kariesangrep uten kavitetsdannelse som er stanset ved remineralisering. Mineraler fra saliva har trengt inn i lesjonen gjennom mikroporøsiteter i overflaten etter at den har vært holdt ren for plakk. Fargestoffer fra munnhulen har også samlet seg i porøsitetene, og derfor er deler av lesjonen misfarget. Overflaten er nå blank og hard.
Prinsippene for non-operativ terapi bygger på vår kunnskap om årsaks- og risikofaktorer for karies og som er illustrert i Fig. 1. De er i stor grad de samme som anvendes i profylaksen, og ofte brukes begrepene profylakse og non-operative terapi om hverandre, noe som kan være forvirrende. Det som prinsipielt skiller profylakse og terapi som tiltak er at terapien baserer seg på at det foreligger en klinisk diagnose, mens profylakse er basert på at man enten ikke har undersøkt pasienten(e) eller at det ikke er funnet tegn til karies på den aktuelle pasient/tann/flate.
Non-operativ kariesterapi forutsetter altså at man har undersøkt en pasient, påvist en eller flere karieslesjoner og bedømt dem til å være behandlingskrevende og indisert for denne type behandling. Behandlingen består av to typer intervensjon basert på den individuelle vurderingen av pasienten og karieslesjonen(e) (20):
1. Generell intervensjon: Dette er tiltak som tar sikte på å påvirke risikofaktorer som pasienten selv kan gjøre noe med, og som i hovedsak befinner seg i den ytre sirkelen i Fig. 1. Man tar sikte på å forbedre pasientens kunnskaper, holdninger og tannhelseatferd.
2. Lokal intervensjon: Dette er behandling som man foretar intraoralt med sikte på å forbedre de intraorale miljøfaktorene og redusere de direkte årsaksfaktorene (figur 1).
1. Metoder for generell intervensjon
Ettersom det forefinnes svært få studier der effekten av hjemmebasert tannhelseatferd på initiale kariesangrep er studert (8, 25), må man støtte seg til litteratur om effekten av generelle kariesforebyggende tiltak.
Daglig tannrengjøring med fluortannkrem er det tiltaket som har størst dokumentert effekt på kariesreduksjon blant barn og ungdom, og dette anses i dag som basistiltak både for populasjonen som helhet og for kariesaktive individer (26, 27). Dersom man skal oppnå remineralisering av et initialt kariesangrep må lesjonen holdes fri for plakk daglig og eksponeres for fluor (21–23) og dette må gjøres av pasienten selv eller pårørende. Pasient og pårørende må derfor få informasjon om lokalisasjoner med initiale, aktive kariesangrep, og om hvordan disse kan holdes fri for plakk og eksponeres for fluor.
Hjemmebasert bruk av fluor i tillegg til F-tannkrem, så som daglig skylling og bruk av sugetabletter, anses å ha begrenset tilleggseffekt (26, 28). Men ettersom det mangler gode studier om effekten på spesielt kariesaktive pasienter og initiale karieslesjoner, bør man ikke være tilbakeholdne med å anbefale slike tiltak i tillegg til plakkfjerning av lesjonen(e) og bruk av F-tannkrem.
Approksimalkaries forekommer hyppig blant barn og ungdom, både i primære og permanente tannsett (29–31), og når det forekommer initiale karieslesjoner her er det naturlig å instruere pasientene i bruk av tanntråd. I de få studiene som er gjort når det gjelder effekten av dette, er konklusjonene motstridende (26). En av forklaringene kan være at effekten er avhengig av om de aktuelle lesjonene har klinisk kavitet eller ikke, og derved mulighetene for at tanntråden effektivt fjerner plakket. Dette kan ikke avgjøres på basis av røntgenbildene (25). Men dersom man satser på non-operativ terapi for behandling av initial approksimalkaries, anbefales det likevel å instruere og motivere denne type pasienter for daglig bruk av tanntråd som del av de generelle tiltakene.
Skylling eller børsting med klorhexidin gel eller løsning, enten alene eller i kombinasjon med fluor, har vært anbefalt i en overgangsfase (f eks 2 ganger daglig i 3 uker) for pasienter med svært dårlig munnhygiene (22). Dette vil redusere forekomsten av mutansstreptokokker i munnhulen, men effekten på karies er ikke dokumentert (26, 32).
2. Metoder for lokal intervensjon
Prinsipielt kan man skille mellom behandlinger som tar sikte på å remineralisere lesjonen eller å stanse videre progresjon ved å forsegle den (fissurforsegling). Førstnevnte er mest aktuelt på glattflatene mens det siste bare kan anbefales i fissurer og pits.
Remineralisering. Viktigste forutsetning for remineralisering av en aktiv karieslesjon er at plakket fjernes og at lesjonen daglig holdes ren slik at mineraler fra saliva kommer til den demineraliserte flaten. Profesjonell plakkfjerning blir derfor første ledd i den lokale behandlingen. Deretter må man vurdere applikasjon av eventuelle «medikamenter» som kan bidra til remineraliseringen, og det første man da tenker på er fluor. Som generell regel anbefales applikasjon av fluorlakk minst 2 ganger årlig (20, 33). Effekten av dette på approksimale flater er dokumentert i en svensk studie blant tenåringer der applikasjon av Duraphat™ hver 3. mnd i 3 år førte til signifikant reduksjon i progresjonen av initiale lesjoner (34).
For å øke tilgjengeligheten av kalsium- og fosfationer på overflaten av demineraliserte karieslesjoner, er det utviklet produkter som skal fremme remineraliseringen. Produktene er basert på en teknologi der man stabiliserer høye konsentrasjoner av frie kalsium- og fosfationer på tannoverflaten, uten at disse utfelles som krystallinske kalsiumfosfater («tannstein») før de får anledning til å trenge inn i den demineraliserte emaljen. Mest kjent og utprøvd er CPP-ACP, som står for Casein PhosphoPeptide-Amorphous Calcium Phosphate, med produktnavnene Recaldent™ og Tooth Mousse™. Disse produktene er lansert både for hjemmebruk av pasienten selv (bl. a. tannkrem, skyllemiddel, tyggegummi) og for applikasjon direkte på demineraliserte tannoverflater profesjonelt. I to nylig publiserte oversiktsartikler (35, 36) har man vurdert det vitenskapelige grunnlaget for disse produktene. Det konkluderes med at CPP-ACP produktene bidrar til å remineralisere subsurface lesjoner og hemme kariesprogresjonen in vivo basert på randomiserte, kontrollerte kliniske studier. Men en helt fersk, nordisk studie om behandling av initiale kariesangrep etter debonding på kjeveortopediske pasienter, viste at tilførsel av Tooth Mousse™ ikke ga noen tilleggseffekt i forhold F-tannpasta 2 ganger daglig (37). Selv om det åpenbart er behov for mer forskning om denne type produkter, representerer de eksempler på «medikamenter» som muligens vil inngå i vårt fremtidige repertoar for bruk i non-invasiv kariesterapi.
En annen tilnærming er å applisere medikamenter med antiseptisk effekt på initiale lesjoner med formål å endre det mikrobiologiske miljøet i biofilmen i gunstigere retning. Applikasjon av klorhexidin er det mest aktuelle, og det er spesielt lakken Cervitec™, med 1 % klorhexidine og 1 % thymol, som har vært brukt i kliniske studier. I disse studiene har lakken vært applisert med varierende hyppighet både på friske flater og på initiale karieslesjoner, og effekten har vært evaluert enten ved antall nye lesjoner eller i hvilken grad initiale lesjoner progredierer. Resultatene er svært varierende, men hovedkonklusjonen er at klorhexidinlakken er effektiv når det gjelder å redusere antall mutansstreptokokker i biofilmen, mens den karieshemmende effekten er mer usikker, i alle fall på barn og ungdom som regelmessig blir eksponert for fluor (38, 39). Når den anvendes på initiale lesjoner kan man neppe regne med karieshemmende effekt dersom den appliseres sjeldnere enn hver 3.-4. måned (39).
Ozon (O3) i væske- eller gassform er også aktuell for å redusere eller eliminere mikrobene i biofilmen. Mest kjent og utprøvd er HealOzone™ som er basert på at ozongass pumpes inn i karieslesjonen og dreper mikrobene, og deretter appliserer man en løsning bestående av mineraler og fluor for å fremme remineralisering. Denne behandlingen er foreslått både for initiale lesjoner og åpne kaviteter på tannflater der man kommer til med tilførsel av gassen. Behandlingen har dokumentert god bakteriehemmende effekt, men det foreligger svært få kontrollerte kliniske studier av den karieshemmende effekten. I flere oversiktsartikler basert på litteraturgjennomgang konkluderes det med at effekten er usikker (40–42).
Fissurforsegling. Intensjonen med fissurforsegling er å blokkere inngangsporten til fissuren og derved hindre at bakterier og næringsstoffer som er nødvendig for kariesprosessen trenger inn (figur 4). Dette gjøres enten med et resin (plastmateriale) eller glassionomersement (20). Retensjonen av resin til emaljen er basert på syreetsningsprinsippet, og dette krever optimal rengjøring og tørrlegging før applikasjonen. Da kan denne type fissurforsegling vare i mange år. Retensjonen av glassionomersement er basert på kjemiske bindinger mellom sement og emalje. Den er ikke på langt nær så sterk som for resin, og slike fissurforseglinger løsner og mistes vanligvis etter få måneder. Men ettersom glassionomersement er en vannbasert sement og ikke så følsom for fuktighet som resin, anvendes den på tenner som ikke lar seg tørrlegge slik en resinbasert forsegling krever. I praksis blir glassionomersement derfor anvendt som en midlertidig fissurforsegling på tenner som er i frembruddsfasen og derfor vanskelig å tørrlegge (20).
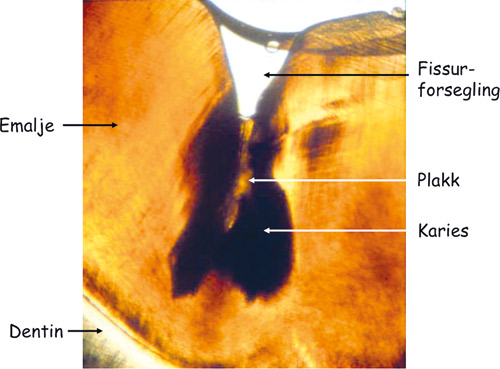
Fig. 4: Slipesnitt av tann med fissurforsegling over en karieslesjon begrenset til emaljen.
Et viktig spørsmål i forbindelse med non-operativ terapi er hvorvidt en fissurforsegling som appliseres på en fissur med aktiv karies er i stand til å stanse videre progresjon av kariesprosessen (fig 4). Dersom fissurforseglingen er tett og hindrer mikrolekkasje av næringsstoffer fra munnhulen inn til mikrobene i det gjenværende plakket i karieslesjonen, kan man tenke seg at disse ikke makter å opprettholde kariesprosessen og dør hen.
I en Cochrane review publisert i 2008 (24) basert på kontrollerte, kliniske studier, konkluderte man med at fissurforsegling med resin må anbefales på permanente molarer hos pasienter med høy kariesrisiko. Effekten var målt ved hvorvidt forseglingen forebygger utvikling av dentinkaries, og tenner med emaljelesjoner ble regnet som friske. Dette innebærer at disse studiene i virkeligheten har evaluert både den forebyggende effekten og effekten på progresjon av emaljekaries. I en oversiktsartikkel publisert i 2008 (43) har man tatt for seg studier om forsegling av kariøse fissurer, med særlig fokus på hvorvidt forseglingen fører til reduksjon av bakterier og stanset kariesprogresjon under forseglingen. Hovedkonklusjonen er at tannleger ikke behøver være tilbakeholdne med å forsegle emaljelesjoner uten kavitet, og det er dette som i dag anbefales ved de nordiske lærestedene (20).
Når det gjelder effekten av glassionomersement som effektiv fissurforsegling til å arrestere initial karies, er dokumentasjonen mangelfull. Men det er indirekte indikasjoner på at materialet er effektivt som midlertidig fissurforseglingsmateriale på frembrytende og nyfrembrutte molarer med tegn på akutt fissurkaries ved at den både hindrer mikrolekkasje og tilfører den demineraliserte emaljen fluor (44, 45).
Det er grunnlag for å konkludere med at fissurforsegling bør anvendes som terapi på initiale kariesangrep snarere enn som profylakse på friske fissurer, ikke minst for at kostnadseffektiviteten skal være akseptabel. Dette var også konklusjonen under et symposium i ORCA i 2007 (46) der det ble anbefalt å bruke fissurforsegling terapeutisk på lesjoner både i emalje og ytre del av dentin. Utgangspunktet er dagens relativt lave kariesforekomst.
Operativ vs non-operativ terapi
Valget mellom operativ og non-operativ terapi i det enkelte kasus må være basert på diagnose som inkluderer karieslesjonens alvorlighetsgrad, kariesaktiviteten og hvilke andre risikofaktorer som foreligger (Fig. 1). Det bærende prinsippet bør være at alle aktive lesjoner behandles med non-operativ terapi med mindre man vurderer progresjonen å være kommet til «the point of no return«/ «restoration threshold», dvs. at den ikke kan stanses uten fyllingsterapi. Når en aktiv lesjon har utviklet en kavitet, og denne ikke er tilgjengelig for at pasienten selv kan holde den ren, vil det være den normale indikasjon for fyllingsterapi (18, 20, 23). Vanskene med å avgjøre hvorvidt initiale lesjoner på approksimalflatene har kavitet eller ikke, gjør at man som hovedprinsipp velger non-operativ terapi, med mindre man på røntgenbilder har registrert at lesjonen progredierer i dentin over tid. I fissurer og pits, der diagnostikken også er vanskelig, vil en fissurforsegling med resin kunne arrestere alle initiale lesjoner (i emalje og ytre del av dentin) under forutsetning av at forseglingen har en kvalitet som effektivt hindrer mikrolekkasje.
Ved vurdering av et mulig «point of no return» i melketannsettet, bør man ta hensyn til at kariesprogresjonen gjennom emaljen er relativt hurtigere enn på permanente tenner, fordi emaljelaget er tynnere (20).
Har non-operativ kariesterapi dokumentert klinisk effekt?
Basert på best mulig forskningsbasert kunnskap om karies hevder mange internasjonalt ledende forskere på dette området at det er grunnlag for å skifte strategi fra operativ til non-operativ behandling, og dette har kommet frem i en rekke internasjonale symposier og oversiktsartikler (1, 9, 18, 23, 46–49). Men for å anbefale dette gjennomført i en organisert barne- og ungdomstannpleie i de nordiske land, kreves evidensbasert kunnskap på høyt nivå, hvilket i praksis betyr kontrollerte kliniske studier. I rapporter fra flere organisasjoner som gjennomfører litteraturbaserte metodevurderinger, såkalte Health Technology Assessments (HTA), og som har vurdert behandling av karies, er det et gjennomgående utsagn at bevisene er for svake eller motstridende til å trekke sikre konklusjoner (25, 26, 50, 51). Grunnlaget for disse konklusjonene er dessverre at det forekommer svært få randomiserte, kontrollerte kliniske studier som evaluerer effekten av non-operativ terapi på initiale karieslesjoner.
Så vidt vites er det bare to kliniske studier i regi av offentlig tannhelsetjeneste i de nordiske land som har evaluert effekten av en behandlingsstrategi basert på non-operativ terapi sammenlignet med operativ terapi (52, 53). Allerede i 1987 startet man et tannhelseprogram for 6-åringene i Nexø kommune på Bornholm basert på non-operativ kariesbehandling (52). Innholdet i programmet var prinsipielt slik som beskrevet i denne artikkelen, nemlig en generell intervensjon (opplæring og motivasjon av barn og foresatte i hjemmebaserte tiltak med særlig fokus på plakkontroll) og lokal intervensjon (profesjonell plakkfjerning, fluorapplikasjon og fissurforsegling på flater med aktiv karies). Dette ble gjort av tannleger og tannhelsesekretærer. Innkallingsintervallene ble individualisert på grunnlag av risikofaktorer, så som responsen på den generelle intervensjonen, kariesprogresjonen og frembruddstatus av de permanente molarer (begynnende fissurkaries). Resultatene ble evaluert da de første to årskullene fylte 18 år i 1999 og 2000 og sammenlignet med 4 andre danske kommuner som var blant de med lavest kariesforekomst i Danmark (52). 18-åringene i Nexø hadde da gjennomsnittlig mindre enn halvparten DMFS (D=dentinlesjoner indisert for fyllingsterapi) (DMFS=1,23) enn i de andre kommunene (DMFS=2,73–3,93). Mer enn halvparten av dem hadde DMFS=0, og ingen tenner var ekstrahert eller rotfylt pga. karies. Antall timeavtaler i perioden fra 5–18 år varierte mellom 24 og 65, men dette var ikke forskjellig fra før man innførte det nye programmet. Kostnadene pr. barn hadde sunket betydelig fra perioden før de innførte programmet. Den viktigste svakheten ved denne studien er at den ikke var basert på et ekte randomisert, kontrollert design, men simulerte dette ved å sammenligne det eksperimentelle programmet i Nexø med 4 andre kommuner med tradisjonelle programmer av god kvalitet.
I byen Pori i Finland ble det i perioden 2001–2005 gjennomført en randomisert, kontrollert studie av et program basert på individuelt tilpasset profylakse og non-operativ terapi for barn i alderen 11–12 år som ved studiens begynnelse hadde minst en initial, aktiv karieslesjon (53). En eksperimentell gruppe fikk et individuelt tilpasset profylakse- og behandlingsopplegg med målsetning å identifisere og eliminere faktorer som førte til kariesaktivitet. Kontrollgruppen fikk ordinær behandling og fulgte det generelle profylakseregimet som tannhelsetjenesten tilbød. Det var tannpleiere med særskilt opplæring av eksperter i pasient- og helsefokusert rådgiving som utførte oppgavene i det eksperimentelle programmet, både den generelle og lokale intervensjonen.
Den generelle intervensjonen var basert på en interaktiv diskusjon mellom tannpleier og pasient, der målsetningen var at de sammen evaluerte årsaken til at de initiale, aktive lesjonene hadde oppstått. Videre fikk de utdelt tannbørster, tannkrem (1500 ppm F og 10 % xylitol) og F-tabletter med instruksjon om hvordan disse skulle brukes. Den lokale intervensjon besto av at de initiale, aktive karieslesjonene og nyfrembrutte fissurer ble rengjort profesjonelt og penslet med Cervitec™ og Duraphat™ to ganger i løpet av 1–2 uker, og dette fortsatte til man mente at kariesprogresjonen var reversert. Når barna hadde behov for operativ terapi ble de henvist til tannlege. Kontrollgruppen fikk samme behandling som var vanlig i tannhelsetjenesten i Pori og som tannleger hadde ansvar for. I perioden når undersøkelsen pågikk ble det gjennomført kampanjer for god tannhelse i skoler, på supermarkeder, i massemedia etc., med tanke på at ikke bare eksperimentgruppen, men hele befolkningen i Pori, skulle være målgruppe for informasjon og motivasjon om god tannhelseatferd. Tilveksten av DMFS (D= lesjoner med kavitet) etter 3,4 år var 2,56 i eksperiment- og 4,60 i kontrollgruppen, hvilket betydde at det non-invasive programmet hadde forebygget 44 % fyllingskrevende karies blant 14–15 åringene som hadde aktiv karies da de var 11–12 år. Men dette hadde kostet betydelig med ressurser, bl.a. i gjennomsnitt 11,4 applikasjoner av fluor- og klorhexidinlakk over 3-års perioden, noe som var syv ganger mer enn i kontrollgruppen. Antall timeavtaler var tre ganger høyere.
I en senere publikasjon om undersøkelsen i Pori evaluerte man kostnadene ved de to behandlingsprogrammene (54). Gjennomsnittlig kostnad pr. barn for hele perioden var ı496,45 i eksperimentgruppen og ı426,95 i kontrollgruppen, og man beregnet kostnadene for hver sparte DMFS til ı34,07. Kostnadene pr. barn i eksperimentgruppen sank utover i perioden mens den var konstant i kontrollgruppen. Siste året var faktisk barna i kontrollgruppen dyrere. Dette tilskriver forfatterne at programmet etter hvert ble mer etablert med behov for færre intervensjoner av tannpleierne. I perioden (2005–2008) etter at den eksperimentelle studien var avsluttet, der ungdommene i begge gruppene fikk standard tilbud om tannpleie, var både kariesforekomsten og kostnadene lavere for de som hadde vært i eksperimentgruppen (55).
Konklusjoner
– Kunnskapene om karies som multifaktoriell sykdom utgjør tilstrekkelig teoretisk grunnlag for å etablere profylakse og non-operativ terapi som basistiltak i tannhelsetjenesten for barn og ungdom.
• En forutsetning for å prioritere non-operativ terapi fremfor fyllingsterapi er at man anvender diagnostiske prinsipper som fanger opp initial karies og bedømmer risikoen for videre progresjon og nye lesjoner.
• Non-operativ terapi inkluderer generell og lokal intervensjon. Elementene i disse intervensjonene bygger på forskningsbasert kunnskap og er stort sett sammenfallende med det som gjerne omtales som profylaksetiltak. Tannbørsting med fluortannkrem, lokal applikasjon av fluorlakk og fissurforsegling er de tiltakene som har best dokumentert effekt.
• Det er få kliniske studier av non-operativ terapi, men to nordiske studier på barn og ungdom indikerer positiv effekt med tanke på å redusere behovet for fyllingskrevende behandling. Kostnadene ved overgang til slike opplegg i tannhelsetjenesten kan være større enn tradisjonell behandling til å begynne med, men vil trolig bli mindre etter hvert.
• Non-operativ terapi kan gjennomføres av tannpleiere og annet hjelpepersonell, og en sannsynlig forutsetning for en kostnadseffektiv overgang til slik terapi er økt tilgang på slikt personell.
• Selv om det er behov for mer forskning om effektiviteten av non-operativ terapi, er det grunnlag for å hevde at det nå må legges bedre til rette for denne behandlingsformen i tannhelsetjenesten for barn og ungdom.
English summary
Non-operative vs. operative treatment of caries in children and adolescents. Time for change of strategy?
The aims of this paper were to describe present knowledge about non-operative caries treatment and to discuss whether it is time for a change in strategy with more focus on non-operative treatment in dental services for children and adolescents. Operative (restorative) treatment is connected with a variety of drawbacks, and it is symptomatic rather than causal by nature. According to the international literature it is possible to reverse or arrest initial caries lesions by use of non-operative treatment techniques, either re-mineralisation or fissure sealing, and thereby reduce the need for restorations. Such a strategy must be based on the use of diagnostic techniques able to detect the early lesions and assess their risks of progression. Since only a few clinical studies comparing non-operative vs. operative caries treatment strategies in organised dental health services have been accomplished, a number of Health Technology Assessments and literature reviews have concluded that there is a lack of evidence that non-operative treatment is effective. However, this strategy is now advocated by an increasing number of recognised researchers in this field, maintaining that there is sufficient evidence for clinical implementation. While waiting for more clear-cut evidence from randomised and controlled clinical studies, it is suggested that the organised dental public service for children and adolescents should prepare for a future with increased emphasis on early diagnosis and non-operative treatment. Since this strategy requires frequent dental visits and short recall intervals for caries-active individuals, increased use of dental hygienists and other auxiliary personnel would probably be necessary for cost effectiveness.
Hovedbudskap | |
|---|---|
• |
Mens man ved operativ kariesterapi (fyllingsterapi) behandler symptomer i avanserte stadier i kariesprosessen, tar non-operativ terapi sikte på å reversere, stanse eller hemme prosessen i tidlige stadier. I klinikken kompletterer disse metodene hverandre. |
• |
Internasjonale forskningsmiljøer mener at det er grunnlag for å innføre program basert på non-operativ terapi, men foreløpig er det få kontrollerte, kliniske studier. |
• |
To nordiske studier, der effekten ble målt ved antall sparte fyllinger i unge permanente tenner, tyder på høy effektivitet av slike program.. |
• |
En forutsetning for at slike program skal være kostnadseffektive er økt bruk av tannpleiere og annet hjelpepersonell, samt insentiver for anvendelse av slik terapi. |
Referanser
1. Selwitz RH, Ismail AI, Pitts NB. Dental caries. Lancet. 2007 Jan 6; 369(9555): 51–9.
2. Aas JA, Griffen AL, Dardis SR, Lee AM, Olsen I, Dewhirst FE, et al. Bacteria of dental caries in primary and permanent teeth in children and young adults. J Clin Microbiol. 2008; 46(4): 1407–17.
3. Beighton D. The complex oral microflora of high-risk individuals and groups and its role in the caries process. Community Dent Oral Epidemiol. 2005; 33(4): 248–55.
4. Fejerskov O. Changing paradigms in concepts on dental caries: consequences for oral health care. Caries Res. 2004; 38(3): 182–91.
5. Slayton RL, Slavkin HC. Scientific investments continue to fuel improvements in oral health (May 2000-present). Acad Pediatr. 2009; 9(6): 383–5.
6. Fejerskov O, Kidd EAM. Dental caries. The disease and its clinical management. Copenhagen: Blackwell Munksgaard; 2003.
7. Pitts NB. Clinical diagnosis of dental caries: a European perspective. J Dent Educ. 2001; 65(10): 972–8.
8. Bader JD, Shugars DA, Bonito AJ. Systematic reviews of selected dental caries diagnostic and management methods. J Dent Educ. 2001; 65(10): 960–8.
9. Pitts NB, Stamm JW. International Consensus Workshop on Caries Clinical Trials (ICW-CCT)--final consensus statements: agreeing where the evidence leads. J Dent Res. 2004; 83 Spec No C: 125–8.
10. Baelum V, Heidmann J, Nyvad B. Dental caries paradigms in diagnosis and diagnostic research. Eur J Oral Sci. 2006; 114(4): 263–77.
11. Zandona AF, Zero DT. Diagnostic tools for early caries detection. J Am Dent Assoc. 2006; 137(12): 1675–84; quiz 730.
12. Pereira AC, Eggertsson H, Martinez-Mier EA, Mialhe FL, Eckert GJ, Zero DT. Validity of caries detection on occlusal surfaces and treatment decisions based on results from multiple caries-detection methods. Eur J Oral Sci. 2009; 117(1): 51–7.
13. Nyvad B. Diagnosis versus detection of caries. Caries Res. 2004; 38(3): 192–8.
14. Elderton RJ. Clinical studies concerning re-restoration of teeth. Adv Dent Res. 1990; 4: 4–9.
15. Klingberg G, Raadal M, Arnrup K. Dental fear and behavior management problems. In: Koch G, Poulsen S, editors. Pediatric Dentistry – A Clinical Approach. 2 ed: Blackwell Publishing Ltd.; 2009. p. 32–43.
16. Wendt LK, Koch G, Birkhed D. Replacements of restorations in the primary and young permanent dentition. Swed Dent J. 1998; 22(4): 149–55.
17. Alm A, Wendt LK, Koch G. Dental treatment in the primary dentition of 7–12 year-old Swedish schoolchildren. Swed Dent J. 2003; 27(2): 77–82.
18. Pitts NB. Are we ready to move from operative to non-operative/preventive treatment of dental caries in clinical practice? Caries Res. 2004; 38(3): 294–304.
19. Mount GJ. A new paradigm for operative dentistry. Aust Dent J. 2007; 52(4): 264–70; quiz 342.
20. Mejàre I, Raadal M, Espelid I. Diagnosis and management of dental caries. In: Koch G, Poulsen S, editors. Pediatric dentistry – A clinical approach: Wiley-Blackwell; 2009. p. 110–37.
21. Pitts NB, Wefel JS. Remineralization/desensitization: what is known? What is the future? Adv Dent Res. 2009; 21(1): 83–6.
22. Featherstone JD. Remineralization, the natural caries repair process–-the need for new approaches. Adv Dent Res. 2009; 21(1): 4–7.
23. Stahl J, Zandona AF. Rationale and protocol for the treatment of non-cavitated smooth surface carious lesions. Gen Dent. 2007; 55(2): 105–11.
24. Ahovuo-Saloranta A, Hiiri A, Nordblad A, Makela M, Worthington HV. Pit and fissure sealants for preventing dental decay in the permanent teeth of children and adolescents. Cochrane Database Syst Rev. 2008(4): CD001830.
25. Karies – diagnostik, riskbedömning och icke-invasiv behandling. Stockholm: SBU Kunskapscentrum för hälso- och sjukvården, 2007.
26. Att förebygga karies. Stockholm: SBU Kunskapscentrum för hälso- och sjukvården, 2002.
27. Marinho VC, Higgins JP, Sheiham A, Logan S. Fluoride toothpastes for preventing dental caries in children and adolescents. Cochrane Database Syst Rev. 2003(1): CD002278.
28. Marinho VC, Higgins JP, Sheiham A, Logan S. Combinations of topical fluoride (toothpastes, mouthrinses, gels, varnishes) versus single topical fluoride for preventing dental caries in children and adolescents. Cochrane Database Syst Rev. 2004(1): CD002781.
29. David J, Raadal M, Wang NJ, Strand GV. Caries increment and prediction from 12 to 18 years of age: a follow-up study. Eur Arch Paediatr Dent. 2006; 7(1): 31–7.
30. Raadal M, Amarante E, Espelid I. Prevalence, severity and distribution of caries in a group of 5-year-old Norwegian children. Eur J Paediatr Dent. 2000; 1(1): 13–20.
31. Skeie MS, Raadal M, Strand GV, Espelid I. Caries in primary teeth at 5 and 10 years of age: a longitudinal study. Eur J Paediatr Dent. 2004; 5(4): 194–202.
32. Caufield PW, Dasanayake AP, Li Y. The antimicrobial approach to caries management. J Dent Educ. 2001; 65(10): 1091–5.
33. Newbrun E. Topical fluorides in caries prevention and management: a North American perspective. J Dent Educ. 2001; 65(10): 1078–83.
34. Modeer T, Twetman S, Bergstrand, F. Three-year study of the effect of fluoride varnish (Duraphat) on proximal caries progression in teenagers. Scand J Dent Res. 1984; 92: 400–7.
35. Reynolds EC. Calcium phosphate-based remineralization systems: scientific evidence? Aust Dent J. 2008; 53(3): 268–73.
36. Reynolds EC. Casein phosphopeptide-amorphous calcium phosphate: the scientific evidence. Adv Dent Res. 2009; 21(1): 25–9.
37. Brochner A, Christensen C, Kristensen B, Tranaeus S, Karlsson L, Sonnesen L, et al. Treatment of post-orthodontic white spot lesions with casein phosphopeptide-stabilised amorphous calcium phosphate. Clin Oral Investig; (In press).
38. Twetman S. Antimicrobials in future caries control? A review with special reference to chlorhexidine treatment. Caries Res. 2004; 38(3): 223–9.
39. Zhang Q, van Palenstein Helderman WH, van"t Hof MA, Truin GJ. Chlorhexidine varnish for preventing dental caries in children, adolescents and young adults: a systematic review. Eur J Oral Sci. 2006; 114(6): 449–55.
40. Azarpazhooh A, Limeback H. The application of ozone in dentistry: a systematic review of literature. J Dent. 2008; 36(2): 104–16.
41. Rickard GD, Richardson R, Johnson T, McColl D, Hooper L. Ozone therapy for the treatment of dental caries. Cochrane Database Syst Rev. 2004(3): CD004153.
42. Espelid I. Ozonterapi-en nyttig metode i odontologisk praksis? . In: Holmstrup P, editor. Odontologi 2007. København: Munksgaard; 2007. p. 149–62
43. Oong EM, Griffin SO, Kohn WG, Gooch BF, Caufield PW. The effect of dental sealants on bacteria levels in caries lesions: a review of the evidence. J Am Dent Assoc. 2008; 139(3): 271–8; quiz 357–8.
44. Raadal M, Utkilen AB, Nilsen OL. Fissure sealing with a light-cured resin-reinforced glass-ionomer cement (Vitrebond) compared with a resin sealant. Int J Pediatr Dent. 1996; 6(4): 235–9.
45. Skartveit L, Tveit AB, Totdal B, Övrebö RC, Raadal M. In vivo fluoride uptake in enamel and dentin from fluoride-containing materials. J Dent Child. 1990; 57(2): 97–100.
46. Splieth CH, Ekstrand KR, Alkilzy M, Clarkson J, Meyer-Lueckel H, Martignon S, et al. Sealants in Dentistry: Outcomes of the ORCA Saturday Afternoon Symposium 2007. Caries Res. 2009; 44(1): 3–13.
47. Horowitz AM. A report on the NIH Consensus Development Conference on Diagnosis and Management of Dental Caries Throughout Life. J Dent Res. 2004; 83 Spec No C: 15–7.
48. Bader JD, Shugars DA, Rozier G, Lohr KN, Bonito AJ, Nelson JP, et al. Diagnosis and management of dental caries. Evid Rep Technol Assess (Summ). 2001; (36): 1–4.
49. Zero DT, Fontana M, Martinez-Mier EA, Ferreira-Zandona A, Ando M, Gonzalez-Cabezas C, et al. The biology, prevention, diagnosis and treatment of dental caries: scientific advances in the United States. J Am Dent Assoc. 2009; 140 Suppl 1: 25S–34S.
50. Preventing Dental Caries in Children at High Caries Risk. Targeted prevention of dental caries in the permanent teeth of 6–16 year olds presenting for dental care. SIGN Publication No. 472000.
51. Diagnosis and management of dental caries throughout life. NIH Consens Statement. 2001; 26–28; 18(1): 1–23.
52. Ekstrand KR, Christiansen ME. Outcomes of a non-operative caries treatment programme for children and adolescents. Caries Res. 2005; 39(6): 455–67.
53. Hausen H, Seppa L, Poutanen R, Niinimaa A, Lahti S, Karkkainen S, et al. Noninvasive control of dental caries in children with active initial lesions. A randomized clinical trial. Caries Res. 2007; 41(5): 384–91.
54. Hietasalo P, Seppa L, Lahti S, Niinimaa A, Kallio J, Aronen P, et al. Cost-effectiveness of an experimental caries-control regimen in a 3.4–yr randomized clinical trial among 11–12-yr-old Finnish schoolchildren. Eur J Oral Sci. 2009; 117(6): 728–33.
55. Hietasalo P, Seppa L, Niinimaa A, Kallio J, Lahti S, Hausen H. Post-trial costs, clinical outcomes, and dental service utilization after a randomized clinical trial for caries control among Finnish adolescents. Eur J Oral Sci. 2010; 118(3): 265–9.
Adresse: Magne Raadal, Institutt for klinisk odontologi, Årstadveien 17, 5009 Bergen. E-post: magne.raadal@iko.uib.no
Artikkelen har gjennomgått ekstern faglig vurdering.
Artikkelen er fagfellevurdert.
Artikkelen siteres som:
Raadal M, Espelid I, Crossner C. Non-operativ vs operativ behandling av karies blant barn og unge. Nor Tannlegeforen Tid. 2011;121:10–17. doi:10.56373/2011-1-11