Kardiovaskulær sygdom og odontologi
overlæge, ph.d., Kardiologisk afdeling Y, Bispebjerg Hospital
overlæge, klinisk lektor, FESC, Kardiologisk afdeling Y, Bispebjerg Hospital
En tiltagende stor del af befolkningen vil fremover være i blodfortyndende medicinsk behandling. Dette skyldes såvel aldringen i befolkningen som nye guidelines for patienter med hjertesygdomme. Der er således gennem de sidste par år tilkommet flere nye effektive blodfortyndende præparater til gavn for patienter med såvel atrieflimmer (forkammerflimmer) som iskæmisk hjertesygdom. Dette muliggør øget blødningsrisiko, og opmærksomheden bør derfor skærpes omkring patienters medicinering før tandindgreb med eventuel blødningsrisiko.
Det er efterhånden fastslået, at de immunologiske anomalier, som ligger til grund for arteriosklerose, som sammen med hypertension er den mest udbredte hjerte-kar-sygdom, har en fælles baggrund med en række odontologiske sygdomme som fx marginal parodontitis og gingivitis (1,2). Dette aspekt vil blive beskrevet under parodontitis og kardiovaskulær sygdom i en efterfølgende artikel i dette tema om patienter med svækket helbred i Tandlægebladet. Ud over ovennævnte foreligger kardiologisk-odontologiske fællessygdomme som endocarditis med udgangspunkt i infektiøst fokus i tænderne samt endocarditisprofylakse ved odontologiske indgreb, som er omtalt i artiklen om antibiotikaprofylakse i første del af dette tema (Tidende nr. 1, 2012). Hertil kommer en række meget udbredte kardiovaskulære sygdomme, hvor antikoagulationsbehandling og anden antitrombotisk behandling kan medføre øget blødningstendens ved odontologiske indgreb, og som derfor frembyder et væsentligt fælles klinisk problemområde mellem kardiolog og odontolog. Det drejer sig hovedsageligt om patienter med kunstige hjerteklapper, lungeemboli, dybe venetromboser og atrieflimren (AF), hvoraf AF er langt den mest udbredte lidelse, hvorfor primært forholdene omkring AF vil blive omtalt nedenfor. Med de fælleseuropæiske guidelines for behandling af atrieflimren, som blev publiceret i oktober 2010 (3), bragte man fokus på forebyggelse af iskæmisk apopleksi (blodprop i hjernen) gennem en mere sofistikeret diagnostik og behandling med især antikoagulerende medikamenter og dermed følgende øget blødningsrisiko ved odontologiske indgreb.
Om atrieflimren (AF)
Baggrunden for ovenfor nævnte rapport er alvorlig nok. Gennem de sidste 20 år har man set en stigning i forekomst af atrieflimren, så den nu fremstår som den almindeligste hjerterytmesygdom, der omfatter 1 - 2 % af befolkningen. Prævalensen er herudover estimeret til en fordobling inden for de næste 50 år på baggrund af aldringen i befolkningen. Prævalensen stiger således med alderen fra 0,5 % ved 40 - 50-års-alderen til 5 - 15 % ved 80-års-alderen. Mænd er oftere ramt end kvinder. Risikoen for senere i livet at udvikle atrieflimren er således ca. 25 % hos en 40-årig (3). I Danmark er aktuelt fundet en forekomst ved 65 år på 5 %, ved 75 år 8 - 9 % og ved 85 år på 15 % (4). Atrieflimren medfører en femdobling af risikoen for apopleksi. Således kan et ud af fem tilfælde af apopleksi tilskrives atrieflimren (5). Ydermere er de tilfælde af apopleksi, der opstår ved atrieflimren, oftere fatale, ligesom de, der overlever, har større risiko for ny apopleksi (3). På denne baggrund foreligger en omfattende forskning, som nu har medført nye fælleseuropæiske guidelines for forebyggelse med vægt på OAC-behandling (Oral Anti Coagulations- behandling, i praksis Vitamin K Antagonist (VKA)-behandling, Marevan) eller som alternativ til visse patienter, den nylig registrerede trombinhæmmer Dabigatran (Pradaxa).
Diagnosen af atrieflimren
Atrieflimren er en elektrokardiografisk (EKG)-diagnose. Klinisk skal enhver uregelmæssig puls give mistanke om atrieflimren og derfor søges diagnosticeret ved EKG. Tilstanden forekommer i flere kliniske former, som opdeles i paroksystisk AF, hvor AF kommer og går med varighed af det enkelte anfald mindre end syv dage (oftest < 48 timer), persisterende AF, hvor det enkelte anfald varer mere end syv dage og kræver behandling med medikamenter eller elektrisk stød (DC-stød) for at svinde, og langvarigt persisterende AF, hvor AF har varet mere end et år, og endelig permanent AF, hvor tilstanden er accepteret af patient og læge som permanent. Hertil kommer stum AF, hvor patienten ikke mærker AF, som kan omfatte en af de ovennævnte former. Når diagnosen er stillet, skal patienten vurderes med henblik på behovet for antikoagulationsbehandling.
Trombedannelsen ved atrieflimren
Ved atrieflimren forekommer tumultarisk elektrisk aktivitet i atriemuskulaturen, hvilket medfører ophævet kontraktion og dermed ingen pumpeevne i atrierne. Betydningen for hjertets pumpeevne er ganske beskeden, i størrelsesordenen en nedgang i minutvolumen på ca. 10 %. Dette er uden klinisk og hæmodynamisk betydning ved normal hjertepumpefunktion med et minutvolumen på 5 - 6 liter, som under aktivitet kan øges til det tre- til firedobbelte afhængigt af individets kondition. Hvad der derimod betyder noget, er, at der ved stilstand i atriemuskulaturen opstår områder i atrierne, hvor blodstrømmen er ophævet, hvilket medfører omdannelse af protrombin til trombin (faktor IIa), som indgår i koagulationskaskaden. Trombin er et enzym, som katalyserer omdannelsen af proteinet fibrinogen til fibrin, der hermed udfælder til et fibrinnetværk, som så opfanger de røde blodlegemer, og der dannes en trombe. Prædilektationsstedet er i venstre atriums aurikel, hvorfra det antages, at omkring 80 - 90 % af embolierne udgår (6).
Risikoen for udvikling af iskæmisk apopleksi (embolisk blodprop i hjernen) ved atrieflimren
Risikoen afhænger af et sammenfald af en række risikofaktorer hos den enkelte patient og udtrykkes i den såkaldte CHA2DS2VASc score (tabel 1), der danner baggrund for indikation for de forskellige former for antitrombotisk behandling.
Bogstav |
Risikofaktorer |
CHA2DS2VAScScore |
|---|---|---|
C (congestive heart failure) |
Hjertesvigt (nylig opstået) / venstre ventrikel dysfunktion |
1 |
H |
Hypertension (eller anamnese med hypertension) |
1 |
A |
Alder 75 år (major risikofaktor) |
2 |
D |
Diabetes mellitus |
1 |
S |
Stroke/TCI/systemisk emboli (major risikofaktor) |
2 |
V |
Vaskulær sygdom (tidligere infarkt, perifer arteriel sygdom, plaque i aorta) |
1 |
A |
Alder 65 - 74 |
1 |
Sc(sex) |
Køn (kvinde 1 point) |
1 |
Max score |
9 |
|
Risikofaktorer |
CHA2DS2VASc score |
Antitrombotisk terapi |
1 major risikofaktor eller 2 non-major risikofaktorer |
2 |
OAC |
1 non-major risikofaktor |
1 |
Enten OAC eller ASA*, OAC foretrækkkes |
Ingen risikofaktorer |
0 |
Enten ASA eller ingen antitrombotisk terapi. Der anbefales ingen antitrombotisk terapi |
Risikoen for blødning ved antitrombotisk behandling af atrieflimren
Der foreligger imidlertid en vanskelig balancegang mellem gevinsten af antitrombotisk behandling i forhold til blødningsrisikoen, hvilket er søgt kvantificeret i den såkaldte HAS-BLED risikoscore (tabel 2). En score på 3 betegnes som høj risiko og skal medføre forsigtighed og hyppig kontrol ved enhver antitrombotisk behandling eller direkte fravalg af behandlingen.
Bogstav |
Kliniske karakteristika |
Score |
|---|---|---|
H |
Hypertension |
1 |
A |
Abnorm leverfunktion /abnorm nyrefunktion (1 point for hver) |
1/1 |
S |
Stroke |
1 |
B |
Blødning |
1 |
L |
Labil INR |
1 |
E |
Ældre (alder > 65 år) |
1 |
D |
Medicin (fx blodfortyndende behandling eller NSAID) |
1 |
Alkohol misbrug |
1 |
|
Max score |
9 |
Odontologiske indgreb, VKA- og Dabigatran-behandling
I forbindelse med almenkirurgiske indgreb hos patienter i VKA-behandling og med høj risiko for tromboemboliske komplikationer har man enten overgået til heparin-behandling eller fortsat VKA-behandling med forbigående reduktion i INR (International Normalised Ratio) til 1,5 - 2,0, uden at man med sikkerhed har kunnet anbefale den ene behandlingsstrategi frem for den anden (8). I forbindelse med odontologiske indgreb i form af indsættelse af implantater og tandekstraktioner er det vist, at dette kan foretages uden forudgående ændring i INR, hvis den ligger mellem 2 - 4 forudsat omhyggelig lokal hæmostase med gelatinesvamp, tranexamsyre, silkesuturer, etc. (9,10). Hvad angår Dabigatran-behandling og odontologiske indgreb, findes endnu ingen kliniske serier, som belyser forholdene ved odontologiske indgreb, og indtil videre har man derfor valgt at sidestille de behandlingsmæssige forholdsregler med dem, der gælder for VKA-behandling, dvs. at fortsætte Dabigatran uændret med omhyggelig lokal hæmostase. Hvis der skal foretages større tandindgreb, der er at betragte som et mindre kirurgisk indgreb, pauseres Dabigatran efter retningslinjer som anført i figur 1, idet der tages hensyn til patientens nyrefunktion (10). Hos patienter, der er i marevanbehandling, og hvor der skal foretages større tandindgreb, anbefales det, at man konfererer med kardiolog før seponering af marevan, idet visse patientgrupper bør behandles med innohep subkutant under pausering med marevan.
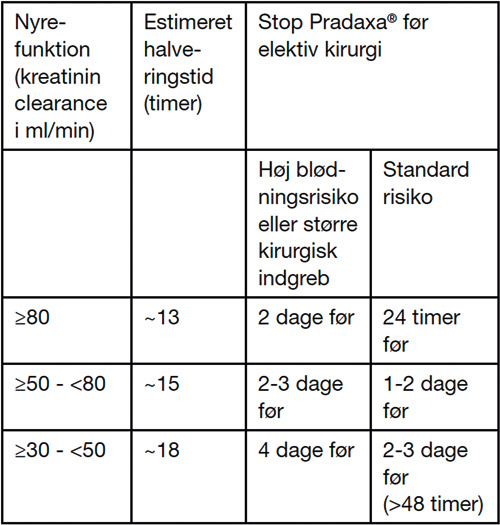
Figur 1. Retningslinjer for Dabigatran-pausering. Pauseringsregler før invasive eller kirurgiske indgreb under Pradaxa-behandling. Fra (10).
Odontologiske indgreb og trombocythæmmerbehandling
Patienter, der har haft en blodprop i hjertet eller har fået påvist betydende koronararteriosklerose, vil ligesom patienter med atrieflimmer være i blodfortyndende behandling. Disse patienter får alle magnyl og en trombocythæmmer enten Clopidogrel (Plavix), Ticagrelor (Brilique) eller Prasugrel (Efient). En del patienter får Clopidogrel, men der er de sidste par år kommet flere nye mere effektive trombocythæmmere på markedet, nemlig Ticagrelor og Prasugrel. Før kirurgiske indgreb anbefales fem dages pause med Clopidogrel og Ticagrelor og syv dages pause med Prasugrel. Hos patienter, der inden for 12 måneder har fået indsat en stent, bør pausering så vidt muligt undgås af hensyn til risikoen for stenttrombose (tillukning af stenten).
Sammenfatning og perspektiv
Med nye fælleseuropæiske guidelines for antitrombotisk behandling af patienter med atrieflimren og koronararteriosklerose må der i fremtiden forventes en markant stigning i antallet af patienter i en sådan behandling med dermed følgende mulig øget blødningsrisiko ved odontologiske indgreb, som nødvendiggør en særlig omhyggelig lokal hæmostase og medicinpausering før større tandindgreb.
English summary
Heitmann M, Sigurd B.
Cardiovascular diseases and odontology. An update of the present position
34-37
In the coming decades an increasing proportion of the population will receive anti-coagulation medicine. This is due to the increasing age of the population as well as implementation of new guidelines for treatment of patients with heart diseases. During the last few years more effective anticoagulation drugs for treatment of atrial fibrillation and ischemic heart disease have been introduced. This increases the risk of bleeding during dental procedures and attention should be paid to patients'' medication before performing dental procedures with potential bleeding risk.
Hovedpunkt | |
|---|---|
· |
Igennem de seneste år er det kommet en række nye, mere effektive blodfortyndende medikamenter på markedet til behandling af patienter med atrieflimren og iskæmisk hjertesygdom. For disse præparater gælder specifikke forhold vedrørende seponering før større tandindgreb, der potentielt kan føre til blødning. |
Referencer
Geismar K, Stoltze K, Sigurd B et al. Periodontal disease and coronary heart disease. J Periodontol. 2006; 77: 1547 - 54.
Holmstrup P. Role of oral pathogens in the pathogenesis of coronary heart disease. In: Watson RR, Larson DF, eds. Immune dysfunction and immunotherapy in heart disease. Malden, Massachusetts: Blackwell Futura, Malden, 2007; 271 - 9.
The Task Force Of The Management of Atrial Fibrillation of The European Society of Cardiology (ESC). Guidelines for the management of atrial fibrillation. Eur Heart J. 2010; 31: 2369 - 2429.
Friberg J. The epidemiology of atrial fibrillation. The Copenhagen City Heart Study. Ph.D. dissertation. The faculty of Health Science of the University of Copenhagen, May 6. 2004.
Sandercock P, Bamford J, Dennis M et al. Atrial fibrillation and stroke: prevalence in different types of stroke and influence on early and long term prognosis (Oxfordshire community stroke project). BMJ. 1992; 305: 1460 - 5
Blackshear JL, Odell JA. Appendage obliteration to reduce stroke in cardiac surgical patients with atrial fibrillation. Ann Thorac Surg. 1996; 61: 755 - 9.
Bacci C, Maglione M, Favero L et al. Management of dental extraction in patients undergoing anticoagulant treatment. Results from a large, multicentre, prospective, case-control study. Thromb Haemost. 2010; 104: 972 - 5.
Larson BJ, Zumberg MS, Kitchens CS. A feasibility study of continuing dose-reduced warfarin for invasive procedures in patients with high thromboembolic risk. Chest. 2005; 127: 922 - 7.
Madrid C, Sanz M. What influence do anticoagulants have on oral implant therapy? A systematic review. Clin Oral Implants. Res. 2009; 20 (Supp 4): S96 - 106.
Pradaxa ordinationsvejledning til forebyggelse af apopleksi ved atrieflimren. Boehringer Ingelheim. 2011.
Adresse: Merete Heitmann, Kadiologisk Afdeling Y, Bispebjerg Hospital, København. E-post: m.heitmann@dadlnet.dk
Artikkelen har gjennomgått ekstern faglig vurdering.