Orale komplikasjoner ved moderne kreftbehandling
tannlege, dr.odont., førsteamanuensis ved Avdeling for oral kirurgi og oral medisin, Institutt for klinisk odontologi, Det odontologiske fakultet, UiO og Avdeling for kjevekirurgi og sykehusodontologi, Radiumhospitalet - Oslo universitetssykehus HF.
tannlege ved Kreftklinikken, Radiumhospitalet - Oslo universitetssykehus HF.
tannlege, lege, PhD, seksjonsoverlege ved Oslo universitetssykehus HF, Avdeling for kjevekirurgi og sykehusodontologi - Rikshospitalet, og professor ved Institutt for klinisk odontologi, Det helsevitenskapelige fakultet, UiT.
Nærmere fire av ti personer vil få kreft en eller annen gang i livet. Kreftbehandling er i dag mer komplisert, aggressiv og individuelt tilpasset enn tidligere. Dette medfører nye og større utfordringer også for tannhelsepersonell. Dødeligheten er stabil eller svakt fallende, noe som innebærer at flere av dem som får kreft overlever sykdommen og vil dø av andre årsaker. Tannhelsepersonell vil derfor møte flere kreftoverlevere som trenger langtidsoppfølging, med henblikk på forebyggelse og håndtering av orale komplikasjoner og seneffekter. Nye intensive behandlingsregimer fører også til at flere kreftpasienter lever lenger med sin sykdom. Bivirkningsprofilen til mange av de nye kreftmedisinene er mindre klarlagt. Sjelden registreres orale komplikasjoner i kreftstudier ved utprøving av nye medisiner. Dette fører til usikkerhet når det gjelder årsakssammenheng mellom orale bivirkninger og kreftbehandlingen. Mistanke om medikamentrelatert oral bivirkning hos kreftpasient bør derfor rapporteres til Staten legemiddelverk via Relis (www.relis.no). Tannhelsepersonell er sjelden inkludert i behandlingsteamet rundt pasienter med kreft utenfor hode-halsområdet. Dette på tross av at orale komplikasjoner forekommer hos opptil 40 % av disse pasientene. Kontinuerlig oppdatering av kunnskap innen onkologisk odontologi er nødvendig, og denne artikkelen fokuserer på de viktigste bivirkninger på kort og lang sikt ved moderne kreftbehandling.
Kreftpasienter lever i dag lenger med sin sykdom, og dette nødvendiggjør økt kunnskap hos alle tannleger om orale bivirkninger på kort og lang sikt ved kreft og kreftbehandling. Kompliserte og langvarige behandlingsregimer fordrer medisinsk-odontologisk tverrfaglig samarbeid for å kunne ivareta pasientenes orale helse på en best mulig måte.
Kreftbehandling i dag er svært avansert og består av kirurgi, stråleterapi, stamcelletransplantasjon, medikamentell behandling og ofte en kombinasjon av disse. Dette medfører nye og større utfordringer, også for tannhelsepersonell (1, 2). Tabell 1 og 2 viser orale komplikasjoner ved ulike former for kreftbehandling, inkludert nye og målrettede medikamenter. National Cancer Institute (www.cancer.gov/) i USA angir følgende estimater når det gjelder frekvens av orale komplikasjoner: 10 % ved adjuvant kjemoterapi, 40 % ved kurativ kjemoterapi, 80 % ved stamcelletransplantasjon og 100 % ved hode-hals-bestråling der munnhulen er involvert.
Komplikasjon/bivirkning |
Kort sikt |
Lang sikt |
||
|---|---|---|---|---|
Stråling |
Cytostatika |
Stråling |
Cytostatika |
|
Mukositt |
+ |
+ |
- |
- |
Infeksjon |
+ |
+ |
+ |
- |
Xerostomi |
+ |
+ |
+ |
+(?) |
Spyttkjerteldysfunksjon |
+ |
+ |
+ |
+(?) |
Smaksforstyrrelser |
+ |
+ |
+ |
+(?) |
Smerte |
+ |
+ |
+(?) |
- |
Blødning |
+ |
+ |
- |
- |
Neuropati |
- |
+ |
- |
- |
Karies |
- |
- |
+ |
+(?) |
Periodontal sykdom |
- |
- |
+ |
+(?) |
Fibrose og atrofi |
- |
- |
+ |
- |
Trismus |
- |
- |
+ |
- |
Osteoradionekrose |
- |
- |
+ |
- |
Dentale og skeletale vekstforstyrrelser (barn) |
- |
- |
+ |
+ |
Ny primær kreftsykdom |
- |
- |
+ |
- |
Behandlingsformer
Kirurgi, som er den viktigste behandlingsform ved hode-og halskreft, kan føre til kosmetiske og funksjonelle komplikasjoner med uttalt effekt på pasientenes livskvalitet.
Høydose tumoricid strålebehandling (60Gy) er den viktigste ikke-kirurgiske behandling for kreft i hode-og halsregionen. Stråleindusert skade skiller seg blant annet fra cytostatika-induserte forandringer ved at bestrålt vev viser mer permanent skade.
Tidligere var medikamentell kreftbehandling ensbetydende med cytotoksisk kjemoterapi, altså cellegiftbehandling med kombinasjon av mange typer cytostatika. Nyutviklede kreftmedikamenter, med målrettet effekt på cellereceptornivå er nå tilgjengelig, og stadig flere er under utprøving (se tabell 2). Dette gir pasienter med avansert kreftsykdom nye livsforlengende behandlingsmuligheter, men medikamentene har også bivirkningsprofiler som kan påvirke pasientenes livskvalitet (3, 4).
Preparat; generisk navn (salgsnavn) |
Behandlingsindikasjon |
Virkningsmekanisme |
Type bivirkninger |
|---|---|---|---|
Bevacizumab (Avastin®) |
Kolorektalkreft, brystkreft, ikke-småcellet lungekreft, nyrecellekreft |
Hemmer binding av vaskulær endotelial vekstfaktor (VEGF) til sine reseptorer |
Stomatitt Nedsatt smakssans Blødning Nedsatt sårtilheling |
Denosumab (Prolia®) |
Prostatakreft med økt risiko for brudd |
Hemmer osteoklastisk benresorpsjon |
Osteonekrose i kjeven |
Denosumab (Xgeva®) |
Forebyggelse av skjelettrelaterte hendelser hos voksne pasienter med skjelettmetastaser fra solide tumorer |
Hemmer osteoklastisk benresorpsjon |
InfeksjonOsteonekrose i kjeven |
Letrozol (Femar®) |
Hormonreseptor-positiv brystkreft |
Hemmer aromataseenzymet ved kompetitiv binding. |
Stomatitt Munntørrhet |
Zoledronsyre (Zometa®)Pamidronsyre (Aredia®) |
Forebygging av skjelettrelaterte hendelser hos pasienter med utbredt kreftsykdom som involverer skjelettet |
Hemmer osteoklastisk benresorpsjon |
Osteonekrose i kjeven Bensmerte Stomatitt Munntørrhet Nedsatt smakssans |
Imatinib (Glivec®) |
Kronisk myelogen leukemi (KML), akutt lymfoblastisk leukemi (ALL), gastrointestinal stromal tumor (GIST) |
Hemmer tyrosinkinasereseptorer |
Munntørrhet Smaksforstyrrelser Stomatitt Sår i munnen |
Sunitinib (Sutent®) |
Gastrointestinal stromal tumor (GIST), nyrecellekreft |
Hemmer flere tyrosinkinasereseptorer som deltar i tumorvekst, neoangiogenese og metastatisk progresjon av kreft |
Stomatitt Munntørrhet Munnsmerter Glossodyni Nedsatt / manglende smakssans Tørre og sprukne lepper Blødning Redusert sårtilheling Osteonekrose i kjeven Oralt ubehag |
Everolimus (Afinitor®) |
Nyrecellekreft |
Hemmer aktiviteten av mTOR |
Stomatitt Smaksforstyrrelser Munntørrhet |
Allogen stamcelletransplantasjon. Transplantasjon av stamceller fra donor (allogen) brukes i behandlingen av forskjellige lymforetikulære kreftsykdommer. I løpet av de siste 25 år har antall pasienter, som har fått slik behandling, økt samtidig med forbedret overlevelsesfrekvens. Dette fordrer økt fokus og håndtering av langtidskomplikasjoner, som kronisk «graft versus host» sykdom (GVHD) og risiko for utvikling av nye maligne sykdommer (5). Akutt GVHD utvikles i løpet av de første 100 dagene av behandlingen og kronisk etter 100 dager. Kronisk GVHD forekommer hos mellom 60 - 80 % av langtidsoverlevere etter stamcelletransplantasjon og mistenkes å være en potensiell risikofaktor for utvikling av plateepitelcarcinom på hud og i munnhule.
Orale komplikasjoner på kort sikt
På kort sikt er oral mukositt (OM) den mest problematiske orale bivirkning ved stråleterapi og medikamentell kreftbehandling.
Oral mukositt
De fleste nye kreftpasienter vil ha en risiko på mellom 20 % og 49 % for å utvikle oral mukositt (OM) en eller annen gang i løpet av behandlingen. OM defineres som en inflammasjonsliknende prosess i oral mucosa som en konsekvens av en kompleks kaskade av biologiske hendelser, der spesifikke transkripsjonsfaktorer (som for eksempel NF-kB) og inflammatoriske mediatorer (som for eksempel COX-2) synes å ha stor betydning (6, 7).
Orale komplikasjoner på lang sikt
De viktigste og alvorligste komplikasjonene på lang sikt ved kreftbehandling generelt er spyttkjerteldysfunksjon, med xerostomi, trismus, risiko for utvikling av osteoradionekrose og medikamentrelatert osteonekrose, samt dentale og skeletale mineraliserings og/eller utviklingsforstyrrelser ved behandling av barn og unge (figur 1,2). (8).
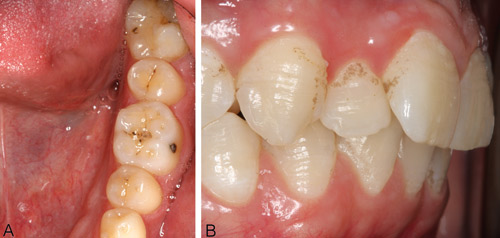
Figur 1. Dentale utviklingsforstyrrelser hos to voksne kreftoverlevere behandlet med cytostatika for akutt lymfatisk leukemi og som deltar i en pågående tverrfaglig PhD-studie om langtidsfølger av kreftbehandling i barne- og ungdomsalder (Wilberg P, Herlofson BB). A: Mikrodonti av tann 37 (også 47) hos 30 år gammel mann behandlet i 2 - 3 årsalder. B: Mineraliseringsforstyrrelser på flere tenner i form av furer og groper hos 18 år gammel mann behandlet fra 2.5 årsalder over tre perioder (foto Wilberg P).
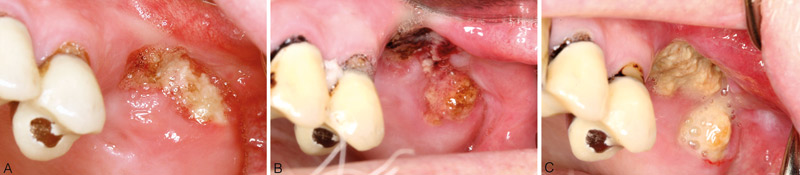
Figur 2. Kjeveosteonekrose (ONJ) med eksponert ben i maxilla etter fjernelse av rotrester (26, 27) hos 67 år gammel nyrekreft pasient med spredning til skjelettet behandlet med zoledronsyre og sunitinib. Totalt fått 19 zoledronsyre-infusjoner, 6 før ekstraksjonen. A: Ved seponering av zoledronsyre og oppstart med 50 mg sunitinib daglig i 4 ukers kurer med 2 ukers pause mellom kurene. B: 6 måneder senere; litt større defekt og mer lettblødende mucosa. Pasienten rapporterer i tillegg økt sårhet i munnen mot slutten av hver sunitinib kur. C: Progresjon av eksponert ben 18 måneder etter seponering av zoledronsyre og fortsatt under behandling med sunitinib. Kombinasjon av bisfosfonat og sunitinib synes å øke risko for ONJ, og kan forverre etablert ONJ (4).
Spyttkjerteldysfunksjon/xerostomi
Spyttkjertelhypofunksjon (objektivt påvist redusert salivasekresjon) og xerostomi (subjektiv følelse av munntørrhet) er velkjente bivirkninger under og etter strålebehandling av hode-halskreft. I en systematisk litteraturgjennomgang er det rapportert en prevalens av xerostomi på 73 - 85 % fra èn måned til mer enn 2 år etter endt strålebehandling (9).
Trismus
Trismus defineres som en tonisk kontraksjon av tyggemuskler med redusert gapeevne som resultat. En prevalens av trismus på mellom 5 % og 38 % av pasienter som får stråling mot hode-halskreft er rapportert, og variasjonene skyldes sannsynligvis fravær av ensartede kriterier for definisjon av trismus. En interincisalavstand på 35mm er derfor foreslått som «cut-off»-grense for trismus (10). Strålebehandling som involverer kjeveledd, pterygoideus- og massetermuskulatur, samt stråledose over 60 Gy, fører til degenerasjon og fibrose av tyggemuskler og kjeveledd med trismus som resultat (11). Dette fører igjen til økt morbiditet med tyggeproblemer som reduserer næringsinntak, vanskeliggjør tale og munnhygiene. Redusert evne til å spise i sosiale lag øker risiko for sosial isolasjon og reduserer pasientenes livskvalitet.
Osteoradionekrose
Osteoradionekrose (ORN) er karakterisert ved et ikke tilhelet område med eksponert ben, som har persistert i minst 6 måneder hos kreftpasient behandlet med ioniserende stråling (12). ORN er assosiert med smerte og morbiditet og krever i avanserte stadier kirurgisk reseksjon og rekonstruksjon. Risiko for ORN øker med stråledose over 60 Gy, tidligere kreftreseksjon, dårlig tannstatus og tannekstraksjoner utført etter endt strålebehandling (13).
Medikamentrelatert osteonekrose
Siden 2003 har osteonekrose i kjevene (ONJ) blitt assosiert med bruk av bisfosfonater i behandlingen av kreftpasienter med skjelettmetastaser og av pasienter med osteoporose. Foreløpig baseres diagnostikk av bisfosfonatrelatert kjeveosteonekrose (BRONJ) på kliniske funn, og defineres som tilstedeværelse av nekrotisk ben i over 6 - 8 uker hos en pasient som behandles eller er behandlet med bisfosfonater, og som ikke har fått stråling mot hode-halsområdet (14). Prevalensen av ONJ hos kreftpasienter som får intravenøst administrert bisfosfonat beskrives i litteraturen å ligge mellom 3 og 12 %, og mindre enn 1 % hos osteoporosepasienter som bruker bisfosfonat per oralt. Tallene er basert på retrospektive studier og kan være biased i måten ONJ-tilfellene ble diagnostisert. Bisfosfonater ligger på overvåkingslisten til Legemiddelverket i de nordiske land, og helsepersonell oppfordres til å rapportere alle tilfeller av ONJ (www.relis.no). I den senere tid er det rapportert ONJ-tilfeller hos kreftpasienter som behandles med andre medikamenter, inkludert antiangiogene- og nyutviklede antiresorptive medikamenter (4, 15, figur 2, tabell 2). Disse preparatene studeres intensivt til bruk innen onkologi og andre applikasjoner, og økt bruk av disse kan forventes i nær fremtid.
Et av de nye antiresorptive medikamentene, denosumab (tabell 2), administreres i form av en subkutan injeksjon. Preparatet er nylig blitt godkjent til behandling av osteoporose (Prolia®, 60mg, 2 ganger i året) og i behandlingen av skjelettmetastaser hos kreftpasienter med solide tumores (Xgeva®, 120mg hver 4 uke). Tannhelsepersonell gjøres oppmerksom på at infeksjon og osteonekrose i kjeven er rapporterte bivirkninger ved denosumabbehandling, hovedsakelig hos kreftpasienter.
Konklusjon
Kreftpasienter lever lenger med sin sykdom ettersom nye og intensive medikamentelle behandlingsregimer implementeres. Tannhelsepersonell må derfor være innstilt på å øke sin kunnskap om orale problemstillinger ved kreft og kreftbehandling, for å kunne bidra til en optimal og helhetlig kreftomsorg. Mer forskning er nødvendig, spesielt for å bedre dokumentasjon av orale bivirkninger på lang sikt ved medikamentell kreftbehandling.
English summary
Herlofson BB, Løken K, Støre G.
Oral complications of modern cancer treatment
130-3.
The current trend in modern advanced cancer treatment involves a more complex and aggressive approach, applying a spectrum of modalities, ranging from surgery and radiotherapy to new chemo- and immunotherapy. They are all responsible for various degrees of oral complications and side effects, representing a challenge to the dental team, both in prophylaxis, diagnosis and treatment of such compromised patients, aiming to improve their quality of life. This presentation brings a survey of the current cancer treatment regimens and their effect on oro-facial tissues.
Hovedpunkter | |
|---|---|
· |
Moderne kreftbehandling er mer aggressiv og individuelt tilpasset enn tidligere, og bivirkningsprofilen er ofte mer komplisert og vanskelig å forutsi, både med tanke på nye medikamenter og behandlingsregimer |
· |
Tannhelsepersonell må forvente å bli eksponert for nye orale problemstillinger og oppfølging av kreftpasienter, som lever lenger med sin sykdom på grunn av mer effektiv og nyere kreftbehandling |
· |
Kontinuerlig faglig oppdatering innen odontologisk onkologi er nødvendig |
Referanser
Hong CHL, Napenas JJ, Hodgson BD, Stokman MA, Mathers-Stauffer V, Elting LS, Spijkervet FKL, Brennan MT. A systematic review of dental disease in patients undergoing cancer therapy. Support Care Cancer. 2010; 18: 1007 - 21.
Herlofson BB, Løken K. Hvordan påvirkes munnhulen av kreftbehandling? Tidsskr Nor Lægeforen. 2006; 126: 1349 - 52.
Sonis S, Treister N, Chawla S, Demetri G, Haluska F. Preliminary characterization of oral lesions associated with inhibitors of mammalian target of Rapamycin in cancer patients. Cancer. 2010; 116: 210 - 5.
Hoefert S, Eufinger H. Sunitinib may raise the risk of bisphosphonate-related osteonecrosis of the jaw: presentation of three cases. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2010; 110: 463 - 9.
Demarosi F, Lodi G, Carrassi A, Soligo D, Sardella A. Oral malignancies following HSCT: Graft versus host disease and other risk factors. Oral Oncol. 2005; 41: 865 - 77.
Sonis ST. Mucositis: The impact, biology and therapeutic opportunities of oral mucositis. Oral Oncol. 2009; 45: 1015 - 20.
Cheng KK, Leung SF, Liang RH, Tai JW, Yeung RM, Thompson DR. Severe oral mucositis associated with cancer therapy: impact on oral functional status and quality of life. Support Care Cancer. 2010; 18: 1477 - 85.
Allen G, Logan R, Gue S. Oral manifestations of cancer treatment in children: A review of the literature. Clin J Oncol Nursing. 2010; 14: 481 - 90.
Jensen SB, Pedersen AM, Vissink A, Andersen E, Brown CG, Davies AN, et al. A systematic review of salivary gland hypofunction and xerostomia induced by cancer therapies: prevalence, severity and impact on quality of life. Support Care Cancer. 2010; 18: 1039 - 60.
Dijkstra PU, Kalk WI, Roodenburg JLN. Trismus in head and neck oncology: a systematic review. Oral Oncol. 2004; 40: 879 - 89.
Wranicz P, Herlofson BB, Evensen JF, Kongsgaard UE. Prevention and treatment of trismus in head and neck cancer: A case report and a systematic review of the literature. Scand J Pain. 2010; 1: 84 - 8.
Marx RE. Osteoradionecrosis: A new consept of its pathophysiology. J Oral Maxillofac Surg. 1983; 41: 283 - 8.
Peterson DE, Doerr W, Hovan A, Pinto A, Saunders D, Elting LS, et al. Osteoradionecrosis in cancer patients: The evidence base for treatment-dependent frequency, current management strategies, and future studies. Support Care Cancer 2010; 18: 1089 - 98.
Ruggiero SL, Dodson TB, Assael LA, Landesberg R, Marx RE, Mehrotra B. American Association of Oral and Maxillofacial Surgeons position paper on bisphosphonate-related osteonecrosis of the jaws - 2009 update. J Oral Maxillofac Surg. 2009; 67: 2 - 12. http://www.aaoms.org/docs/position_papers/bronj_update.pdf
Migliorati CA, Covington JS. New oncology drugs and osteonecrosis of the jaw (ONJ). J Tenn Dent Assoc. 2009; 89: 36 - 8.
Adresse: Bente Brokstad Herlofson, Avdeling for oral kirurgi og oral medisin, Institutt for klinisk odontologi, Det odontologiske fakultet, UiO, P.Box 1109 Blindern, Oslo. E-post: b.b.herlofson@odont.uio.no
Artikkelen har gjennomgått ekstern faglig vurdering.
Herlofson BB, Løken K, Støre G. Orale komplikasjoner ved moderne kreftbehandling. Nor Tannlegeforen Tid. 2012; 122: 130-3.