Medikamentrelatert osteonekrose i kjevene. Del 1: oversikt og retningslinjer
Osteonekrose i kjevene (Eng. «OsteoNecrosis of the Jaws», forkortet ONJ) ses i stigende grad verden over. ONJ er en alvorlig komplikasjon relatert til behandling med bisfosfonater og denosumab, samt også visse kjemoterapeutika. ONJ kan føre til tap av tenner og deler av kjeveben, og invalidisere tyggefunksjon. Antiresorptive medikamenter anvendes hovedsakelig i behandling av skjelettmetastaser ved en rekke maligne tilstander, og mot benskjørhet (osteoporose). I den senere tid benyttes medikamentene også som adjuvant behandling hos postmenopausale kvinner med brystkreft for å redusere risiko for tilbakefall av sykdommen. Artikkelen gir en oversikt over epidemiologi, symptomer, diagnostikk, klinikk og behandling av ONJ. Til slutt gis retningslinjer om hvordan tannhelsepersonell bør forholde seg ved tannbehandling av pasienter på antiresorptiv behandling.
Hovedbudskap | |
|---|---|
· |
Osteonekrose i kjevene (ONJ) relatert til antiresorptiv behandling er globalt økende, og en odontologisk- og medisinsk utfordring. |
· |
Indikasjon for slik behandling er økende, noe som gjør flere pasientgrupper utsatt for utvikling av ONJ. |
· |
Det er rapportert flest ONJ-tilfeller hos kreft- og osteoporosepasienter. |
· |
Tannhelsepersonell vil alle i sin kliniske hverdag måtte håndtere pasienter på antiresorptiv behandling. |
· |
Oppdatert kunnskap om disse medikamentenes effekt på oral helse er viktig i takt med stigende alder i befolkningen og mer komplekse sykdomstilstander. |
Osteonekrose i kjevene (Eng. «OsteoNecrosis of the Jaws, forkortet ONJ) ble for første gang rapportert i USA i 2003 (1). Marx og medarbeidere fant da hva de kalte for «avaskulær nekrose i kjevene» hos en rekke pasienter som var behandlet med pamidronsyre (Aredia®) og zoledronsyre (Zometa®). Herved startet på mange måter en epidemi, som har rammet pasienter verden over der antiresorptive medikamenter benyttes. Bisfosfonater (f.eks. zoledronsyre, pamidronsyre, ibandronsyre eller alendronat) brukes for å styrke skjelettet da de hemmer osteoklastaktivitet. Osteoklaster er celler som resorberer ben som ledd i den fysiologiske benombyggingen. Bisfosfonater har liten effekt på celler som bygger ben, osteoblastene, det vil si at det fortsatt dannes nytt ben, og mineralinnholdet i benvevet økes. Bisfosfonater er vist å være effektive mot smerter og spontanfrakturer (f.eks. kompresjonsfrakturer i ryggsøylen) hos pasienter med skjelettmetastaser og hos osteoporosepasienter på slik behandling.
Nitrogenholdige bisfosfonater har vært brukt i behandling av osteoporose i Norge siden 1995 og siden 2001 for skjelettmetastaser (2). Medikamentene administreres i høy dose ved maligne tilstander, som myelomatose og kreft i bryst og prostata, og i lav dose ved osteoporose. En ny type antiresorptivt medikament, denosumab, kom på markedet i 2010 (Prolia®) og 2011(XGEVA®). Denosumab er et monoklonalt antistoff som er rettet mot RANKL-(Receptor Activator of Nuclear factor Kappa-B Ligand)reseptoren på osteoklastene som dermed inaktiveres. Dette resulterer i redusert bennedbrytning på lik linje som ved bruk av bisfosfonater. Mens bisfosfonater inkorporeres og akkumuleres i benvev og har en halveringstid på mange år, halveres denosumab på 25 - 28 dager og er så godt som ute av kroppen etter 6 - 9 måneder (3). Både bisfosfonater og denosumab kan føre til osteonekrose i kjevene. Tabell 1 viser ulike norskregistrerte preparater.
Generisk navn, salgsnavn (adm.form) |
Behandlingsindikasjon |
Intervall |
Dose |
|---|---|---|---|
Zoledronsyre Zometa® (iv) |
Forebygge skjelettrelaterte
hendelser hos pasienter med skjelettmetastaser. |
4 uker/3 mnd |
4 mg |
Aclasta® (iv) |
Postmenopausal osteoporose og osteoporose hos menn med risiko for frakturer. |
Årlig |
5 mg |
Pamidronsyre Pamidronatdinatrium Hospira® (iv) |
Tumorindusert hyperkalsemi. Skjelettmetastaser fra brystkreft eller benlesjoner fra multippelt myelom. |
4 uker |
90 mg |
Ibandronsyre Bondronat® (tbl/iv*) |
Forebygge skjelettforandringer hos pasienter med brystkreft og skjelettmetastaser. |
Daglig |
50 mg |
Bonviva® (tbl/iv*) |
Postmenopausal osteoporose hos kvinner med risiko for frakturer. |
1 mnd |
150mg |
Klodronat Bonefos® (tbl) |
Tumorindusert hyperkalsemi. Osteolyse pga. maligne prosesser. |
Daglig |
1600 mg |
Alendronat Alendronate® (tbl) Fosamax® (tbl) |
Postmenopausal osteoporose og osteoporose hos menn med risiko for frakturer. |
Ukentlig |
70 mg |
Risedronsyre Optinate Septimum® (tbl) |
Postmenopausal osteoporose og osteoporose hos menn med risiko for frakturer. |
Ukentlig |
35 mg |
Denosumab XGEVA® (sc) |
Forebygge skjelettrelaterte hendelser hos voksne med skjelettmetastaser fra solide tumores. |
4 uker |
120 mg |
Prolia® (sc) |
Postmenopausal osteoporose og osteoporose hos menn med risiko for frakturer. Prostatakreft-pasienter som får hormonbehandling. |
6 mnd |
60 mg |
iv= intravenøst, sc=subcutant, tbl=tablett,
Epidemiologi
Siden 2003 da de første publikasjoner med beskrivelse av ONJ kom (1, 4), er det rapportert tusenvis av tilfeller med økende hyppighet verden over. En rekke oversiktsartikler har beskrevet epidemiologi, som best kan oppsummeres slik: ONJ forekommer i hovedsak sjelden hos osteoporosepasienter, i gjennomsnitt rundt 0,12 %, men hyppigheten varierer i forskjellige studier fra 0,0 til 4,3 % (5). I Norge er nesten 60.000 personer med osteoporose under behandling med bisfosfonater (alendronat) eller denosumab (Prolia®).
Når det gjelder pasienter som behandles med en høy dose bisfosfonat eller denosumab (XGEVA®) er forekomsten av ONJ svært varierende, fra 0 % opp mot 27,5 % (5 - 8). Det er hovedsakelig pasienter med brystkreft, prostatakreft og myelomatose som gis slik behandling. I denne pasientgruppen er forekomsten av ONJ på mellom 5 - 10 %. Mellom 5000 - 7000 pasienter i Norge antas å være under behandling med høy dose bisfosfonat eller denosumab. I tillegg er ONJ rapportert i forbindelse med bruk av nye typer kjemoterapeutika, såkalte tyrosinkinasehemmere (9) (tabell 2). Disse benyttes også i behandling av en rekke kreftsykdommer, med og uten skjelettmetastaser, f.eks. ved kreft i nyre, lunge, og i mage- og tarmsystemet. ONJ i forbindelse med tyrosinkinasehemmere er sjelden forekommende, men er registrert hos noen pasienter. ONJ er også rapportert i forbindelse med behandling med bevacizumab (antineoplastisk medikament) alene og i kombinasjon med zoledronsyre, med en hyppighet på henholdsvis 0,2 % og 0,9 % (9).
Generisk navn, salgsnavn |
Benhandlingsindikasjon |
Virkningsmekanisme |
|---|---|---|
Imatinib Glivec® |
Kronisk myelogen leukemi |
Hemmer tyrosinkinasereseptorer |
Sunitinib Sutent® |
Metastatisk nyrecellekarsinom Imatinib-resistent GISTPankreatisk nevroendokrin tumor |
Hemmer tyrosinkinasereseptorer |
Gefitinib Iressa® |
Lokalavansert eller metastatisk ikke-småcellet lungekreft (NSCLC) med aktiverende mutasjoner |
Hemmer selektivt epidermal vekstfaktorreseptor (EGFR) med tyrosinkinase-aktivitet |
Erlotinibhydroklorid Tarceva® |
NSCLC |
Potent hemmer av den intracellu-lære fosforyleringen av EGFR hos normale celler og kreftceller via type 1- tyrosinkinase-inhibitor |
Sorafenib Nexavar® |
Hepatocellulært karsinom |
Multikinasehemmer som hemmer proliferasjonen av kreftceller in vitro |
Bevacizumab Avastin® |
Nyrecellekreft |
Rekombinant humant monoklonalt antistoff. Hemmer binding av vaskulær endotelial vekst-faktor (VEGF) til sine reseptorer |
Kabozantinib Cometriq® |
Inoperabel eller metastatisk thyroidea-karsinom |
Hemmer tyrosinkinaserreseptorer involvert i tumorvekst og angio-genese, patologisk benremodellering og metastatisk preogresjon av kreft |
Antiresorptive medikamenter
Antiresorptive medikamenter omfatter bisfosfonater og denosumab (10 - 12) (tabell 1).
Bisfosfonater
De mest potente er zoledronsyre (Zometa®) og pamidronsyre (Aredia®). Alendronat, som gis peroralt i tablettform og brukes ved behandling av osteoporose er mindre potent. De to første benyttes hovedsakelig i behandlingen av kreftpasienter med skjelettmetastaser og ved tumorindusert hyperkalsemi og administreres intravenøst (3). En ny indikasjon for bisfosfonatbehandling er zoledronsyre (Zometa®), gitt intravenøst to ganger per år i fem år adjuvant til systemisk behandling av postmenopausale brystkreftpasienter for å redusere risiko for tilbakefall av sykdommen (13). Som tilleggsinformasjon nevnes at zoledronsyre, (Aclasta®, 5mg) også markedsføres og administreres intravenøst en gang per år i behandlingen av osteoporose.
Denosumab
Denosumab er markedsført som XGEVA®(120 mg, månedlig, dvs en høy dose), til behandling av kreftpasienter og som Prolia®(60 mg, hver 6. måned) til behandling av osteoporosepasienter. Begge preparatene gis som subkutan injeksjon.
Hva er behandling med høy dose versus lav dose?
Som det fremgår av teksten over, kan de fleste preparater gis både i høy dose til kreftpasienter med skjelettmetastaser, og i lav dose til osteoporosepasienter. Da de ulike preparatene administreres peroralt, subkutant og intravenøst både i høy- og lav dose, kan ikke administreringsmåten i seg selv brukes til å skille høy fra lav dose. Den viktigste måte å skille mellom høy- og lav dose er å se på behandlingsindikasjon, da kreftpasienter i hovedsak får høy dose og osteoporosepasienter lav. Man bør dog vite at noen kreftpasienter uten metastaser tilbys lav dose i forebyggende øyemed mot osteoporose.
Tyrosinkinasehemmere
Tyrosinkinasehemmere er antiangiogene medikamenter, og benyttes i behandling av en rekke kreftsykdommer (tabell 2) (9, 14 - 16). De mange antiresorptive medikamenter og tyrosinkinasehemmere med sine kompliserte navn, er vanskelig å huske for de fleste pasienter. Dette kan være en utfordring for tannlege og lege når pasientens medikamentanamnese skal registreres. Pasienten bør derfor spørres direkte om vedkommende behandles med medikamenter som er ment å styrke skjelettet og en detaljert medikamentliste bør innhentes.
Når oppstår ONJ etter påbegynt antiresorptiv behandling?
Utvikling av ONJ relatert til bisfosfonater er avhengig av behandlingens varighet og type bisfosfonat, da de mest potente som f.eks. zoledronsyre og pamidronsyre gir tidligere debut av ONJ enn de mindre potente, som for eksempel alendronat. De høypotente benyttes hovedsakelig i behandling av kreftpasienter og i høyere doser enn det som gis til osteoporosepasienter. Fra oppstart med lav dose ved osteoporose til utvikling av ONJ går det vesentlig lengre tid enn ved behandling med høy dose ved malign sykdom. Den gjennomsnittlige behandlingstiden til påvist ONJ for kreftpasienter i den såkalte «Copenhagen ONJ Cohort (n=215, aug. 2015) er 24-30 måneder for bisfosfonatbehandling (kortere tid for zoledronsyre og lengre tid for pamidron og ibandronsyre) (variasjon 1-114 måneder), mens gjennomsnittet er 15 måneder for behandling med høy dose denosumab (XGEVA®). For alendronat er behandlingstiden til påvisning av ONJ, 86 måneder (variasjon 13-142 måneder), mens tiden for denosumab i lav dose (Prolia®) er 39 måneder (variasjon 12-16) måneder (Upubliserte data, Morten Schiødt). Da denosumab har vært på markedet i relativt kort tid, er erfaringene mindre for denne type medikament enn for bisfosfonater.
Terminologi
Siden de første ONJ-tilfeller relatert til bisfosfonater kom i 2003, er det etter 2010 også rapportert osteonekrose relatert til denosumab og tyrosinkinasehemmere. Terminologien er derfor endret fra «bisfosfonat-relatert osteonekrose» til «medikament-relatert osteonekrose» (eng. medication-related osteonecrosis), som tar høyde for ulike typer medikamenter (3).
Definisjon av ONJ
ONJ defineres ved «synlig eksponert ben eller ben som kan sonderes gjennom en fistel, tilstedeværende i minst åtte uker hos en pasient som behandles eller er behandlet med antiresorptive eller antiangiogene medikamenter, og som ikke har fått strålebehandling mot hode- og halsområdet» (3,12, 17-20). Det er også rapportert osteonekrose i kjeven hos pasienter som ikke har synlig eksponert ben eller fistel. Denne type ONJ kalles «non-exposed ONJ» og synes ikke å skille seg biologisk fra «exposed ONJ» (21). Det er økt oppmerksomhet rundt denne formen for ONJ som er anslått å utgjøre opp mot 25 % av alle pasienter med tilstanden (22). Det er særlige utfordringer ved diagnostisering av «non-exposed ONJ». Det er derfor fremmet forslag til kriterier som blant annet krever histologisk påvisning av nekrotisk ben (21). «Non-exposed ONJ» kan i flere tilfeller påvises ut ifra klinikk og billeddiagnostikk, men det er ennå ingen global konsensus om diagnostiske kriterier.
Klassifikasjon
ONJ deles inn i 3 stadier, hvor stadium 1 er uten symptomer, stadium 2 er med symptomer og/eller infeksjon og stadium 3 utgjør de mer avanserte og alvorlige tilfellene (tabell 3). Fordeling av de ulike ONJ-stadier domineres av stadium 1 (13 - 45 % av tilfellene) og stadium 2 (hyppigst med 41 - 60 % av tilfellene), stadium 3 er mindre vanlig (8 - 13 %) (21, 23). I 2009 ble et nytt stadium tilføyet (stadium 0) som omfatter uspesifikke symptomer. Da definisjonen av dette stadiet er noe uklart, synes forfatterne av denne artikkelen at det er vanskelig å bruke dette stadiet ved klassifisering av ONJ. I daglig praksis anbefales inndelingen i 3 stadier (1 - 3), se tabell 3.
ONJ Stadium |
Beskrivelse av ONJ-stadium |
|---|---|
Risikogrupper |
Ikke synlig nekrotisk ben hos pasienter som har vært i behandling med enten peroral eller IV bisfosfonater. |
Stadium 0 |
Ingen kliniske tegn på nekrotisk benvev, men uspesifikke kliniske funn, radiologiske forandringer eller symptomer. |
Stadium 1 |
Eksponert og nekrotisk benvev eller fistel hvor benvev kan sonderes hos pasienter uten symptomer og uten tegn til infeksjon. |
Stadium 2 |
Eksponert og nekrotisk benvev, eller fistel hvor benvev kan sonderes, assosiert med infeksjon, smerte og erytem i området med eksponert benvev, med eller uten pussdannelse. |
Stadium 3 |
Eksponert og nekrotisk benvev, eller en fistel hvor benvev kan sonderes hos pasienter med smerter, infeksjon, og en eller flere av følgende: eksponert og nekrotisk benvev som bres ut over regionen av alveolært benvev,(dvs. inferiore grense (kanalis mandibula), ramus mandibula, sinus maxillaris og zygomaticus), patologisk fraktur, ekstra-oral fistel, oro-antral/oro-nasal kommunikasjon, eller osteolyse ned til inferiore grense av mandibelen eller inn mot sinus maxillaris. |
* Eksponert eller sonderbart benvev i den maksillofaciale regionen uten tilheling i mer enn 8 uker hos pasienter behandlet med antiresorptive og/eller antiangiogene legemidler og som ikke har mottatt bestråling av kjevene.
Uavhengig av hvilket sykdomsstadium bør mobile bensekvestere fjernes. Ekstraksjon av symptomatiske tenner i eksponert, nekrotisk benvev kan vurderes, da det er lite sannsynlig at ekstraksjonen vil forverre den etablerte nekrotiske prosessen.
Demografi og klinikk
ONJ forekommer hyppigst hos kvinner, og disse utgjør to tredeler av pasientene. I de fleste undersøkelser varierer aldersgruppen fra mellom 35 til 95 år, med en gjennomsnittsalder på 65 - 68 år (5, 21, 22). De yngste pasientene som rammes av ONJ er unge kvinner med brystkreft, som tidlig har utviklet skjelettmetastaser og dermed blitt behandlet med antiresorptive medikamenter. De fleste ONJ-pasienter er i aldersgruppen 60-85 år og har oftest brystkreft, prostatakreft, myelomatose, eller sjelden andre typer kreft som i lunge, nyre, mage- og tarmsystem og thyroidea (3). Pasienter med myelomatose utgjorde tidligere størsteparten av kreftpasienter med ONJ, nå er det hyppigst påvist hos de med brystkreft.
Kliniske manifestasjoner
Osteonekrose i kjevene viser seg klinisk ved eksponert ben eller ben som kan sonderes via en intra- eller ekstraoral fistel, ofte i tilslutning til en ikke tilhelet ekstraksjonsalveole. Figur 1 - 7 viser eksempler på en rekke typiske manifestasjoner.
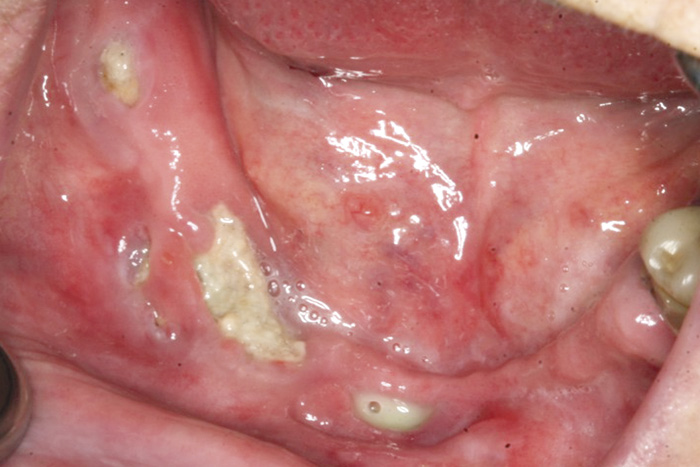
Figur 1. Osteonekrose med multiple områder med eksponert ben i mandibula hos 82-årig kvinne med brystkreft og skjelettmetastaser. Zoledronsyrebehandling (Zometa®) i 30 måneder. Merk pussdannelse anteriort. Pasienten hadde nerveutfall fra høyre n. mentalis region. Osteonekrose stadium 3. Foto: Schiødt M.
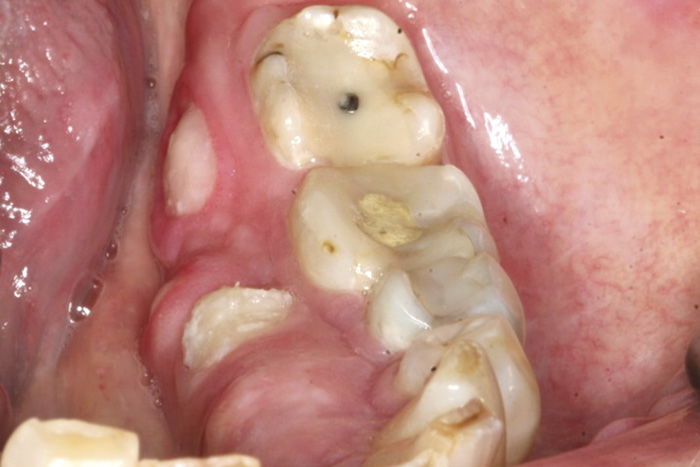
Figur 2. Osteonekrose med eksponert ben svarende til torus mandibularis hos 58-årig kvinne med brystkreft og metastaser behandlet med zoledronsyre (Zometa®) og ibandronsyre (Bondronat®) i 35 måneder. Foto: Schiødt M.
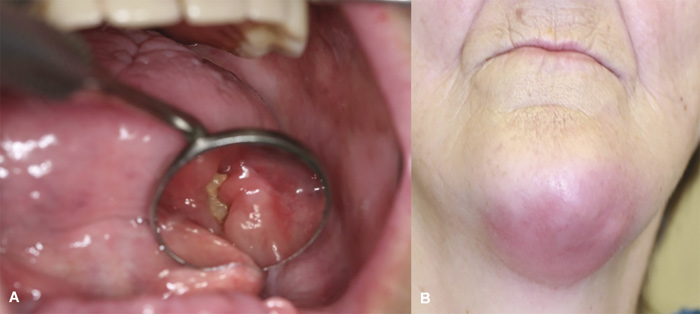
Figur 3 A-B. Osteonekrose og submandibulær abscess hos 72-årig kvinne med myelomatose behandlet med pamidronsyre (Aredia®) i 114 måneder. A: Intraoralt ses eksponert ben i mandibula venstre side. ONJ. B: Submandibulær abscess. Foto: Schiødt M.
Anatomisk forekommer ONJ hyppigst i underkjeven (2/3), og i ca. 8 - 10 % er både over- og underkjeven affisert (21). Fordelingen skiller seg fra osteoradionekrose som kan oppstå etter bestråling mot hode- og halsregionen, som nesten utelukkende forekommer i underkjeven.
Pasienter med torus mandibularis, torus palatinus og andre eksostoser er særlig utsatt for å utvikle ONJ (figur 2). Eksostosene består ofte av kompakt benvev, sparsom blodforsyning og er dekket av en svært tynn slimhinne. ONJ kan her opptre spontant, eller være traumatisk indusert ved for eksempel protesegnag, skade fra avtrykkskje, subgingival kyrretasje eller skade fra laryngoskop ved intubering (24).
De fleste pasienter har kun ett fokus med eksponert ben, mens andre utvikler store og multiple områder med nekrotisk benvev både i maxilla og mandibula (Figur 1). Ved noen tilfeller sees kun en fistel som kan være nesten usynlig og som kan identifiseres ved sondering eller palpasjon der mindre mengder puss kan presses ut. (figur 6A).
I andre tilfeller er det det kun hevelse og smerte, uten fisteldannelse eller eksponert ben, som er tegn på ONJ. Disse tilfellene av «non-exposed ONJ» kan kun diagnostiseres ved en kombinasjon av symptomer og billeddiagnostisk påvisning av nekrotisk ben. Denne typen ONJ er diagnostisk utfordrende og kan være vanskelig å skille differensialdiagnostisk fra periapikal eller periodontal infeksjon. Diagnosen må da baseres på billeddiagnostikk (fig 6B, C), helst i kombinasjon med histologisk påvisning av nekrotisk ben.
Radiologi
Osteonekrose kan vise seg radiologisk som sekvesterdannelse ved et radiopakt område omgitt av en radiolucent sone (fig 4B, 7C). I andre tilfeller ses en ikke tilhelet ekstraksjonsalveole (fig 4B, 5B). Røntgenforandringene kan være lite uttalte eller spesifikke, på tross av relativt uttalte klinske funn ved eksponert ben. Det kan ses områder med økt radiopacitet og radiolucens (osteolyse). Radiologiske tegn på langvarig antiresorptiv behandling kan være utvidet lamina dura rundt tannrøttene, og generelt økt sklerose i kjevene.
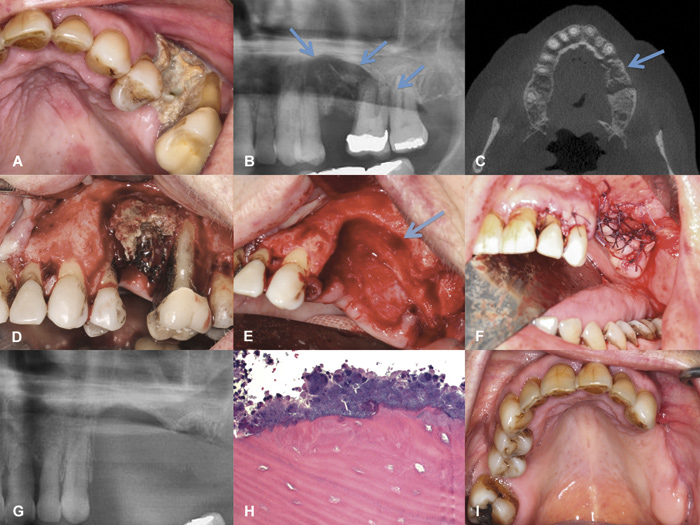
Figur 4 A-I. Eksponert ben regio 24 - 26 hos 62-årig kvinne med osteoporose, behandlet med alendronat i 84 måneder, etterfulgt av denosumab (Prolia®) i 18 måneder, totalt 102 måneder på antiresorptiv behandling. Tann 25 ble fjernet 13 måneder tidligere. Mobile 24 og 26. A: Klinisk eksponert ben. B: Utsnitt av panoramaopptak som viser ikke tilhelet alveole regio 25, og radiolucent process (osteolyse) regio 24 - 27 (pil) med sentralt sekvester. C: CBCT viser et stort sekvester svarende til processus alveolaris i venstre overkjeve (pil). D: Peroperativt. Etter oppklapping ses demarkert sekvester. Merk den grå-grønne fargen på det nekrotiske benvevet. E: Det er fjernet granulasjonsvev, involverte tenner og nekrotisk ben til klinisk vitalt ben. Det er åpning til sinus maxillaris (pil). Merk at ganeslimhinnens periost er eksponert over et større område. F: Primærsuturering. Pasienten ble behandlet med antibiotika i 10 dager postoperativt. G: Postoperativt kontrollrøntgen. H: Histologisk undersøkelse viste nekrotisk ben med tomme osteocyttlakuner og ansamling av bakterier på overflaten. Bildet er stilt til rådighet av Prof. Jesper Reibel ved Tannlægeskolen, Københavns Universitet, Danmark. I: Tilstanden en måned postoperativt viser tilheling. Pasienten er symptomfri og betraktes som helbredet for sin osteonekrose. Pasientens tanntap og tyggefunksjon er gjenopprettet med en delprotese. Foto: Schiødt M.
CT/CBCT scanning
ONJ kan på CT-bilder vise seg som sekvesterdannelse, med radiopake eller radiolucente strukturer slik som ved konvensjonel røntgen. CT-bildene kan vise avgrensningen av det osteonekrotiske området. Det har særlig betydning i maxilla da en eventuell involvering av sinus maxillaris kan identifiseres. En del pasienter med ONJ i posteriore del av maxilla, har ledsagende sinusitt med puss og/eller reaktivt fortykket sinusslimhinne. Deler av bakre sinusvegg og sinusbunn kan også være nekrotisk (figur 6C). I mandibelen posteriort for foramen mentale, er det av særlig betydning å kunne identifisere eventuell involvering av kanalis mandibularis (figur 7C). Rundt 8 % av ONJ-pasienter har utfallssymptomer fra nervus alveolaris inferior som uttrykk for nekrose og inflammasjon i kjevebenet rundt kanalen (21).
SPECT/CT scanning og scintigrafi
Ved scintigrafi av ben, injiseres en radioaktiv isotop i blodet som gir signal i benvev der det foregår benombygging. Dette signalet er uspesifikt og forekommer forekommer ved såvel osteonekrose, inflammasjon og metastaser, noe som kan være en diagnostisk utfordring da 2/3 av ONJ-pasienter er kreftpasienter med skjelettmetastaser. Imidlertid er det sjelden tvil om hvorvidt det er ONJ eller en metastase ut fra den kliniske og radiologiske undersøkelsen. Dersom det foreligger tvil, skal det alltid utføres histologisk undersøkelse av vevet for å verifisere diagnosen. Årsaken til det kraftige signalet ved scintigrafi, er sannsynligvis at den reaktive periostale reaksjon med nydannet ben rundt det nekrotiske gir signal. Det er altså ikke det nekrotiske benvevet i seg selv som gir scintigrafisignalet.
Ved SPECT/CT-scanning kombineres lavdose CT-scanning med scintigrafi og man får et 3D-bilde av ONJ-tilstandens utbredelse. Det er ofte sammenheng mellom det kliniske, radiologiske og scintigrafiske bildet, men i mange tilfeller ser utbredelsen i vevet større ut ved scintigrafi enn ved radiologisk undersøkelse (figur 5D). Disse forhold, inklusiv muligheten for 3D-rekonstruksjon og snittbilder gjennom kjeven for vurdering av sinus maxillaris og kanalis mandibularis med mer, har stor betydning for behandlingsplanlegging.
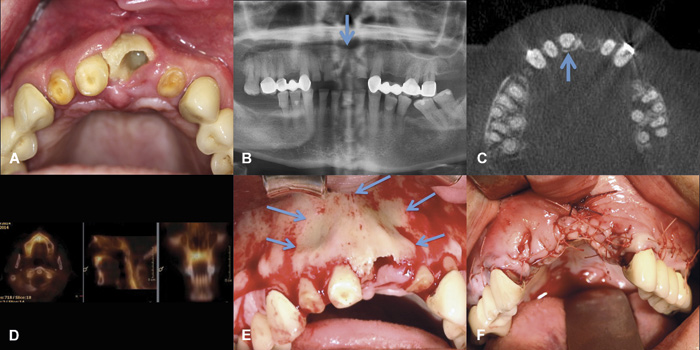
Figur 5. Eksponert ben hos 53-årig kvinne med lungekreft og skjelettmetastaser, behandlet med zoledronsyre (Zometa®) i 16 måneder etterfulgt av denosumab ((XGEVA®) i 15 måneder, totalt 31 måneders antiresorptiv behandling. Pasienten fikk i tillegg en tyrosinkinasehemmer, asatinib. A: Pasienten hadde fått ekstrahert 21 fire måneder tidligere. B: Utsnitt av panoramaopptak viser en ikke tilhelet alveole regio 21 samt gjenstående rotrester. C: CBCT viser tom alveole regio 21, samt osteolyse palatinalt for 21 (pil). D: SPECT-CT scanning viser økt signal i den anteriore del av maxilla, noe som tyder på involvering av hele premaxillen. E: Peroperativt bilde viser utbredt nekrose, omfattende processus alveolaris regio 12 - 22, som ble resecert (piler). Merk den manglende blodforsyningen. F: Primær suturering etter reseksjon av nekrotisk alveolarprosess regio 12 - 22. Foto: Schiødt M.
Behandling av ONJ
Behandlingen avhenger blant annet av tilstandens symptomer og alvorlighetsgrad. Stadium 1, som er uten symptomer, behandles hovedsakelig konservativt med klorheksidin munnskyll eller alternativt saltvannsskyll, etablering av god munnhygiene og jevnlig klinisk kontroll (fig 2). Hvis det eksponerte benet har skarpe kanter som kan gi gnagsår, kan benoverflaten med fordel nivelleres og utjevnes. Enkelte pasienter i stadium 1 blir operert, men det er ikke hovedregelen. Noen få tilfeller av stadium 1 tilheler av seg selv etter spontan avstøtning av sekvestere. De fleste forblir uendret med blottlagt ben, eller utvikler infeksjonssymptomer i form av hevelse, smerte og/eller pussdannelse og går dermed over i stadium 2 (figur1). Disse krever alltid behandling; antibiotika og eventuelt kirurgi. Vanlig penicillin (fenoxymetylpenicillin) pleier å ha god effekt (infeksjonssymptomene reduseres) av og til supplert med metronidazol. Ubehandlet residiverer infeksjonen ofte, og ikke sjelden ses progresjon av tilstanden, spesielt hos kreftpasienter på høye doser antiresorptiva.
Hos pasienter med stadium 2, har det vist seg at kirurgisk fjernelse av nekrotisk ben ved blokkreseksjon og/eller sekvestrektomi etterfulgt av primær bløtvevslukning har ført til tilheling i over 85 % av tilfellene (figur 4,6) (25). Stadium 3 utgjør rundt 10 % og omfatter de mest alvorlige symptomene med blant annet kutan fisteldannelse (figur 7), spontan fraktur (Figur 7) og infeksjon i sinus maxillaris (figur 6). Behandling av disse pasientene krever nesten alltid langvarig antibiotisk behandling og ofte kirurgi (24 - 26).
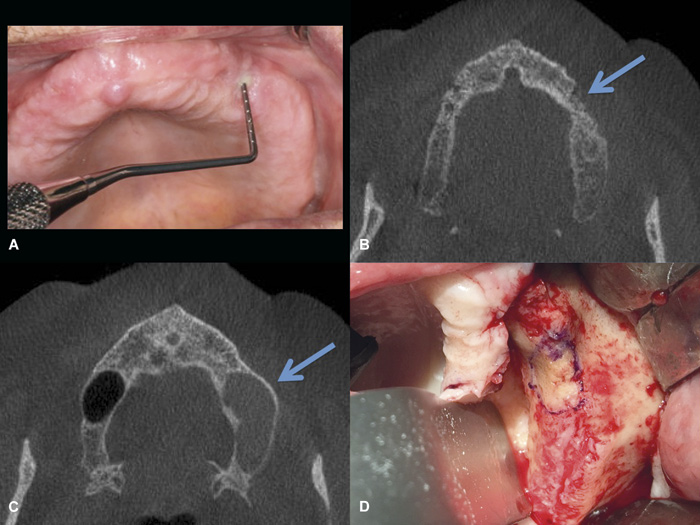
Figur 6 A-D. Non-exposed osteonekrose i maxilla hos 69-årig mann med prostatakreft og metastaser, behandlet med denosumab (XGEVA®) i 19 måneder. Pasienten har smerter i venstre overkjeve. A: Klinisk ses tilsynelatende normal tannløs kjeve, men ved palpasjon og sondering kan det eksprimeres puss gjennom en liten, nesten usynlig fistel som går inn til ben (figur 6B). B: CBCT viser sekvester regio 24,25 (pil). Infeksjonen omfatter også venstre sinus maxillaris. C: Infeksjonen omfatter også venstre sinus maxillaris. D: Peroperativt bilde viser osteonekrose som er opptegnet på benoverflaten. Processen involverer sinus maxillaris, som ble renset for puss og granulasjonsvev, og defekten ble lukket med stilket lapp fra den bukkale fettputen etterfulgt av bløtvevslukning. Ukomplisert tilheling. Foto: Schiødt M.
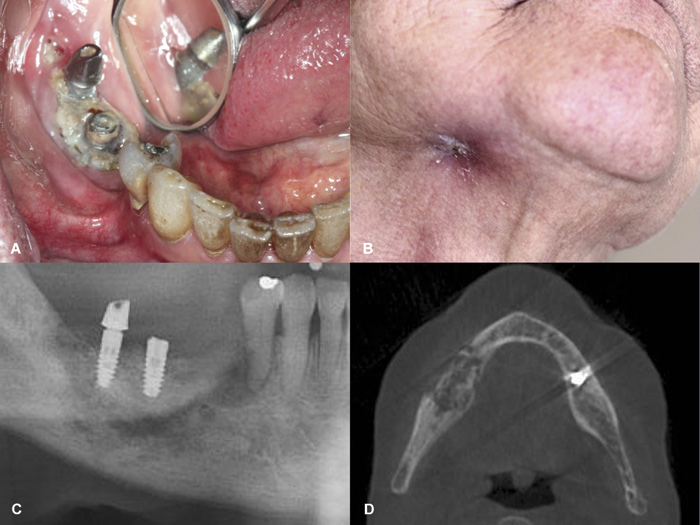
Figur 7. Osteonekrose i høyre mandibula hos 67-årig kvinne med osteoporose behandlet med alendronat i 60 måneder. A: Pasienten har fått innsatt 2 implantater 2 år tidligere og har etter dette utviklet aktuelle tilstand. B: Ekstraoral fistel hvor det siver puss. Betydelig smerte og nedsatt sensibilitet i høyre mentalisregion. Osteonekrose Stadium 3. C: Utsnitt av panoramaopptak viser et sekvester, høyre side av mandibula, som involverer de to implantatene og som er omgitt av en radiolucent sone. Videre ses spontan fraktur av mandibula. D: CBCT viser utbredt osteonekrose i høyre side av mandibula, inklusiv spontan fraktur. Pasienten ble behandlet med en kontinuitetsreseksjon og innsettelse av rekonstruksjonsskinne. Foto: Schiødt M.
Kirurgisk behandling ved stadium 3 med affeksjon av mandibula, kan kreve kontinuitetsreseksjon og innsetting av rekonstruksjonsskinne. I alvorlige, heldigvis sjeldne tilfeller, hvor mandibelen ikke kan rekonstrueres med skinne, kan man anvende fibulatransplantat med sikring av blodforsyningen med mikrovaskulær kirurgisk teknikk. Dette gjøres imidlertid bare dersom pasienten har en rimelig prognose for overlevelse og dersom pasientens helsetilstand er god nok. Noen pasienter med ONJ fremviser en submandibulær eller intraoral abscess som tegn på akutt infeksjon i kombinasjon med blottlagt ben intraoralt (Fig 3). Abscessdannelse kan oppstå på et hvilket som helst tidspunkt i sykdomsforløpet og opptrer i rundt 30 % av tilfellene og er derfor ganske vanlig forekommende. Abscessdannelse er i hovedsak forbundet med ONJ stadium 2 og stadium 3, men operasjonsresultatene synes å være like gode som for de som ikke har abscessdannelse (27).
Generelle retningslinjer for tannleger og leger
Det er samlet en betydelig mengde kunnskap om ONJ siden de første tilfeller ble rapportert i 2003. En rekke organisasjoner har publisert konsensus-artikler vedrørende diagnostikk, behandling og forebyggelse (3, 12, 17 - 20), men det er internasjonal enighet om behov for mer forskning. Forskningsaktiviteten er stor i Norge, Sverige og Danmark og i resten av verden for øvrig. Det forskes innen epidemiologi, klassifikasjon, kliniske manifestasjoner, billeddiagnostikk, risikofaktorer, behandling og i tillegg utføres eksperimentelle studier med dyremodeller og cellekulturer (3, 21, 24, 28 - 32). I de følgende avsnitt beskrives foreløpige retningslinjer og forholdsregler ved antiresorptiv behandling, samt behandling av pasienter med diagnostisert ONJ.
Før oppstart av antiresorptiv behandling
Pasienter som skal begynne på bisfosfonat- eller denosumabbehandling bør informeres om risiko for å utvikle osteonekrose. Risikoen er betraktelig større for kreftpasienter med skjelettmetastaser som skal ha høy medikamentell dose, sammenliknet med osteoporosepasienter der risikoen er lav (3). Risikoen kan reduseres betraktelig ved å fjerne odontogene infeksjonsfoci før oppstart av behandlingen (5, 12, 17, 19, 20, 33).
Alle pasienter anbefales derfor å konsultere egen tannlege for undersøkelse og eventuell behandling. Ideelt sett bør pasientene ikke ha behov for tannekstraksjoner eller annen dentoalveolær kirurgi når antiresorptiv behandling startes. Det er svært viktig at bløtvevstilhelingen etter eventuelle tannekstraksjoner er komplett, før oppstart av behandlingen. Regelmessig tannlegekontroll bør være livslang, da risikoen for å utvikle ONJ øker med varigheten av antiresorptiv terapi (3). I Norge har kreftpasienter med skjelettmetastaser rett til refusjon ved tannbehandling fra Folketrygden gjennom HELFO («gule heftet»), mens kreftpasienter uten metastaser foreløpig ikke har refusjonsrettigheter. Pasienter med bekreftet ONJ har også krav på trygderefusjon.
Under antiresorptiv behandling
Risikoen for å utvikle ONJ etter tannekstraksjon er mye høyere for kreftpasienter som behandles med høy dose bisfosfonat, enn for osteoporosepasienter som gis en mye lavere bisfosfonatdose (34). Da risikoen hos osteoporosepasienter er meget lav, kan tannekstraksjon vanligvis utføres uten problemer hos pasientens egen tannlege. Osteoporosepasienter som får zoledronsyre en gang årlig eller denosumab hver 6 måned, bør ikke få utført kirurgiske inngrep eller tannekstraksjoner like etter at disse medikamentene er gitt. Om mulig bør man vente til det nærmer seg neste infusjon (zoledronsyre) eller injeksjon (denosumab), og i noen tilfeller kan man i tillegg vurdere å forlenge perioden mellom to administreringer i samråd med behandlende lege. Det foreligger ikke evidens for eller mot antibiotikabehandling i forbindelse med tannekstraksjoner hos osteoporosepasienter. Hver pasient bør vurderes individuelt. Tannekstraksjon hos osteoporosepasienter kan utføres som en enkel fjernelse uten primær kirurgisk lukning, men tannlegen bør sikre tilhelingen av alveolen og henvise pasienten til oral/kjevekirurg hvis den ikke er komplett etter 4 uker (34). Det anbefales munnskylling med 0,1 % klorhexidin i tilhelingsperioden inntil tannbørsting kan utføres tilfredsstillende. Pasienter på antiresorptiv behandling er vist å ha en forlenget alveolær tilhelingstid etter tannekstraksjon sammenliknet med pasienter som ikke får slik behandling (35). Tannekstraksjon hos pasienter som behandles med høy dose antiresorptiva (Zometa®, XGEVA®) bør henvises til oral/kjevekirurg, mens ekstraksjoner hos pasienter som får lav dose (Aclasta®, Prolia®) i utgangspunktet kan utføres hos egen tannlege. Annen dentoalveolær kirurgi, som perio- og apikalkirurgi, inklusiv fjerning av retinerte visdomstenner hos pasienter på lav dose uten ytterligere risikofaktorer, kan gjennomføres etter ovenstående retningslinjer.
Implantatbehandling
Innsetting av tannimplantater er en risikofaktor for utvikling av ONJ, men risikoen synes å være lav hos osteoporosepasienter på perorale antiresorptiva. Det anbefales å følge disse pasientene spesielt godt, da implantatproblemer kan oppstå lenge etter innsettelse. I en studie med 82 osteoporosepasienter med tannimplantater, fantes ingen tilfeller av ONJ (36). Således synes innsettelse av tannimplantater å kunne gjøres hos osteoporosepasienter under forutsetning av at det gjøres individuell risikovurdering, med hensyn på benkvalitet og kvantitet, samt andre generelle risikofaktorer som bruk av tobakk, diabetes og annen komorbiditet. Alle pasienter bør informeres om at det foreligger en risiko for utvikling av ONJ og dermed mulighet for tap av implantat. Risikoen er betydelig større for kreftpasienter som behandles med høy dose bisfosfonat, og for denne gruppe er implantatinnsetting i utgangspunktet kontraindisert. Når det gjelder brystkreftpasienter på adjuvant høypotent bisfosfonat (Zometa®) to ganger i året over 5 år, har man foreløpig ikke nok kunnskap til å konkludere, da slik behandling er såpass ny. Oppfølging er viktig, og utover de medikamentrelaterte risikofaktorene, bør man alltid ved en aktuell risikovurdering også være oppmerksom på andre faktorer av betydning som røyking, steroidbehandling og autoimmune sykdommer inkludert diabetes. Når det gjelder pasienter som behandles med denosumab, finnes det foreløpig ikke systematiske data vedrørende implantatbehandling, så inntil videre henvises derfor til avsnittet over om de bisfosfonatbehandlede til vi har studier med fokus på denosumab.
Tannbehandling inkludert tannekstraksjoner hos pasienter med diagnostisert ONJ
Pasienter med diagnostisert ONJ kan få vanlig tannbehandling hos egen tannlege, inkludert tannrens, fyllingsterapi, krone- og brobehandling, endodontisk behandling og lignende som ikke inkluderer kirurgi. Pasienter som har behov for tannekstraksjoner eller annen kirurgi, bør henvises til oral-/kjevekirurg eller til klinikk med erfaring innen håndtering av disse pasientene. Tannekstraksjon bør utføres under antibiotikaparaply, for eksempel vanlig penicillin i 7 dager, og gjøres så atraumatisk som mulig, og bør inkludere alveolektomi og primær bløtvevslukning for ikke å etterlate eksponert benvev. Det pågår en rekke studier som søker å belyse risikoen for utvikling av ONJ etter tannekstraksjoner med primær bløtvevslukning hos pasienter på høy dose antiresorptiv behandling.
Retningslinjer for pasienter der man mistenker ONJ
Pasienter med nyoppdaget ONJ eller hvor man har mistanke om ONJ, bør henvises til oral-/kjevekirurg. Er det eksponert ben, vil man neppe være i tvil, men ved fistel og non-exposed ONJ kan diagnostikken være vanskelig. Det bør primært sikres at det ikke dreier seg om apikal eller marginal periodontitt da det kan behandles hos egen tannlege.
Takk
Forfatterne vil takke Fredrik Haugen Pedersen, Fotoseksjonen, Det odontologiske fakultetet, Universitetet i Oslo, for hjelp med sammensetting av kliniske bilder.
English summary
Herlofson BB, Wexell CL, Nørholt SE, Helgevold J, Schiødt M.
Medication-related osteonecrosis of the jaw, part 1; Overview and mangagement
880-90.
Osteonecrosis of the jaws (ONJ) is an increasing problem all over the world. ONJ is a severe complication to antiresorptive treatment with bisphosphonate, denosumab, and certain chemotherapeutic drugs. ONJ can lead to loss of teeth and parts of the jaw, and invalidate the masticatory function. The antiresorptive treatment is used towards metastases from certain malignant conditions and osteoporosis. Lately, the antiresorptive treatment is also used as an adjuvant treatment in postmenopausal women with breast cancer to reduce risk of recurrence. In this paper the epidemiology, symptoms, diagnostic features, clinical findings, and treatment are reviewed. Finally, guidelines are given for dental treatment, oral surgery, and referral of patients on antiresorptive treatment in the primary health care sector.
førsteamanuensis dr.odont, spes. oral kirurgi og oral medisin. Institutt for klinisk odontologi, Det odontologiske fakultetet, Universitetet i Oslo. Avd. for øre-nese-hals, Tannhelseteamet, Radiumhospitalet, Oslo Universitetssykehus.
overtannlæge, dr.odont. Tand-Mund-Kæbekirurgisk klinik, Rigshospitalet, København, Denmark
övertandläkare, specialist i käkkirurgi, odont.dr. Avd för käkkirurgi, Folktandvården Västra Götaland, Södra Älvsborg Sjukhus, Borås Avd. för biomaterialvetenskap, Inst för kliniska vetenskaper, Sahlgrenska akademin, Göteborgs universitet, Göteborg.
tannlege, forskningsmedarbeider. Avd. for oral kirurgi og oral medisin, Institutt for klinisk odontologi, Det odontologiske fakultet, Universitetet i Oslo, Norge.
overtandlæge, PhD, professor. Avdeling for Tann- og Munn- og kjevekirurgi. Aarhus Universistetssykehus og Seksjon for Kjevekirurgi og Oral Patologi. Institutt for Odontologi. Health. Aarhus Universitet Danmark.
Referanser
Marx RE. Pamidronate (Aredia) and zoledronate (Zometa) induced avascular necrosis of the jaws: a growing epidemic. J Oral Maxillofac Surg. 2003; 61 (9): 1115 - 7.
Herlofson BB. Bisfosfonater - Bivirkninger og komplikasjoner i munnhulen. Munksgaard Danmark, København 2009. Odontologi. 2009; (1); 65 - 84. ISBN; 978 - 87 - 628 - 0878 - 2.s65 - 84.
Ruggiero SL, Dodson TB, Fantasia J, et al. American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw--2014 update. J Oral Maxillofac Surg. 2014; 72(10): 1938 - 56.
Ruggiero SL, Mehrotra B, Rosenberg TJ, et al. Osteonecrosis of the jaws associated with the use of bisphosphonates: a review of 63 cases. J Oral Maxillofac Surg. 2004; 62(5): 527 - 34.
Kuhl S, Walter C, Acham S, et al. Bisphosphonate-related osteonecrosis of the jaws - a review. Oral Oncol. 2012; 48(10): 938 - 47.
Walter C, Al-Nawas B, Grotz KA, et al. Prevalence and risk factors of bisphosphonate-associated osteonecrosis of the jaw in prostate cancer patients with advanced disease treated with zoledronate. Eur Urol. 2008; 54(5): 1066 - 72.
Bamias A, Kastritis E, Bamia C, et al. Osteonecrosis of the jaw in cancer after treatment with bisphosphonates: incidence and risk factors. J Clin Oncol. 2005; 23(34): 8580 - 7.
Yamazaki T, Yamori M, Yamamoto K, et al. Risk of osteomyelitis of the jaw induced by oral bisphosphonates in patients taking medications for osteoporosis: a hospital-based cohort study in Japan. Bone. 2012; 51(5): 882 - 7.
Guarneri V, Miles D, Robert N, et al. Bevacizumab and osteonecrosis of the jaw: incidence and association with bisphosphonate therapy in three large prospective trials in advanced breast cancer. Breast Cancer Res Treat. 2010; 122(1): 181 - 8.
Marx RE, Cillo JE, Jr., Ulloa JJ. Oral bisphosphonate-induced osteonecrosis: risk factors, prediction of risk using serum CTX testing, prevention, and treatment. J Oral Maxillofac Surg. 2007; 65(12): 2397 - 410.
Drake MT, Clarke BL, Khosla S. Bisphosphonates: mechanism of action and role in clinical practice. Mayo Clin Proc. 2008; 83(9): 1032 - 45.
Ruggiero SL, Fantasia J, Carlson E. Bisphosphonate-related osteonecrosis of the jaw: background and guidelines for diagnosis, staging and management. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2006; 102(4): 433 - 41.
Rathbone EJ, Brown JE, Marshall HC, et al. Osteonecrosis of the jaw and oral health-related quality of life after adjuvant zoledronic acid: an adjuvant zoledronic acid to reduce recurrence trial subprotocol (BIG01/04). J Clin Oncol. 2013; 31(21): 2685 - 91.
Brunello A, Saia G, Bedogni A, et al. Worsening of osteonecrosis of the jaw during treatment with sunitinib in a patient with metastatic renal cell carcinoma. Bone. 2009; 44(1): 173 - 5.
Hopp RN, Pucci J, Santos-Silva AR, et al. Osteonecrosis after administration of intravitreous bevacizumab. J Oral Maxillofac Surg. 2012; 70(3): 632 - 5.
Marino R, Orlandi F, Arecco F, et al. Osteonecrosis of the jaw in a patient receiving cabozantinib. Aust Dent J. 2014; dec: 4.10.1111
American Association of Oral and Maxillofacial Surgeons position paper on bisphosphonate-related osteonecrosis of the jaws. J Oral Maxillofac Surg. 2007; 65(3): 369 - 76.
Ruggiero SL, Dodson TB, Assael LA, et al. American Association of Oral and Maxillofacial Surgeons position paper on bisphosphonate-related osteonecrosis of the jaw - 2009 update. Aust Endod J. 2009; 35(3): 119 - 30.
Migliorati CA, Casiglia J, Epstein J, et al. Managing the care of patients with bisphosphonate-associated osteonecrosis: an American Academy of Oral Medicine position paper. JADA. 2005; 136(12): 1658 - 68.
Hellstein JW, Adler RA, Edwards B, et al. Managing the care of patients receiving antiresorptive therapy for prevention and treatment of osteoporosis: executive summary of recommendations from the American Dental Association Council on Scientific Affairs. JADA. 2011; 142(11): 1243 - 51.
Schiodt M, Reibel J, Oturai P, et al. Comparison of nonexposed and exposed bisphosphonate-induced osteonecrosis of the jaws: a retrospective analysis from the Copenhagen cohort and a proposal for an updated classification system. Oral Surg Oral Med Oral Pathol Oral Radiol. 2014; 117(2): 204 - 13.
Fedele S, Bedogni G, Scoletta M, et al. Up to a quarter of patients with osteonecrosis of the jaw associated with antiresorptive agents remain undiagnosed. Br J Oral Maxillofac Surg. 2015; 53(1): 13 - 7.
Di Fede O, Fusco V, Matranga D, et al. Osteonecrosis of the jaws in patients assuming oral bisphosphonates for osteoporosis: a retrospective multi-hospital-based study of 87 Italian cases. Eur J int Med. 2013; 24(8): 784 - 90.
Yazdi PM, Schiodt M. Dentoalveolar trauma and minor trauma as precipitating factors for medication-related osteonecrosis of the jaw (ONJ): a retrospective study of 149 consecutive patients from the Copenhagen ONJ Cohort. Oral Surg Oral Med Oral Pathol Oral Radiol. 2015; 119(4): 416 - 22.
Schiodt M Rostgaard J, Oturai P, et al. Surgical treatment of Bisphosphonate-induced Osteonecrosis of the jaws significantly reduces pain. Association for Oral & Maxillofacial Surgery biannual Congress, Barcelona, Spain. 2013; ICOMS13.
Otto S, Abu-Id MH, Fedele S, et al. Osteoporosis and bisphosphonates-related osteonecrosis of the jaw: not just a sporadic coincidence-a multi-centre study. J Craniomaxillofac Surg. 2011; 39(4): 272 - 7.
Schiodt M. Ahrensburg SS. Does abscess formation affect prognosis and treatment outcome of bisphosphonate-induced osteonecrosis of the jaws? Report from the Copenhagen ONJ Cohort. European Association for Cranio Maxillofacial Surgery Congress. September 2014.
Pautke C, Kreutzer K, Weitz J, et al. Bisphosphonate related osteonecrosis of the jaw: A minipig large animal model. Bone. 2012; 51(3): 592 - 9.
Abtahi J, Agholme F, Aspenberg P. Prevention of osteonecrosis of the jaw by mucoperiosteal coverage in a rat model. Int J Oral Maxillofac Surg. 2013; 42(5): 632 - 6.
Otto S, Pautke C, Opelz C, et al. Osteonecrosis of the jaw: effect of bisphosphonate type, local concentration, and acidic milieu on the pathomechanism. J Oral Maxillofac Surg. 2010; 68(11): 2837 - 45.
Schiodt M, Larsson Wexell C, Herlofson BB, et al. Existing data sources for clinical epidemiology: Scandinavian Cohort for osteonecrosis of the jaw - work in progress and challenges. Clin Epidemiol. 2015; 7: 107 - 16.
Ehrenstein V, Gammelager H, Schiodt M, et al. Evaluation of an ICD-10 algorithm to detect osteonecrosis of the jaw among cancer patients in the Danish National Registry of Patients. Pharmacoepidemiol Drug Saf. 2015 (Epub ahead of print) Published online in Wiley Online Library (wileyonlinelibrary.com) DOI: 10.1002/pds.3786.
Ruggiero S, Gralow J, Marx RE, et al. Practical guidelines for the prevention, diagnosis, and treatment of osteonecrosis of the jaw in patients with cancer. J Oncol Pract. 2006; 2(1): 7 - 14.
Yazdi PM, Schiodt M. Retningslinjer for tandekstraktion på patienter i bisfosfonatbehandling. (Guidelines for tooth extractions on patients in bisphosphonate treatment). Tandlægebladet. 2013; 117: 298 - 305.
Migliorati CA, Saunders D, Conlon MS, et al. Assessing the association between bisphosphonate exposure and delayed mucosal healing after tooth extraction. JADA. 2013; 144(4): 406 - 14.
Koka S, Babu NM, Norell A. Survival of dental implants in post-menopausal bisphosphonate users. J Prosthodont Res. 2010; 54(3): 108 - 11.
Korrespondanse: Bente Brokstad Herlofson, Avdeling for oral kirurgi og oral medisin, Institutt for klinisk odontologi, Det odontologiske fakultet, Universitetet i Oslo, Postboks 1109 Blindern, 0317 Oslo. Epost: b.b.herlofson@odont.uio.no
Artikkelen har gjennomgått ekstern faglig vurdering.
Herlofson BB, Wexell CL, Nørholt SE, Helgevold J, Schiødt M. Medikamentrelatert osteonekrose i kjevene. Del 1: oversikt og retningslinjer. Nor Tannlegeforen Tid. 2015; 125: 880-90.