Obstruktivt søvnapnésyndrom - hvordan kan tannlegen bidra i behandlingen?
Behandling av pasienter med obstruktivt søvnapnésyndrom (OSAS) hos tannlege har i de senere år blitt stadig mer utbredt også i Norge. Fra søvnmedisinsk hold anerkjennes protrusjon av mandibelen ved hjelp av spesialtilpasset skinne som et effektivt tiltak mot snorking og obstruktivt betinget pustestopp under søvn. Fremdeles er likevel kunnskapen om denne behandlingsformen relativt beskjeden både blant leger og tannleger. Behandling er viktig for å redusere forekomst av komorbide tilstander som for eksempel en rekke kardiovaskulære sykdommer. Forutsatt søvnutredning og diagnostisering av sykdom hos ansvarlig behandlende lege, kan tannlege fremstille aktuell skinne. Nært samarbeid og god kommunikasjon mellom lege og tannlege er viktig for optimalt behandlingsresultat. Søvnlegens overordnede behandlingsansvar understrekes. Klare retningslinjer for hvordan et slikt samarbeid best kan foregå, savnes og utvikling av fagprosedyrer på feltet synes overlatt til fagmiljøet selv. Tannlegen må i tillegg til å beherske den tekniske fremstillingsprosedyren for søvnapnéskinner, herunder bestemmelse av mandibelens protrusjonsgrad, ha god kunnskap om respirasjonsrelaterte søvnforstyrrelsers patofysiologi.
Så lenge undervisning i dental søvnmedisin ikke blir gitt under den generelle grunnutdanningen ved norske læresteder, etterlyses et kvalifiserende autorisasjonsprogram.
Fra og med 2012 er det etablert refusjonsordninger via de regionale helseforetakenes behandlingshjelpemiddelenheter for økonomisk bidrag til den enkelte pasient.
Hovedbudskap | |
|---|---|
· |
Udiagnostisert og ubehandlet obstruktivt søvnapnésyndrom (OSAS) kan medføre en rekke systemiske komplikasjoner |
· |
Tannleger kan spille en viktig rolle ved å identifisere og videre henvise pasienter til legespesialist for diagnostisering, samt å behandle OSAS-pasienter med søvnapnéskinne |
· |
Tverrfaglig samarbeid mellom leger og tannleger er viktig for å sikre optimal behandling av pasienter med OSAS |
· |
Tannleger som tilbyr behandling med søvnapnéskinne, bør ha grunnleggende kunnskap om søvnmedisin |
· |
Et kvalifiserende autorisasjonsprogram etterlyses i Norge |
Tannlegers interesse for behandling av søvnforstyrrelser som snorking og pustestopp under søvn har tiltatt markant i løpet av de senere år. Behandling med oralt tilpasset apparatur for bedring av søvnkvalitet ble introdusert på 1980-tallet og behandlingseffekt etter hvert dokumentert i årene som fulgte (1). I løpet av drøye to desennier er det publisert en lang rekke artikler om emnet, inkludert randomiserte kliniske studier (2-4) og omfattende oversiktsartikler (5) der effekten av mandibulære protrusjonsskinner er sammenlignet med andre behandlingsalternativer som for eksempel kirurgiske inngrep og CPAP, eller der forskjellige skinnetyper er vurdert mot hverandre.
I en artikkel i Tidende i 2007 omtalte Johansson og Fondenes (6) prinsippene ved skinnebehandling ved OSAS. Det ble der referert til tallmateriale fra en systematisk litteraturoversikt om OSAS fra Kunnskapssentrene i Norden (7) som viste at behandling med søvnapnéskinne til da var en svært lite benyttet behandlingsform i Norge sammenlignet med de øvrige nordiske landene. I løpet av de siste 7 - 8 årene har imidlertid antall fremstilte skinner økt betydelig også i Norge, mye takket være en til tider meget intensiv informasjons- og kursaktivitet fra enkelte store skinneprodusenter. Fremdeles er imidlertid kunnskapsnivå og klinisk erfaring blant norske tannleger relativt beskjedent (8) og hensikten med denne artikkelen er derfor å gi oppdatert informasjon om hvordan tannleger kan bidra i behandlingen av pasienter med OSAS i samarbeid med søvnmedisinere, samt å belyse virkningsmekanismen ved bruk av søvnapnéskinne.
Definisjon og patofysiologi
Obstruktiv søvnapné (OSA) er en respirasjonsrelatert søvnforstyrrelse ofte med symptomer som snorking og total eller delvis pustestopp av flere sekunders varighet. I ekstremtilfeller kan luftstrømshindringen vare i flere minutter. OSA skyldes kollaps i de øvre luftveiene som fører til totalt opphør (apné) eller betydelig reduksjon (hypopné) av luftstrømmen, til tross for fortsatt respirasjonsanstrengelse. Tilstanden medfører intermitterende reduksjon av oksygenmetningen i blodet. Som en konsekvens utløses vekkerespons hos den sovende pasienten med mikro-oppvåkninger og varierende grad av søvnforstyrrelse, ofte med redusert mengde dyp søvn og REM-søvn.
I en større norsk studie fant Hrubos-Strøm og medarbeidere (9) en forekomst av OSA i aldersgruppen 30 - 65 år på 16 % når OSA ble definert som fem eller flere pustestopp av minimum 10 sekunders varighet per time. Blant menn over 50 år ble det registrert 23 % OSA etter de samme kriterier.
Det er en økt risiko for utvikling av komorbide tilstander som hjerte-kar-sykdom, diabetes mellitus type 2, fedme og kognitiv funksjonssvikt, dersom søvnforstyrrelsen vedvarer. Funn i en amerikansk undersøkelse om komorbide lidelser viser at prevalensen av atrieflimmer, urinsyregikt, hjertesvikt og diabetes type 2 er høyere blant pasienter med OSA enn i befolkningen generelt (10). I tillegg til helsemessige konsekvenser for den enkelte pasient vil uttalt snorking dessuten kunne være en plage for medsovende partner og representere en belastning i parforholdet (11).
Når det hos pasienter med OSA forekommer andre symptomer enn snorking og pustestopp, er det etter gitte kriterier vanlig å betegne sykdomstilstanden som obstruktivt søvnapnésyndrom (OSAS) (12).
Typisk og mest fremtredende symptom i syndromet er uttalt søvnighet på dagtid. Morgenhodepine og konsentrasjonssvikt er vanlig forekommende. Av andre symptomer sees ikke sjelden hyppig trang til urinering på nattetid, nedsatt libido og av og til også depressive tilstander.
Det har lenge vært kjent at OSAS i befolkningen utgjør et stort folkehelseproblem. Tidlige studier har oppgitt prevalens av OSAS blant middelaldrende kvinner og menn til henholdsvis 2 % og 4 % (13). Disse tallene er senere bekreftet i flere andre studier der det også dokumenteres at prevalenstallene for begge kjønn er jevnt stigende med økende alder, men med en avflating etter ca. 65 års alder (14, 15).
Diagnostisering og behandling
Diagnose og sykdommens alvorlighetsgrad bestemmes optimalt ved klinisk utredning og en polysomnografisk undersøkelse (PSG). Full polysomnografi er relativt ressurskrevende og forutsetter normalt innleggelse i sykehus, men kan i prinsippet også utføres ambulant (det vil si mens pasienten sover hjemme i sin egen seng). For hjemmeregistrering blir imidlertid en noe enklere polygrafiundersøkelse (PG) ansett å være tilfredsstillende for å verifisere diagnose når forhåndsundersøkelse indikerer sykdom (16).
Ved den poly(somno)grafiske undersøkelsen registreres blant annet antall totale og delvise pustestopp som varer i 10 sekunder eller lenger, per time under søvn, og klassifiseres ved Apné-Hypopné-Indeks (AHI), som uttrykker alvorlighetsgrad ved summen av apnéer og hypopnéer pr. søvntime, etter følgende norm:
5 ≤ Mild < 15 ≤ Moderat < 30 ≤ Alvorlig
Diagnosen OSAS stilles normalt ubetinget når AHI 15, men kan også stilles allerede fra AHI 5 hvis pasienten samtidig oppviser karakteristiske dagtretthetssymptomer (12).
Sykdommens alvorlighetsgrad er avgjørende for valg av behandling. Kontinuerlig luftveisovertrykk (CPAP) er normalt førstevalgsbehandling ved alvorlig grad av søvnapné. Mer spesialiserte maskeventilasjonsapparater er utviklet for behandling av pasienter med spesielle respirasjonsforstyrrelser (eksempelvis BiPAP - ved hypoventilasjonstilstander og overlappsyndromer, som for eksempel KOLS, og ASV - ved behandling av pasienter med hovedsakelig sentrale apnéer, som for eksempel ved Cheyne Stokes respirasjon).
Kirurgisk korreksjon av den bløte gane og oropharynx (UPPP) og tonsillektomi kan være aktuelt ved behov for modifisering av anatomiske forhold. Omfanget av kirurgisk behandling ved OSAS er imidlertid kraftig redusert i de senere år på grunn av lav grad av vellykkethet (17).
Selv om velfungerende CPAP er dokumentert å være mer effektiv enn søvnapnéskinne ved alvorlig OSAS (18), tyder flere sammenlignende studier på at et flertall pasienter foretrekker å bruke skinne fremfor CPAP (19 - 21). Gitt bedre etterlevelse ved skinnebruk enn CPAP fordi skinne brukes gjennomgående flere timer per natt enn CPAP - så kan det stilles spørsmål ved om ikke behandlingseffekt totalt sett kan likestilles mellom de to behandlingsformene (21). Behandling med søvnapnéskinne er uansett et godt alternativ til CPAP-behandling ved mild til moderat OSAS, og kan også være aktuell for pasienter som er alvorlig rammet, men som ikke responderer på, eller som av en eller annen grunn ikke tolererer eller vil bruke CPAP (22).
Videre kan kombinasjonbehandling med både skinne og CPAP være indisert i tilfeller der det av ulike grunner er nødvendig å senke CPAP-trykket (23).
Forkortelser benyttet i artikkelen | |||
|---|---|---|---|
ASV |
Adaptiv servoventilasjon |
||
BiPAP |
Bilevel positive airway pressure |
||
CPAP |
Continuous positive airway pressure |
||
OSA |
Obstruktiv søvnapné |
||
OSAS |
Obstruktivt søvnapnésyndrom |
||
KOLS |
Kronisk obstruktiv lungesykdom |
||
UPPP |
Uvulopalatopharyngoplastikk |
||
Dersom pasienten er overvektig, er innledende informasjon og oppmuntring til vektreduksjon viktig. Endring av sovestilling fra ryggleie til sideleie kan også ha betydning. Uavhengig av behandlingstype tilstrebes opphør av kliniske symptomer og reduksjon av AHI. Det er vanlig å anse behandling som helt vellykket om AHI reduseres til <5, eller også som relativt vellykket om AHI reduseres med mer enn 50 % fra baseline (24).
Ved rutineundersøkelse for ordinær tannbehandling kan tannlegen som førstelinjehelsepersonell bidra til å oppdage tegn og symptomer på OSAS. Lang bløt gane, smal mandibel og stor tunge er vesentlige anatomiske risikofaktorer. Ved mistanke om OSAS bør tannlegen kunne spørre pasienten om snorking, dagtretthet, høyt blodtrykk og for eksempel om hyppighet av nattlig urinering. Epworth søvnighetsskala (ESS) kan være et nyttig verktøy også for tannleger (25). Testen er enkel og består i at pasienten skriftlig besvarer spørsmål om egen tendens til å døse av eller sovne i åtte spesifikke hverdagssituasjoner med en tallverdi fra 0 - 3 (tabell 1). Om pasienten til sammen scorer 10 eller mer på ESS-testen, og en eller flere av forannevnte symptomer eller anatomiske varianter foreligger, bør pasientens fastlege kontaktes for videre henvisning til en søvnspesialist- vanligvis en øre-nese-hals-spesialist, nevrolog eller lungespesialist. Validitet og reliabilitet ved ESS-testen mot forekomst av OSAS er funnet å være tilfredsstillende i flere studier (26, 27).
Hvor sannsynlig er det at du døser av eller sovner i følgende situasjoner, i motsetning til kun å føle deg trett?Bruk følgende skala for å velge det mest passende tallet for hver situasjon. | |||
|---|---|---|---|
Ville aldri døse/sovne |
0 |
||
Liten sjanse for å døse/sovne |
1 |
||
Moderat sjanse for å døse/sovne |
2 |
||
Stor sjanse for å døse/sovne |
3 |
||
Sitte og lese |
|||
Se på TV |
|||
Sitte, inaktivt på offentlig sted (f.eks på teater eller et møte) |
|||
Som passasjer på en 1-times biltur uten pause |
|||
Legge deg for å hvile om ettermiddagen hvis omstendighetene tillater det |
|||
Sitte og snakke med noen |
|||
Sitte stille etter lunsj (uten å ha inntatt alkohol) |
|||
I en bil, som har stoppet noen få minutter i trafikken |
|||
SUM |
|||
Tannleger kan bidra i behandling av pasienter med diagnostisert OSAS ved tilpasning av søvnapnéskinne. Aktuelle skinnetyper omtales i faglitteratur og reklamebrosjyrer med ulike betegnelser (tabell 2).
SAS = Søvnapnéskinne | ||
AAS = Antiapnéskinne | ||
OA = Oral Appliance | ||
MAS = Mandibular Avancement Splint | ||
MAD = Mandibular Advancement Device | ||
MRA = Mandibular Repositioning Appliance | ||
MRD = Mandibular Repositioning Device | ||
TRD = Tongue Repositioning Device | ||
TSD = Tongue Stabilizing Device |
I norsk medisinsk omtale har betegnelsen «bittskinne» beklageligvis fått et visst innpass. Det er en uheldig betegnelse fordi «bittskinne» i norsk odontologisk begrepsverden har et helt annet terapeutisk anvendelsesområde. Den folkelige betegnelsen «snorkeskinne» er heller ikke helt heldig, og bør unngås fordi snorking per se som oftest bare er et delsymptom i et mer komplekst sykdomsbilde.
Skinnedesign og virkningsmekanisme
En søvnapnéskinne fungerer ved at mandibelen forskyves fremover og samtidig trekker med seg tungen til en relativt stabil protrudert posisjon. Derved økes volumet i de øvre luftveiene særlig ved lateral utvidelse i velopharynx (28). Skinnens konstruksjon forhindrer underkjeven i å sige bakover når pasienten sover, spesielt i ryggleie, og på den måten holdes de øvre luftveiene åpne gjennom natten. Man skal imidlertid være klar over at ikke alle pasienter responderer like effektivt.
Det finnes et rikt utvalg av forskjellige skinnevarianter på markedet (figur 1A-E). Materialet skinnene er laget av, skinnekonstruksjon, protrusjonsmekanisme, grad av vertikal åpning og lateral bevegelsesfrihet er blant de faktorer som varierer. Studier har vist at design kan påvirke behandlingseffekt og pasienttoleranse (29, 30). De to viktigste hovedgrupper av søvnapnéskinner er henholdsvis mono- og bibloc-skinner.
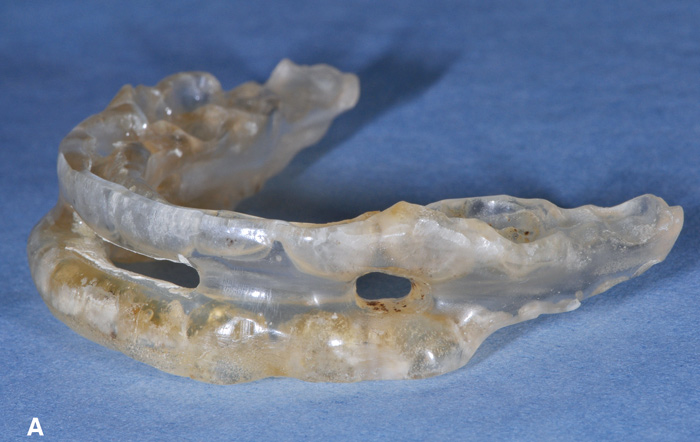
Figur 1A. Velbrukt monobloc søvnapnéskinne.
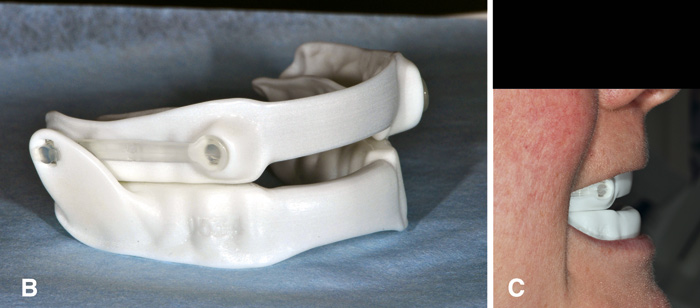
Figur 1B-C. Narval CC® søvapnéskinne.
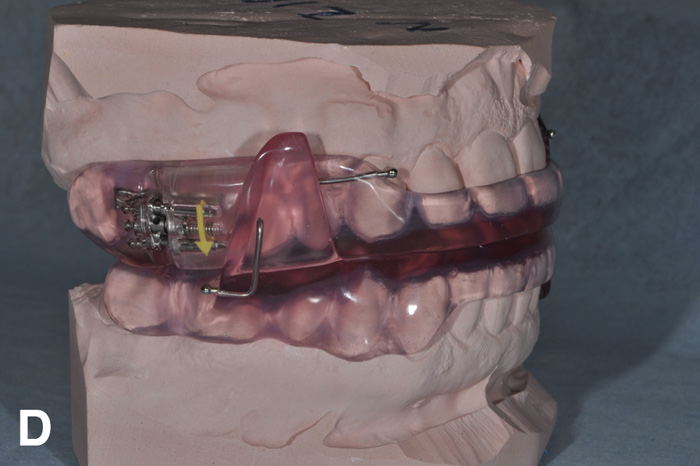
Figur 1D. SomnoDent® søvnapnéskinne.
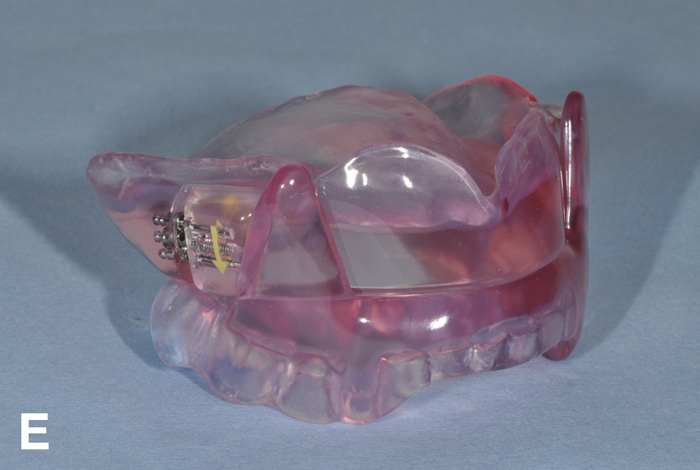
Figur 1E. SomnoDent EDENT® søvnapnéskinne for tannløs overkjeve.
Monobloc-skinnene var de første som kom til anvendelse, men fremstilles nå i langt mindre utstrekning. En monobloc-skinne består av kun én sammenhengende over- og underkjevedel (figur 1A). Ved behov for justering av protrusjonsgraden må over- og underkjevedelene separeres og settes sammen på nytt hos tanntekniker.
Bibloc-skinnene består av to deler, en mandibulær og en maksillær, som retineres til pasientens tenner. En fordel med disse skinnene er at de som regel har en innebygd mulighet for endring av mandibulas posisjon og dermed protrusjonsgraden, enten knyttet til utskiftbare forbindelseselementer mellom de to skinnedelene (figur 1 B-C) eller i form av en innebygd, justerbar protrusjonsmekanisme (figur 1 D-E).
Søvnapnéskinner tilpasses individuelt enten indirekte etter avtrykk og fremstilling i tannteknisk laboratorium eller direkte i pasientens munn basert på prefabrikerte standardsjablonger - såkalte «boil and bite»-skinner. Tannteknikerfremstilte skinner har vist seg langt mer effektive og med vesentlig bedre holdbarhet. Når disse også tillater vertikal åpning og frie laterale bevegelser av mandibelen, gir de mindre risiko for bivirkninger og aksepteres lettere av de fleste pasienter (31).
Normalt forutsettes god betanning i begge kjever og sunn tannhelse for at skinnebehandling skal være aktuell. Som en tommelfingerregel bør pasienten ha minst 8 - 10 friske tenner tilnærmet likt fordelt på hver side av midtlinjen i hver kjeve. For pasienter med total tannløshet i overkjeven og rimelig god betanning i underkjeven finnes riktignok på markedet et bibloc-alternativ (figur 1 E), mens helt tannløse pasienter til en viss grad kan hjelpes med en tungeholder (figur 2) som fungerer ved at tungen «suges» inn og holdes i en anterior posisjon og dermed forhindres fra å falle bakover og blokkere luftveiene. En slik tungeholder er imidlertid nokså ubehagelig å bruke og etterlevelsen er da også funnet å være relativt dårlig (32).

Figur 2. AveoTSD® tungeholder mot søvnapné ved total tannløshet.
Hvor mye bør underkjeven protruderes?
Graden av mandibulær protrusjon er av stor betydning for effekt ved behandling med søvnapnéskinne. For å oppnå ønsket effekt, anbefales at pasienten kan protrudere underkeven minst 5 mm. Behandlingseffekt er rapportert proposjonal med mandibulær protrusjon, det vil si jo større den mandibulære protrusjonen er, alltid målt i forhold til pasientens maksimale protrusjonsevne, desto mer vil AHI-indeks reduseres og normaliseres (33).
Det finnes ingen konsensus med anbefaling om ideell protrusjonsgrad. Antatt positiv doserelatert effekt er noe omdiskutert. Aarab og medarbeidere sammenlignet effekt hos skinnebehandlede pasienter med henholdsvis 0 %, 25 %, 50 % og 75 % protrusjonsgrad ved konstant vertikal dimensjon, og fant signifikant bedring og normalisering av AHI med økende protrusjon (34). Et annet funn i samme undersøkelse var imidlertid at antall bivirkninger tiltok ved protrusjon over 50 %. Walker-Engstrøm og medarbeidere rapporterte lik behandlingseffekt ved 50 % som ved 75 % mandibulær protrusjon hos pasienter med mild til moderat OSA (35). Allment akseptert klinisk erfaring tilsier at terapeutisk protrusjon bør ligge et sted i området 50 - 75 % forutsatt at pasienten tolererer dette. Terapeutisk effekt av mandibelfremførende skinnebehandling er påvist i flere kort- og langtidsstudier (2 - 4, 18, 36, 37).
På markedet finnes flere enkle instrumenter for individuell bestemmelse av protrusjonsgrad; George Gauge (figur 3) er ett eksempel.
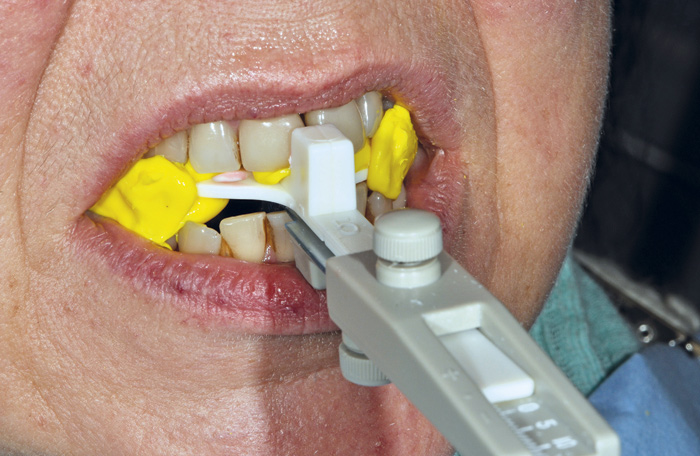
Figur 3. Protrusjonsregistrering ved hjelp av George Gauge.
Vertikal åpning (VO) er også en vesentlig parameter for behandlingseffekten. Ca. 5 mm gapehøyde er gjerne anbefalt som utgangspunkt. I en randomisert kontrollstudie ble to pasientgrupper sammenlignet på forskjellig VO, henholdsvis 4 mm og 14 mm, når samme protrusjonsgrad ble benyttet. I gruppen med 4 mm åpning fikk 74 % av pasientene hel eller delvis behandlingseffekt mens 61 % i gruppen med 14 mm økning oppnådde samme resultat. Delvis behandlingseffekt var da definert som 50 % reduksjon i AHI sammenlignet med behandlingsstart, og fullstendig respons som AHI £ 5. Det ble konkludert at vertikal åpning ikke er av signifikant betydning for behandlingseffekt, men at den har betydning for pasientkomfort. Pasientene foretrakk skinne med 4 mm åpning (30). I en annen studie demonstreres dessuten at pharynxtverrsnittet ved tungebasis vil kunne minske hos de fleste pasienter dersom VO økes for mye, med andre ord vil resultere i redusert luftpassasje og ditto effekt av skinnebehandlingen (38). Økning av den vertikale dimensjon alene uten mandibulær protrusjon kan ellers gi symptomforverring fordi mandibelen og tungebenet da forflyttes posteriort og dermed kan bidra til kollaps av øvre luftveier (39).
Tannlegens plass i behandlingsteamet
Tannleger som tilbyr behandling med søvnapnéskinne, bør ha god kunnskap om søvnmedisin, skinnens virkningsmekanisme og mulige bivirkninger. Kunnskap om søvninduserte fysiologiske endringer i det nevrologiske system, muskel-hjerte- og respiratoriske system i tillegg til kunnskap om symptomer assosiert med respirasjonsrelaterte søvnforstyrrelser er viktig. Videre bør tannlegen forstå ulike diagnostiske tester som utføres av den medisinske søvnspesialisten. Et nært samarbeid mellom tannlege og søvnspesialist er nødvendig for å kunne tilby trygg og effektiv behandling (40, 41).
Fra andre land foreligger beskrevne anbefalinger for slikt samarbeid mellom profesjonene (42, 43). I den grad norske tannleger involveres i behandling av OSAS, synes det å eksistere ulik praksis for hvordan pasienter diagnostiseres og behandles. Per dags dato foreligger ingen formelle retningslinjer for hvilken rolle norske tannleger best og riktigst bør ha i et tverrfaglig behandlingsteam rundt OSAS-pasienten. Følgelig anes en viss bekymring med hensyn til pasientsikkerhet så lenge det er vanskelig å sikre at tjenesten blir levert av kompetente behandlere. Det synes å være behov for at tannleger orienteres bedre om søvnapnébehandling, og det ville være ønskelig om helsemyndighetene involverer seg i problematikken. Forfatterne er kjent med at NTF tidligere har anmodet Helsedirektoratet om at det utarbeides nasjonale faglige retningslinjer på feltet, men så langt har man fra helsepolitisk hold ikke kunnet garantere at dette vil prioriteres. Per i dag synes dermed utvikling av fagprosedyrer på feltet overlatt til fagmiljøet selv.
Søvnmedisin er en tverrfaglig disiplin som involverer fagområdene nevrologi og nevrofysiologi, psykologi og psykiatri, lungemedisin, kardiologi, pediatri, øre-nese-hals og odontologi. Betegnelsen «dental søvnmedisin» har etter hvert vunnet innpass på odontologisk hold.
Det er viktig at tannleger som fatter interesse for å behandle «snorkepasienter» er seg bevisst at pusteforstyrrelser under søvn (eng: Sleep related breathing disorders - SRBD) omfatter mer enn OSAS. Pasientene kan ofte ha flere søvnforstyrrelser samtidig, for eksempel insomni og OSAS, eller også såkalt «overlap syndrome», det vil si kronisk obstruktiv lungesykdom (KOLS) samtidig med OSAS. Dette understreker viktigheten og nødvendigheten av at det overordnede ansvar for utredning og diagnostisering må ligge hos behandlende søvnlegespesialist. Når søvnlegen etter utredning finner at pasienten vil være tjent med en søvnapnéskinne, er henvisning til tannlege med spesialkompetanse neste skritt.
Rent praktisk vil nok en samlokalisering av behandlende søvnleger og -tannleger i større, spesialiserte sykehusenheter representere den behandlingsmessig gunstigste samarbeidsorganisering. Pasienten kan da raskere og enklere utredes, behandles og etterkontrolleres på ett og samme sted (44).
Oppfølging og etterkontroll
Tannlegen som fremstiller skinnen, skal etterkontrollere pasienten. Skinnen justeres til subjektive symptomer opphører. Det anbefales 2 - 4 ukers kontroller innledningsvis. Når optimalt protrusjonsleie er funnet og optimal skinneeffekt oppnås, bør tannlegen deretter kalle inn pasienten hver 6. måned det første året, og videre til årlige kontroller (33). Hensikten med etterkontrollene er å evaluere skinnens fortsatte effekt samt å kartlegge pasientens tilfredshet og symptombilde. I tillegg kontrolleres okklusjon, bløtvevsstrukturer og pasientens egenoppfølging, herunder vedlikehold av skinnen. Optimalt renhold av skinnen viser seg ofte å være utfordrende for mange pasienter som gjerne kan presentere seg med skinne full av belegg og misfarging etter lang tids bruk (figur 1 A). Det er selvsagt også tannlegens oppgave å kontrollere for eventuelle materialtekniske komplikasjoner ved den enkelte skinnen og, hvis nødvendig, utbedre disse.
Selve søvnbehandlingen er søvnlegens ansvar, og pasienter som behandles med søvnapnéskinner hos tannlege, bør minst én gang tilbake til søvnlegen for en objektiv søvntest og vurdering av skinnens effekt. Ved disse kontrollene vurderes pasientens OSAS-symptomer, og ny søvnregistrering bør utføres dersom pasienten rapporterer symptomforverring eller liten eller ingen forandring i symptombildet. For å sikre tilfredsstillende terapeutisk nytte av skinnen, utføres revurdering av søvnparametre med skinnen på plass i munnen. Spesielt er dette viktig hos pasienter med moderat til alvorlig OSAS. I denne gruppen kan noen pasienter oppleve en viss symptomforbedring uten adekvat AHI-reduksjon (45).
Ved suboptimal AHI bør pasienten ideelt sett henvises tilbake til samarbeidende tannlege for ytterligere justeringer av skinnen og deretter ny søvntest. Dette krever et godt og tett samarbeid mellom tannlege og søvnspesialist. Dette er opplagt ressurskrevende og kan være vanskelig å gjennomføre av kapasitetsgrunner.
Studier har vist at kun 55 % av pasienter som subjektivt sett er fornøyd med skinnebehandling, faktisk får full terapeutisk effekt (4, 46). 27 - 32 % får først optimal effekt etter ny somnografi og titrering. Den subjektive bedringen er muligens forårsaket av placebo. Alle pasienter bør derfor evalueres objektivt (9).
Bivirkninger
Søvnapnéskinner protruderer mandibelen og utsetter dermed tenner og kjever for resiproke krefter. Innledningsvis kan pasienten oppleve ømhet i tenner, sårt tannkjøtt, økt salivasjon eller xerostomi (4, 19). Smerte i tyggemuskulatur og kjeveledd er også vanlig i den initiale fasen (47). Mange pasienter opplever dessuten en forbigående bittforandring når skinnen fjernes om morgenen (48). Mer sjeldent kan skinnebehandling utløse brekningsrefleks, forårsake fraktur av fyllinger og tenner, og medføre periodontal skade (47, 49). Bivirkningsinsidensen varierer signifikant mellom forskjellige studier.
Noe smerter i kjevemuskulatur og -ledd er relativt vanlig den første tiden etter påbegynt skinnebruk, men er i de aller fleste tilfeller forbigående og representerer sjelden noe stort problem (50).
Det har lenge blitt antatt at pasienter med på forhånd eksisterende TMD-problemer vil kunne oppleve en forverring av tilstanden ved bruk av mandibelprotruderende skinne, og derfor bør avstå fra slik behandling inntil TMD-symptomene er tilfredsstillende behandlet på konvensjonelt vis. Men flere studier er nylig publisert der TMD symptomer til tross for svak initial økning allikevel synes å avta etter en tids bruk av søvnapnéskinne (20, 51, 52). Økt tendens til bruksisme er påvist, men er en sjelden bivirkning (20).
Permanente bittendringer er ofte rapportert (53). Det er vist at vertikale og horisontale overbitt kan reduseres, og hos pasienter som ved behandlingsstart har store horisontale eller vertikale overbitt, kan en dermed av og til se bittendring i gunstig retning, dvs reduksjon av bittanomaliene (54), men også erfare kryssbittutvikling og nedgang i antall okklusale kontaktpunkter (55) samt uønsket lateral åpning av bittet (52). Bittforandringer kan for øvrig også forekomme ved behandling med CPAP (56). Økning av ansiktshøyden og pasientens gapeevne samt endring i fronttennenes inklinasjon kan forekomme (47, 49). Disse endringene har sammenheng med hvor lenge skinnen har vært i bruk (54, 57). Behandling med skinne bør likevel fortsette selv ved observerte bittendringer fordi de medisinske konsekvensene ved ubehandlet OSAS ansees å være langt mer alvorlige (57).
I en evidensbasert oversiktsartikkel oppsummeres bivirkninger og komplikasjoner ved skinnebehandling fra 38 publiserte studier (totalt over 1700 pasienter) der det konkluderes med at mindre alvorlige bivirkninger er svært vanlig og at mer alvorlige bivirkninger forekommer langt sjeldnere (33).
Refusjonsordninger
Et vesentlig moment i tillegg til det rent medisinske er at Helsedirektoratet f.o.m. 2012 har slått fast at alle utgifter forbundet med skinnebehandling av søvnapnésyndrom i spesialisthelsetjenesten, skal dekkes av spesialisthelsetjenesten (lov om spesialisthelsetjenester, § 2 - 1a). Det vil i praksis si at pasienten kan få dekket alle kostnader i forbindelse med skinnebehandling hos tannlegen forutsatt positivt vedtak om dekning fra Behandlingshjelpemiddel-enheten ved det aktuelle regionale helseforetak. De enkelte helseforetakene kan selv velge praksis med hensyn til saksgang og gjennomføring, men det er normalt et krav at søknad om økonomisk støtte skal være underskrevet av den legespesialisten som har utredet pasienten. Legespesialisten må dessuten enten være ansatt i et av de offentlige helseforetakene eller i privat sykehus eller spesialistpraksis som har avtale med et regionalt helseforetak om utredning/behandling av pasienter med søvnforstyrrelser. Hvorvidt pasienter med beskjeden søvnforstyrrelse (det vil si har relativt lav AHI og/eller kun et «sosialt» snorkeproblem) bør få innvilget støtte, er et politisk/økonomisk spørsmål. Det kan også diskuteres om pasienter med velfungerende CPAP skal få innvilget søvnapnéskinne i tillegg. Praksis til nå har nok vært at de to sistnevnte pasientkategorier ikke har fått støtte.
Det må tillegges at gjeldende refusjonspraksis ikke åpner for støtte til eventuell nødvendig dental forbehandling som derfor må bekostes av pasienten selv. Videre vil det alltid måtte være opp til tannlegen å avgjøre om pasientens tannstatus er egnet for behandling med søvnapnéskinne eller ikke.
Bemerk at ansvaret for å vurdere tannlegens kompetanse på dette området for tiden ligger hos legespesialisten, og dette kan representere en utfordring ettersom det ikke gis formell utdanning i dental søvnmedisin i Norge. Til nå har den begrensede informasjonstilgangen hovedsakelig kommet via enkelte store skinneprodusenters egne tilrettelagte kursopplegg for tannleger. Utover dette har en del interesserte kolleger via internasjonale særorganisasjoner som for eksempel American Academy of Dental Sleep Medicine (AADSM) og European Academy of Dental Sleep Medicine (EADSM) kunnet fremstille seg til akkrediteringseksamen, og slik oppnådd disse organisasjonenes sertifisering. Det er åpenbart et behov for klarere kvalifikasjonskriterier innenfor fagfeltet dental søvnmedisin i Norge.
Konklusjon
Tannleger bør kunne identifisere de vanligste symptomene ved OSAS, og ved mistanke henvise til fastlege for søvnmedisinsk utredning. Tverrfaglig samarbeid mellom leger og tannleger er viktig for å sikre optimal behandling av pasienter med obstruktivt søvnapnésyndrom. Leger og tannleger bør informeres om at søvnapnéskinne er et evidensbasert og effektivt hjelpemiddel. Tannleger som tilbyr behandling til OSAS-pasienter, bør ha grunnleggende kunnskap om søvnmedisin i tillegg til rent tekniske fremstillingsferdigheter.
English summary
Khan S, Saxegaard E.
Obstructive sleep apnea syndrome - how can the dentist contribute to the treatment?
784-92
Over the past decades the interest among dental professionals world wide to treat patients with sleep related breathing disorders, in particular obstructive sleep apnea syndrome, has increased markedly. The total number of mandibular advancement splints fitted to patients has indeed increased even in Norway during the past 7 - 8 years. The clinical experience and level of knowledge among Norwegian dentists is, however, in general still modest. The purpose of this review was to provide an update on the issue of OSAS in general for Norwegian dentists, including pathophysiology, diagnosis, alternative treatment modalities, recommended treatment protocol, oral appliance design, mode of action and possible side effects. Thereby also providing an understanding of how the dentist can participate in the treatment of the OSAS-patient in close collaboration with specialist sleep physicians. Established routines for available financial support for patients in the Norwegian health system as of today are also outlined.
Referanser
Ferguson KA, Love LL, Ryan CF. Effect of mandibular and tongue protrusion on upper airway size during wakefulness. Am J Respir Crit Care Med. 1997; 155(5): 1748 - 54.
Aarab G, Lobbezoo F, Heymans MW, Hamburger HL, Naeije M. Long-term follow-up of a randomized controlled trial of oral appliance therapy in obstructive sleep apnea. Respiration. 2011; 82(2): 162 - 8.
Gotsopoulos H, Chen C, Qian J, Cistulli PA. Oral appliance therapy improves symptoms in obstructive sleep apnea: a randomized, controlled trial. Am J Respir Crit Care Med. 2002; 166(5): 743 - 8.
Mehta A, Qian J, Petocz P, Darendeliler MA, Cistulli PA. A randomized, controlled study of a mandibular advancement splint for obstructive sleep apnea. Am J Respir Crit Care Med. 2001; 163(6): 1457 - 61.
Lim J, Lasserson TJ, Fleetham J, Wright J. Oral appliances for obstructive sleep apnoea. The Cochrane database of systematic reviews. 2006(1): Cd004435.
Johansson A, Fondenes O. Snarkskena vid obstruktiv sömnapné och snarkning. Nor Tannlegeforen Tid. 2007; 117(10): 604 - 7.
The Swedish Council on Technology assessment in Health Care (SBU). Obstructive Sleep Apnea Syndrome: A systematic literature review. 2007.
Kahn S, Skau I, Grytten J, Saxegaard E. Obstruktivt søvnapnésyndrom - kunnskap og klinisk erfaring blant et utvalg norske tannleger. Nor Tannlegeforen Tid. 2015; 125: 794-8.
Hrubos-Strom H, Randby A, Namtvedt SK, Kristiansen HA, Einvik G, Benth J, et al. A Norwegian population-based study on the risk and prevalence of obstructive sleep apnea. The Akershus Sleep Apnea Project (ASAP). J Sleep Res. 2011; 20(1 Pt 2): 162 - 70.
Cartwright RD, Diaz F, Lloyd S. The effects of sleep posture and sleep stage on apnea frequency. Sleep. 1991; 14(4): 351 - 3.
Gislason T, Almqvist M, Eriksson G, Taube A, Boman G. Prevalence of sleep apnea syndrome among Swedish men - an epidemiological study. J Clin Epidemiol. 1988; 41(6): 571 - 6.
American Academy of Sleep Medicine. International Classification of Sleep Disorders: Diagnostic and Coding Manual. 2nd ed. Westchester, IL: American Academy of Sleep Medicine; 2005.
Young T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleep-disordered breathing among middle-aged adults. N Engl J Med. 1993; 328(17): 1230 - 5.
Bixler EO, Vgontzas AN, Ten Have T, Tyson K, Kales A. Effects of age on sleep apnea in men: I. Prevalence and severity. Am J Respir Crit Care Med. 1998; 157(1): 144 - 8.
Duran J, Esnaola S, Rubio R, Iztueta A. Obstructive sleep apnea-hypopnea and related clinical features in a population-based sample of subjects aged 30 to 70 yr. Am J Respir Crit Care Med. 2001; 163(3 Pt 1): 685 - 9.
Chesson AL, Jr., Berry RB, Pack A. Practice parameters for the use of portable monitoring devices in the investigation of suspected obstructive sleep apnea in adults. Sleep. 2003; 26(7): 907 - 13.
Franklin KA, Anttila H, Axelsson S, Gislason T, Maasilta P, Myhre KI, et al. Effects and side-effects of surgery for snoring and obstructive sleep apnea - a systematic review. Sleep. 2009; 32(1): 27 - 36.
Barnes M, McEvoy RD, Banks S, Tarquinio N, Murray CG, Vowles N, et al. Efficacy of positive airway pressure and oral appliance in mild to moderate obstructive sleep apnea. Am J Respir Crit Care Med. 2004; 170(6): 656 - 64.
Ferguson KA, Ono T, Lowe AA, Keenan SP, Fleetham JA. A randomized crossover study of an oral appliance vs nasal-continuous positive airway pressure in the treatment of mild-moderate obstructive sleep apnea. Chest. 1996; 109(5): 1269 - 75.
Hoekema A, Stegenga B, De Bont LG. Efficacy and co-morbidity of oral appliances in the treatment of obstructive sleep apnea-hypopnea: a systematic review. Crit Rev Oral Biol Med. 2004; 15(3): 137 - 55.
Phillips CL, Grunstein RR, Darendeliler MA, Mihailidou AS, Srinivasan VK, Yee BJ, et al. Health outcomes of continuous positive airway pressure versus oral appliance treatment for obstructive sleep apnea: a randomized controlled trial. Am J Respir Crit Care Med. 2013; 187(8): 879 - 87.
Gagnadoux F, Fleury B, Vielle B, Petelle B, Meslier N, N'Guyen XL, et al. Titrated mandibular advancement versus positive airway pressure for sleep apnoea. Eur Respir J. 2009; 34(4): 914 - 20.
Borel JC, Gakwaya S, Masse JF, Melo-Silva CA, Series F. Impact of CPAP interface and mandibular advancement device on upper airway mechanical properties assessed with phrenic nerve stimulation in sleep apnea patients. Respir Physiol Neurobiol. 2012; 183(2): 170 - 6.
Dieltjens M, Braem MJ, Van de Heyning PH, Wouters K, Vanderveken OM. Prevalence and clinical significance of supine-dependent obstructive sleep apnea in patients using oral appliance therapy. J Clin Sleep Med. 2014; 10(9): 959 - 64.
Johns MW. A new method for measuring daytime sleepiness: the Epworth sleepiness scale. Sleep. 1991; 14(6): 540 - 5.
Banhiran W, Assanasen P, Nopmaneejumruslers C, Metheetrairut C. Epworth sleepiness scale in obstructive sleep disordered breathing: the reliability and validity of the Thai version. Sleep & breathing = Schlaf & Atmung. 2011; 15(3): 571 - 7.
Beiske KK, Kjelsberg FN, Ruud EA, Stavem K. Reliability and validity of a Norwegian version of the Epworth sleepiness scale. Sleep & breathing = Schlaf & Atmung. 2009; 13(1): 65 - 72.
Chan AS, Sutherland K, Schwab RJ, Zeng B, Petocz P, Lee RW, et al. The effect of mandibular advancement on upper airway structure in obstructive sleep apnoea. Thorax. 2010; 65(8): 726 - 32.
Gauthier L, Laberge L, Beaudry M, Laforte M, Rompre PH, Lavigne GJ. Efficacy of two mandibular advancement appliances in the management of snoring and mild-moderate sleep apnea: a cross-over randomized study. Sleep Med. 2009; 10(3): 329 - 36.
Pitsis AJ, Darendeliler MA, Gotsopoulos H, Petocz P, Cistulli PA. Effect of vertical dimension on efficacy of oral appliance therapy in obstructive sleep apnea. Am J Respir Crit Care Med. 2002; 166(6): 860 - 4.
Vanderveken OM, Devolder A, Marklund M, Boudewyns AN, Braem MJ, Okkerse W, et al. Comparison of a custom-made and a thermoplastic oral appliance for the treatment of mild sleep apnea. Am J Respir Crit Care Med. 2008; 178(2): 197 - 202.
Deane SA, Cistulli PA, Ng AT, Zeng B, Petocz P, Darendeliler MA. Comparison of mandibular advancement splint and tongue stabilizing device in obstructive sleep apnea: a randomized controlled trial. Sleep. 2009; 32(5): 648 - 53.
Ferguson KA, Cartwright R, Rogers R, Schmidt-Nowara W. Oral appliances for snoring and obstructive sleep apnea: a review. Sleep. 2006; 29(2): 244 - 62.
Aarab G, Lobbezoo F, Hamburger HL, Naeije M. Effects of an oral appliance with different mandibular protrusion positions at a constant vertical dimension on obstructive sleep apnea. Clin Oral Investig. 2010; 14(3): 339 - 45.
Walker-Engstrom ML, Ringqvist I, Vestling O, Wilhelmsson B, Tegelberg A. A prospective randomized study comparing two different degrees of mandibular advancement with a dental appliance in treatment of severe obstructive sleep apnea. Sleep & breathing = Schlaf & Atmung. 2003; 7(3): 119 - 30.
Blanco J, Zamarron C, Abeleira Pazos MT, Lamela C, Suarez Quintanilla D. Prospective evaluation of an oral appliance in the treatment of obstructive sleep apnea syndrome. Sleep & breathing = Schlaf & Atmung. 2005; 9(1): 20 - 5.
Johnston CD, Gleadhill IC, Cinnamond MJ, Gabbey J, Burden DJ. Mandibular advancement appliances and obstructive sleep apnoea: a randomized clinical trial. Eur J Orthod. 2002; 24(3): 251 - 62.
Vroegop AV, Vanderveken OM, Van de Heyning PH, Braem MJ. Effects of vertical opening on pharyngeal dimensions in patients with obstructive sleep apnoea. Sleep Med. 2012; 13(3): 314 - 6.
Meurice JC, Marc I, Carrier G, Series F. Effects of mouth opening on upper airway collapsibility in normal sleeping subjects. Am J Respir Crit Care Med. 1996; 153(1): 255 - 9.
Barsh LI. Dentistry's role in the recognition and treatment of sleep-breathing disorders: the need for cooperation with the medical community. J Calif Dent Assoc. 1998; 26(8): 591 - 8.
Barsh LI, Schmidt-Nowara W. Collaborative Care. Sleep & breathing = Schlaf & Atmung. 2000; 4(2): 51 - 2.
Gauthier L, Almeida F, Arcache JP, Ashton-McGregor C, Cote D, Driver HS, et al. Position paper by Canadian dental sleep medicine professionals on the role of different health care professionals in managing obstructive sleep apnea and snoring with oral appliances. Can Respir J. 2012; 19(5): 307 - 9.
Schwarting S, Huebers U, Heise M, Schlieper J, Hauschild A. Position paper on the use of mandibular advancement devices in adults with sleep-related breathing disorders. A position paper of the German Society of Dental Sleep Medicine (Deutsche Gesellschaft Zahnaerztliche Schlafmedizin, DGZS). Sleep & breathing = Schlaf & Atmung. 2007; 11(2): 125 - 6.
Johansson A, Gjerde K, Lehmann S, Bjorvatn B, Al-azawy K, Gulati S, et al. Skinnebehandling mot søvnapne. Tidsskr Nor Legeforen. 2014; 134: 1030 - 1.
Schmidt-Nowara W, Lowe A, Wiegand L, Cartwright R, Perez-Guerra F, Menn S. Oral appliances for the treatment of snoring and obstructive sleep apnea: a review. Sleep. 1995; 18(6): 501 - 10.
Krishnan V, Collop NA, Scherr SC. An evaluation of a titration strategy for prescription of oral appliances for obstructive sleep apnea. Chest. 2008; 133(5): 1135 - 41.
Pantin CC, Hillman DR, Tennant M. Dental side effects of an oral device to treat snoring and obstructive sleep apnea. Sleep. 1999; 22(2): 237 - 40.
Lindman R, Bondemark L. A review of oral devices in the treatment of habitual snoring and obstructive sleep apnoea. Swed Dent J. 2001; 25(1): 39 - 51.
Rose E, Staats R, Virchow C, Jonas IE. A comparative study of two mandibular advancement appliances for the treatment of obstructive sleep apnoea. Eur J Orthod. 2002; 24(2): 191 - 8.
Doff MH, Veldhuis SK, Hoekema A, Slater JJ, Wijkstra PJ, de Bont LG, et al. Long-term oral appliance therapy in obstructive sleep apnea syndrome: a controlled study on temporomandibular side effects. Clin Oral Investig. 2012; 16(3): 689 - 97.
Giannasi LC, Almeida FR, Magini M, Costa MS, de Oliveira CS, de Oliveira JC, et al. Systematic assessment of the impact of oral appliance therapy on the temporomandibular joint during treatment of obstructive sleep apnea: long-term evaluation. Sleep & breathing = Schlaf & Atmung. 2009; 13(4): 375 - 81.
Perez CV, de Leeuw R, Okeson JP, Carlson CR, Li HF, Bush HM, et al. The incidence and prevalence of temporomandibular disorders and posterior open bite in patients receiving mandibular advancement device therapy for obstructive sleep apnea. Sleep & breathing = Schlaf & Atmung. 2013; 17(1): 323 - 32.
Rose EC, Schnegelsberg C, Staats R, Jonas IE. Occlusal side effects caused by a mandibular advancement appliance in patients with obstructive sleep apnea. Angle Orthod. 2001; 71(6): 452 - 60.
Almeida FR, Lowe AA, Sung JO, Tsuiki S, Otsuka R. Long-term sequellae of oral appliance therapy in obstructive sleep apnea patients: Part 1. Cephalometric analysis. Am J Orthod Dentofacial Orthop. 2006; 129(2): 195 - 204.
Doff MH, Finnema KJ, Hoekema A, Wijkstra PJ, de Bont LG, Stegenga B. Long-term oral appliance therapy in obstructive sleep apnea syndrome: a controlled study on dental side effects. Clin Oral Investig. 2013; 17(2): 475 - 82.
Tsuda H, Almeida FR, Tsuda T, Moritsuchi Y, Lowe AA. Craniofacial changes after 2 years of nasal continuous positive airway pressure use in patients with obstructive sleep apnea. Chest. 2010; 138(4): 870 - 4.
Almeida FR, Lowe AA, Otsuka R, Fastlicht S, Farbood M, Tsuiki S. Long-term sequellae of oral appliance therapy in obstructive sleep apnea patients: Part 2. Study-model analysis. Am J Orthod Dentofacial Orthop. 2006; 129(2): 205 - 13.
Adresse: Erik Saxegaard, Avdeling for protetikk og bittfunksjon, Det odontologiske fakultet, Universitetet i Oslo, postboks 1109 Blindern, 0317 Oslo. E-post: erik.saxegaard@odont.uio.no
Artikkelen har gjennomgått ekstern faglig vurdering.
Khan S, Saxegaard E. Obstruktivt søvnapnésyndrom - hvordan kan tannlegen bidra i behandlingen? Nor Tannlegeforen Tid. 2015; 125: 784-92.
spesialist i oral protetikk. Avdeling for protetikk og bittfunksjon, Det odontologiske fakultet, Universitetet i Oslo
førsteamanuensis, dr.odont. Avdeling for protetikk og bittfunksjon, Det odontologiske fakultet, Universitetet i Oslo