Palle Holmstrup, Dagmar Bunæs, Mervi Gürsoy og Pernilla Lundberg
Den nye klassifikation af parodontitis
Professor, dr.odont., odont.dr. (h.c.). ph.d., Odontologisk Institut, Det Sundhedsvidenskabelige Fakultet, Københavns Universitet
Førsteamanuensis, ph.d., Department of Clinical Dentistry, Faculty of Medicine, University of Bergen, Bergen, Norge
Docent. ph.d., Department of Periodontology, Institute of Dentistry, University of Turku, Turku, Finland
Professor, overtandlæge, odont.dr., Section of Molecular Periodontology, Department of Odontology, Umeå University, Umeå, Sverige
Klinisk relevans
Det er indlysende, at en korrekt diagnose er en forudsætning for optimal behandling. Sammenlignet med tidligere klassifikationer rummer den nye parodontitisklassifikation en mere præcis beskrivelse af de forandringer, der sker i parodontiet. Klassifikationen er baseret på den nyeste viden, og den anvendes i de førende videnskabelige tidsskrifter og lærebøger såvel som ved præ- og postgraduat undervisning i parodontologi. Det er derfor vigtigt, at tandlæger i de nordiske lande er fortrolige med den nye klassifikation og anvender den i deres daglige arbejde.
Klassifikationen af parodontale sygdomme er blevet reorganiseret efter et omfattende arbejde i ekspertgrupper efterfulgt af en international workshop arrangeret af American Academy of Periodontology og European Federation of Periodontology i 2017. På workshoppen enedes et internationalt ekspertpanel med repræsentanter fra lande over hele verden om definitionerne, som ud over en beskrivelse af parodontitis også indeholdt beskrivelser af det intakte parodontium, parodontal sundhed, biofilminduceret gingivitis og ikke-biofilminduceret gingival sygdom. Denne artikel fokusererpåparodontitis.
Parodontitis er en tilstand med klinisk fæstetab (clinical attachment loss, CAL) på mindst 1 mm interdentalt på mindst to tænder, som ikke er nabotænder, eller CAL på mindst 3 mm facialt/lingvalt på mindst to tænder. Parodontitis inddeles yderligere i fire stadier (I-IV) efter sygdommens alvorlighed og i tre grader (A, B, C) efter progressionshastighed og risikofaktorer. Endvidere skal sygdommens udbredelse og fordeling i tandsættet angives.
Vi beskriver her, hvordan den nye parodontitisklassifikation kan anvendes i daglig klinisk praksis, og hvordan implementering af den nye klassifikation kan gavne patienter og klinikere og give et bud på, hvor stort problemet er, dvs. prævalensen af fremskreden parodontitis. Artiklen illustrerer endvidere de nye begreber, stadier og grader ved hjælp af repræsentative patienttilfælde.
Det er indlysende, at en korrekt diagnose er en forudsætning for optimal behandling. Dette indebærer, at en diagnose til enhver tid må baseres på en sygdomsklassifikation, der hviler på relevant viden fra den tilgængelige videnskabelige litteratur. En konsekvens af den løbende udvikling i vores videnskabeligt underbyggede viden er, at sygdomsklassifikationer fra tid til anden må opdateres. Den nye klassifikation af parodontale sygdomme er tidligere blevet gennemgået i de nordiske tandlægeforeningers medlemsblade (1–3), og denne artikel ligger i forlængelse af disse beskrivelser.
Klassifikationen blev debatteret og vedtaget på World Workshop on Classification of Periodontal and Peri-Implant Diseases and Conditions (WWCP), der blev afholdt i Chicago i november 2017 og var organiseret af American Academy of Periodontology og European Federation of Periodontology. Fire arbejdsgrupper med diverse undergrupper havde til mødet udarbejdet en række oversigtsartikler, som parodontologer fra hele verden på selve mødet diskuterede, hvorefter man enedes om den nye klassifikation (4–26). De nordiske lande var repræsenteret af to svenskere og en dansker. Den nye klassifikation danner grundlag for den aktuelle finske retningslinje for parodontalbehandling (27).
Formålet med denne artikel er at præsentere en kort oversigt over den nye parodontitisklassifikation (28) og ved hjælp af repræsentative patienttilfælde at illustrere og diskutere, hvordan den kan indpasses i daglig klinisk praksis, hvordan patienter og fagpersoner kan have gavn af klassifikationen, og hvordan den påvirker prævalensen af parodontale sygdomme.
Klassifikationen indeholder definitioner på parodontal sundhed, et intakt parodontium, biofilminduceret gingivitis, ikke-biofilminduceret gingival sygdom, parodontitis og peri-implantære sygdomme. For sidstnævnte henvises til artikel 4 i dette tema. Nærværende artikel fokuserer på parodontitis.
Parodontitis
Formålet med klassifikationssystemet er at lette identifikation, behandling og forebyggelse af parodontitis hos den enkelte patient. Den diagnostiske proces har tre trin:
Identifikation af personen som en parodontitispatient
Identifikation af patientens overordnede parodontitisdiagnose
Detaljeret beskrivelse af patientens sygdomsbillede
Når man skal arbejde med diagnosen parodontitis, er det naturligvis vigtigt at forstå begrebet parodontal sundhed, der defineres som en tilstand uden inflammatorisk parodontal sygdom og indebærer normal funktion uden mentale eller fysiske følger af nuværende eller tidligere sygdom (5). Ifølge den nye klassifikation kan parodontal sundhed forekomme hos:
En parodontitisfri person med et intakt parodontium
En stabil parodontitispatient med et reduceret parodontium efter vellykket parodontalbehandling
En patient, der har tandbørsteinduceret gingival retraktion eller har fået foretaget klinisk kroneforlængelse.
I forbindelse med den kliniske undersøgelse af patienten er det vigtigt at bemærke, at der selv ved parodontal sundhed på grund af måleusikkerhed kan være enkelte steder, der bløder lidt under pochemåling.
I klinikken vil kombinationen af parodontal sundhed og et intakt parodontium være karakteristisk for en person uden tegn på gingivitis (tabel 1). Det er vigtigt at skelne mellem en patient med gingival sundhed og et reduceret, men stabilt parodontium efter parodontalbehandling og en patient med gingival sundhed og et reduceret parodontium som følge af tandbørsteinduceret gingival retraktion eller kirurgisk kroneforlængelse (ikke parodontitisrelateret), da der er forskel på risikoen for sygdomsprogression i de to tilfælde.
Intakt parodontium |
Sund |
Gingivitis |
|---|---|---|
CAL |
Nej |
Nej |
Pochedybde (ingen pseudopocher) |
≤3 mm |
≤3 mm |
BoP |
<10% |
Ja (≥ 10 %) |
Knogletab på røntgenoptagelse |
Nej |
Nej |
|
Reduceret parodontium Patient uden parodontitis |
Sund |
Gingivitis |
CAL |
Ja |
Ja |
Pochedybde (ingen pseudopocher) |
≤3 mm |
≤3 mm |
BoP |
<10% |
Ja (≥10%) |
Knogletab på røntgenoptagelse |
Eventuelt |
Eventuelt |
Stabil parodontitispatient efter vellykket behandling |
Sund |
Gingivitis hos en patient med tidligere parodontitis |
CAL |
Ja |
Ja |
Pochedybde (ingen pseudopocher) |
≤ 4 mm (ingen steder ≥ 4 mm med BoP)b |
≤ 3 mma |
BoP |
<10% |
Ja (≥10%) |
Knogletab på røntgenoptagelse |
Ja |
Ja |
a Selv efter vellykket parodontalbehandling vil der ved lokaliseret blødning (BoP) stadig være betydelig risiko for recidiv af parodontitis med CAL ved disse steder. Derfor defineres gingivitis som forekomst af BoP på steder med pochedybde ≤ 3 mm (ligesom ved definitionen på gingival sundhed) i stedet for ≤ 4 mm.
b På workshoppen var der et mindretal, der mente, at tærskelværdien for definitionen på sundhed hos en parodontitispatient efter vellykket behandling skulle være pochedybde ≤ 3 mm uden BoP, idet der ellers var forøget risiko for recidiv af parodontitis. Flertallet argumenterede imidlertid for, at pochedybde på ≤ 3 mm sjældent opnås overalt i et tandsæt efter parodontalbehandling, og at dette kunne føre til overbehandling, da tænder med pochedybder >3 mm uden BoP ikke kunne klassificeres som sunde og dermed var kandidater til fortsat aktiv behandling i stedet for kontrol og støttebehandling. Tærskelværdien blev derfor sat til ≤ 4 mm, fordi det kliniske billede skal bedømmes anderledes hos en tidligere parodontitispatient end hos en patient, der aldrig har haft parodontitis.
Identifikation af en parodontitispatient
Parodontitis er en inflammatorisk tilstand. Sygdommen diagnosticeres primært gennem registrering af klinisk fæstetab (clinical attachment loss, CAL).
En person defineres som en parodontitispatient, hvis der er et CAL på mindst 1 mm på mindst to tænder, der ikke er nabotænder, eller hvis der er et CAL på ≥ 3 mm og pochedybde (PD) ≤ 4 mm facialt eller lingvalt på mindst to tænder (som gerne må være nabotænder). Det forudsættes, at fæstetabet skyldes parodontitis og ikke andre forhold som fx caries, traumatisk retraktion, afløb fra endodontisk læsion, rodfraktur eller komplikationer i forbindelse med visdomstænder.
Identifikation af den overordnede diagnose
Klassifikationen indebærer et fuldstændigt brud med tidligere anvendte parodontitisdiagnoser, idet der nu kun opereres med tre typer af parodontitis:
Nekrotiserende parodontitis med de velkendte karakteristika: smerte, ulcerationer, fibrindækkede nekroser af papiltoppe og undertiden blotlæggelse af marginalt knoglevæv.
Parodontitis som en direkte manifestation af systemiske sygdomme som fx Downs syndrom, Papillon-Lefévres syndrom og cyklisk neutropeni.
Parodontitis
Da de to førstnævnte tilstande er ekstremt sjældne, vil næsten alle parodontitispatienter få den overordnede diagnose parodontitis.
Detaljeret beskrivelse af patientens sygdomsbillede
Stadier
Efter en grundig undersøgelse defineres sygdomsstadiet (I-IV) ud fra sygdommens alvorlighed og kompleksitet (Tabel 2), og derefter bestemmes sygdommens udbredelse i tandsættet.
Stadium I
Ved Stadium I har tandsættets værst afficerede tand et CAL på 1–2 mm. På røntgenoptagelse udgør knogletabet < 15 % af rodens længde, og svindet er overvejende horisontalt. PD er ≤ 4 mm, og patienten har ikke mistet tænder på grund af parodontitis.
Stadium II
Ved Stadium II har den værst afficerede tand et CAL på 3–4 mm. På røntgenoptagelse udgør knogletabet 15–33 % af rodens længde, og knoglesvindet er overvejende horisontalt. PD er ≤ 5 mm, og patienten har ikke mistet tænder på grund af parodontitis.
Stadium III
Ved Stadium III har den værst afficerede tand et CAL på ≥ 5 mm. På røntgenoptagelse har knogletabet bredt sig til den midterste eller mest apikale tredjedel af rodens længde, og der ses vertikalt knoglesvind på ≥ 3 mm. Der kan være PD ≥ 6 mm, furkaturinvolvering af klasse II eller III samt moderat svind af processus alveolaris. Patienten kan have mistet op til fire tænder på grund af parodontitis.
Stadium IV
Ved Stadium IV har den værst afficerede tand et CAL på ≥ 5 mm. På røntgenoptagelse har knogletabet bredt sig til den midterste eller mest apikale tredjedel af rodens længde, og der ses vertikalt knoglesvind på ≥ 3 mm. Der kan være PD ≥ 6 mm, furkaturinvolvering af klasse II eller III samt moderat svind af processus alveolaris. Endvidere kan patienten have mistet mindst fem tænder på grund af parodontitis, og der kan være behov for kompleks rehabilitering som følge af mastikatorisk dysfunktion, ligesom der kan forekomme traumatisk okklusion med mobilitet af 2. eller 3. grad og bidkollaps med mindre end 10 okkluderende tandpar.
Stadium I (initial) |
Stadium II (moderat) |
Stadium III (alvorlig) |
Stadium IV (fremskreden) |
|
|---|---|---|---|---|
CAL approksimalt på den værst afficerede tand |
1–2 mm |
3–4 mm |
≥ 5 mm |
≥ 5 mm |
Radiologisk bedømt knogletab |
Koronale tredjedel af roden (< 15 %) |
Koronale tredjedel af roden (15–33 %) |
Midterste eller apikale tredjedel af roden |
Midterste eller apikale tredjedel af roden |
Mistede tænder |
Ingen tænder mistet på grund af parodontitis |
Ingen tænder mistet på grund af parodontitis |
1–4 tænder mistet på grund af parodontitis |
≥ 5 tænder mistet på grund af parodontitis |
Sygdommens kompleksitet |
Pochedybder ≤ 4 mm Overvejende horisontalt knogletab |
Pochedybder ≤ 5 mm Overvejende horisontalt knogletab |
Pochedybder ≥ 6 mm Vertikalt knogletab ≥ 3 mm Furkaturinvolvering Klasse II eller III Moderat svind af processus alveolaris |
Kompleksitet som ved Stadium III Desuden behov for omfattende rehabilitering som følge af: Mastikatorisk dysfunktion Traumatisk okklusion (løsningsgrad 2–3) Omfattende svind af processus alveolaris Bidkollaps Resttandsæt på mindre end 20 tænder (10 okkluderende tandpar) |
Hvad gør man, hvis patienten ikke passer ind i nogen af stadierne?
Patienter behøver ikke opfylde alle kriterier for at kunne indplaceres i et bestemt stadium. I udgangspunktet er en enkelt komplicerende faktor nok til, at patienten rykker op i et højere stadium. En patient med furkaturinvolvering som følge af lav rodsokkel bør derfor karakteriseres som Stadium III, selv om CAL er < 5 mm. Tilsvarende kan en patient indpasses i Stadium IV, hvis der fx er mindre end 10 okkluderende tandpar, men hverken mastikatorisk dysfunktion eller traumatisk okklusion.
Bedømmelse af sygdommens udbredelse i tandsættet
Efter indplacering i stadium vurderes, hvordan sygdommen er fordelt i tandsættet:
Lokaliseret: < 30 % af tænderne er afficerede i det definerede stadium
Generaliseret: ≥ 30 % af tænderne er afficerede i det definerede stadium
Molar-/incisiv-mønster: sygdommen findes kun på incisiver og molarer.
Gradinddeling
Gradinddelingen er et udtryk for, om tilstanden kan forventes at progrediere hurtigere end normalt eller respondere dårligere end normalt på behandling. WWCP‘s kriterier for gradinddeling præsenteres i Tabel 3. Som udgangspunkt placeres patienter i Grad B (moderat progressionshastighed); men anamnestiske oplysninger, kliniske fund og radiologiske fund kan føre til, at patienten enten opgraderes til Grad C eller nedgraderes til Grad A.
Grad A (langsom progression)
Hvis kliniske eller radiologiske data viser, at der ikke er sket noget fæstetab i løbet af de seneste fem år, kan patienten nedgraderes til Grad A. Hvis sådanne data ikke er tilgængelige, kan man anvende indicier som fx beskedent CAL på trods af store mængder biofilm. Et mere præcist indirekte mål for progressionshastigheden opnås ved at dividere knogletabet (i pct. af rodlængden) med patientens alder. Den oprindelige tærskelværdi (Grad A; < 0,25) er blevet modificeret af The British Society of Periodontology (29) med to begrundelser: udregningen skal være nem og ukompliceret for klinikeren, og den gradinddeling, beregningen munder ud i, må nødvendigvis afspejle spektret for parodontitisfølsomhed i hele befolkningen. Fx skulle en 80-årig patient have < 20 % knogletab på alle tænder, hvis sygdommen skulle karakteriseres som langsomt progredierende (29). Dietrich et al. har derfor på baggrund af genberegninger foreslået alternative tærskelværdier: Grad A < 0,5; Grad B 0,5–1,0 og Grad C > 1,0. Disse modificerede kriterier vil blive anvendt i denne artikel. Hvis facit bliver < 0,50 (fx 0,42 ved 25 % knogletab hos en 60-årig patient) (29), kan patienten nedgraderes til Grad A. Endvidere peger det også i retning af Grad A, hvis patienten ikke har risikofaktorer som rygning og diabetes.
Grad B (moderat progression)
Hvis kliniske og radiologiske data viser, at der er sket et fæstetab på < 2 mm i løbet af de seneste fem år, hører patienten til Grad B. Andre karakteristika er, at der er korrelation mellem CAL og mængden af biofilm, eller at forholdet mellem knogletab og alder ligger fra 0,50 til 1,0 (fx 0,63 ved 25 % CAL hos en 40-årig). Personer med moderat tobaksforbrug (< 10 cigaretter/dag) og velkontrolleret diabetes (HbA1c <7,0 %) vil typisk også høre til Grad B.
Grad C (hurtig progression)
Hvis kliniske og radiologiske data viser, at der er sket et fæstetab på mindst 2 mm i løbet af de seneste fem år, hører patienten til Grad C. Andre karakteristika er, at CAL er større end forventet ud fra mængden af biofilm, eller at forholdet mellem knogletab og alder er > 1,0 (fx 1,50 ved 30% knogletab hos en 20-årig). Storrygere (≥ 10 cigaretter/dag) og patienter med dårligt reguleret diabetes (HbA1c ≥ 7,0%) vil typisk også høre til Grad C. Endelig kan Grad C også omfatte patienter, der ikke responderer som forventet på sufficient infektionskontrol, og patienter med CAL, der er lokaliseret til incisiver og molarer.
|
Grad A Langsom progression |
Grad B Moderat progression |
Grad C Hurtig progression |
|
|---|---|---|---|
Bedømmelse af CAL over tid |
Ingen CAL de seneste fem år |
< 2 mm de seneste fem år |
≥ 2 mm de seneste fem år |
Pct. knogletaba/alder |
<0,5 |
0,5–1 |
>1,0 |
CAL i relation til mængden af biofilm |
Beskedent CAL trods betydelige mængder biofilm |
CAL som forventet ud fra mængden af biofilm |
Mere CAL end forventet ud fra mængden af biofilm |
Risikofaktorer |
Ikke-ryger Ingen diabetes / normoglykæmisk (HbA1c < 6,5 %) |
Ryger 1–9 cigaretter pr. dag Velreguleret diabetes (HbA1c < 7,0 %) |
Ryger ≥ 10 cigaretter pr. dag Forhøjet HbA1c (≥ 7,0 %) |
Generelt formoder man, at patienten har Grad B, og efterfølgende kigger klinikeren efter fund, der kan berettige nedgradering til Grad A eller opgradering til Grad C.
a Registreret radiologisk på den værst afficerede tand.
Hvordan påvirkes stadier og grader af behandling?
En patient kan stige til et højere stadium, hvis tilstanden forværres over tid; men det er som regel ikke muligt at gå den modsatte vej, selv ikke efter vellykket behandling. Mistede tænder vender ikke tilbage, og det radiologisk bedømte knogletab vil almindeligvis være uforandret, selv om pochedybde og klinisk fæstetab reduceres efter behandlingen. Ligeledes vil der oftest stadig være vertikalt knogletab og furkaturinvolvering, selv om disse defekter på grund af opstramning af vævet ikke længere kan sonderes. Selv om det efter vellykket regenerationsbehandling er muligt at reducere fæstetab og/eller knogletab fra mere end en tredjedel af rodlængden til højst en tredjedel, anbefales det at lade patienten beholde det stadium, der blev tildelt inden behandlingen (30).
Derimod kan gradinddelingen løbende ændres. Fx kan man nedgradere, hvis det lykkes at standse sygdomsprogressionen og opnå kontrol over risikofaktorerne, eller man kan opgradere, hvis sygdomsbilledet forværres, fx i forbindelse med udvikling af dårligt reguleret diabetes.
Hvordan anvendes den nye parodontitisklassifikation i daglig klinisk praksis?
Klinisk beslutningsproces
Trin 1: Parodontal undersøgelse og udfyldelse af diagram
Alle patienter skal i forbindelse med regelmæssige undersøgelser have foretaget parodontal undersøgelse af samtlige tænder med vurdering af, om der er tale om parodontal sundhed eller sygdom (31). Med henblik på at etablere en definitiv diagnose af forskellige parodontale tilstande registreres synlig plak, blødning ved pochemåling (BoP), fordybede pocher, gingivale retraktioner, furkaturinvolveringer og tandmobilitet i et parodontaldiagram. Endvidere noteres, hvor mange tænder der er mistet på grund af parodontitis.
Fig. 1 viser et klinisk beslutningsdiagram, som kan vejlede klinikeren i at stille den korrekte parodontale diagnose (29,31,32). Når der ikke konstateres noget parodontitisrelateret fæstetab, baseres den parodontale diagnose på BoP-registreringer fra hele tandsættet (fx BoP < 10 % repræsenterer et sundt parodontium, mens der ved gingivitis er BoP ≥ 10 %) (9).
Klinisk beslutningsvej
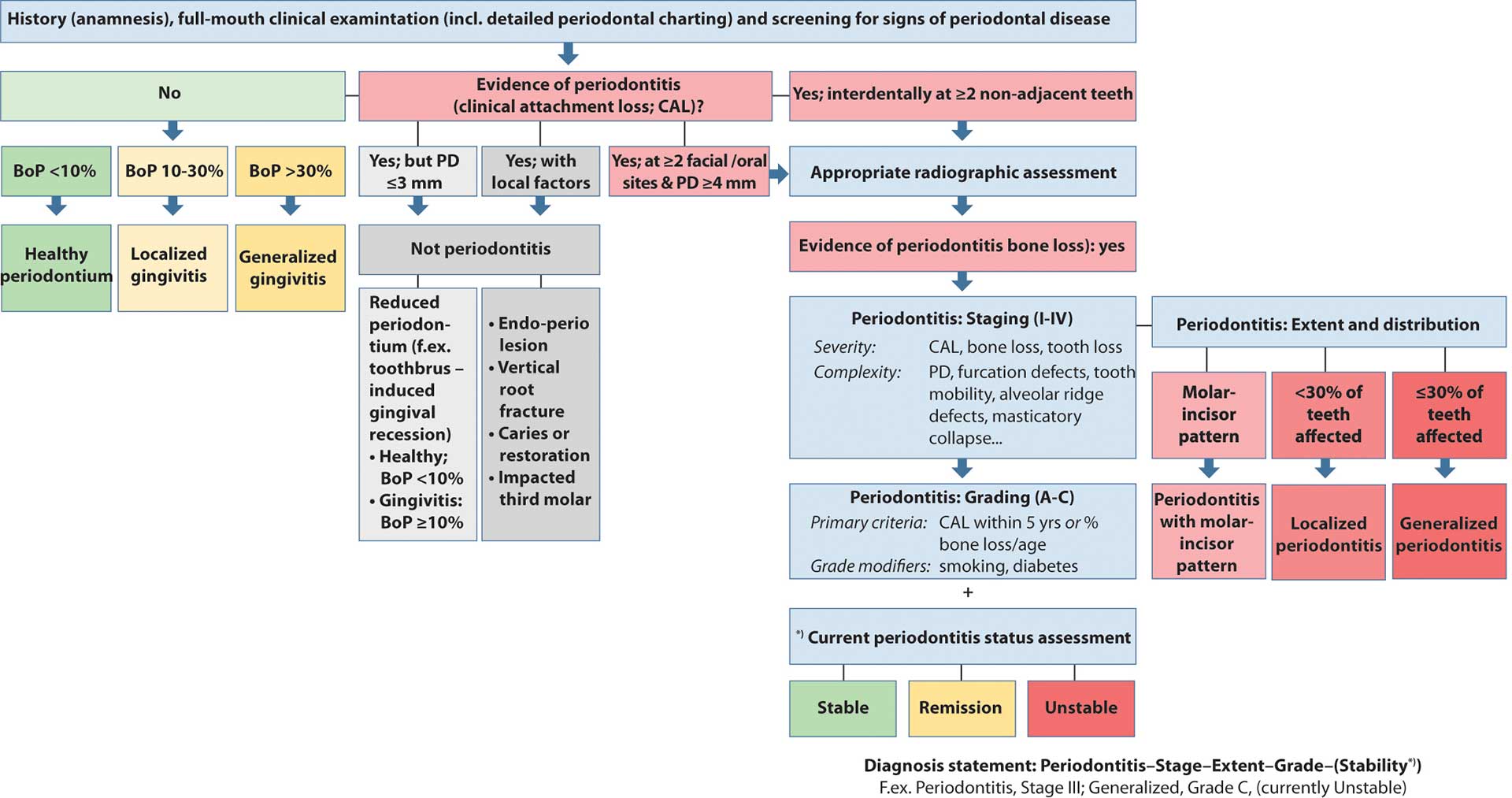
Fig. 1.Flowdiagram over den kliniske beslutningsvej, når den nye klassifikation af parodontale sygdomme i klinisk praksis skal udmøntes i en parodontologisk diagnose (tillempet fra (29,31,32)). Kriterierne for stadier (I-IV) og grader (A-C) gennemgås detaljeret i hhv. Tabel 2 og Tabel 3. Den aktuelle parodontalstatus defineres som: Stabil = sunde forhold hos en velbehandlet patient (BoP < 10 %; PD ≤4 mm og ingen BoP ved pocher på mm), Remission = fortsat gingival inflammation (BoP ≥ 10 % på steder med PD ≤ 3mm og ingen PD > 4mm) eller Ustabil = fortsat parodontitis med blødende pocher ≥ 4 mm eller PD ≥ 5 mm uanset blødning (27).
Trin 2: Initial parodontitisdiagnose og differentialdiagnostik
Når der konstateres kliniske tegn på CAL, som tyder på potentiel forekomst af parodontitis, undersøges knogleniveauet på et passende antal røntgenoptagelser. Klinikeren skal vurdere, om der findes horisontalt og/eller vertikalt knogletab eller furkaturinvolveringer som følge af parodontitis. De mulige differentialdiagnoser som vertikale rodfrakturer, endodontisk-parodontale læsioner eller gingivale retraktioner som følge af mekaniske traumer skal kunne udelukkes. I tilfælde med CAL (herunder PD ≥ 4 mm) og radiologisk konstaterede knogledefekter stilles diagnosen parodontitis, som derefter udbygges med bestemmelse af sygdomsudbredelse, stadium og grad (14,15).
Trin 3: Bestemmelse af parodontitisstadium og sygdomsudbredelse
Inddelingen af parodontitis i stadier afspejler sygdommens alvorlighed, som den udtrykkes ved CAL, knogledefekter og tab af tænder som følge af parodontitis (Tabel 2). Endvidere giver stadierne et billede af den samlede behandlingsplans kompleksitet gennem registrering af PD, furkaturer, vertikale knogledefekter, hypermobile tænder, sekundære okklusale traumer, bidkollaps og/eller antallet af okkluderende tandpar.
Ud fra antallet af afficerede tænder og disses placering i tandsættet angives sygdomsudbredelsen som lokaliseret (< 30 % af tænderne), generaliseret (≥ 30 % af tænderne) eller molar-/incisiv-mønster (14).
I konsensusartiklen (14) slås det fast, at sygdomsudbredelsen skal beskrives efter fastlæggelsen af stadiet. »Udbredelse« refererer således til det stadium, der overordnet beskriver tilfældets alvorlighed og kompleksitet. Dermed beskrives den procentandel af tænderne, der er alvorligt ramt af sygdommen og sandsynligvis vil kræve behandling med høj kompleksitet (33).
Trin 4: Gradinddeling af sygdommen – bestemmelse af patientens sygdomsmodtagelighed
Gradinddelingen skal afspejle patientens modtagelighed for parodontitis gennem identifikation af de potentielle risikofaktorer, der igennem patientens livsforløb har relation til knogletab (14,29,31). Sygdommens progressionshastighed (A: langsom/B: moderat/C: hurtig) i løbet af de seneste fem år bedømmes ud fra tidligere parodontale registreringer (Tabel 3). Hvis man ikke har adgang til tidligere registreringer, kan ratioen knogletab-pct./alder beregnes ved hjælp af panoramaoptagelser eller enorale røntgenoptagelser. Det er den værst ramte tand, der danner grundlag for denne vurdering. Alle patienter skal udspørges om rygevaner og blodglukoseværdier, da rygning og diabetes kan medføre opgradering til en højere grad.
Den overordnede diagnose, udbredelsen og inddelingen i stadier og grader kan munde ud i forskellige komplekse diagnoser som fx:
Parodontitis Stadium II, lokaliseret, Grad A
Parodontitis Stadium IV, molar-/incisiv-mønster, Grad B
Nekrotiserende parodontitis Stadium III, lokaliseret, Grad C.
I Fig. 2 ses et eksempel på praktisk anvendelse af klassifikationen.
Praktisk eksempel
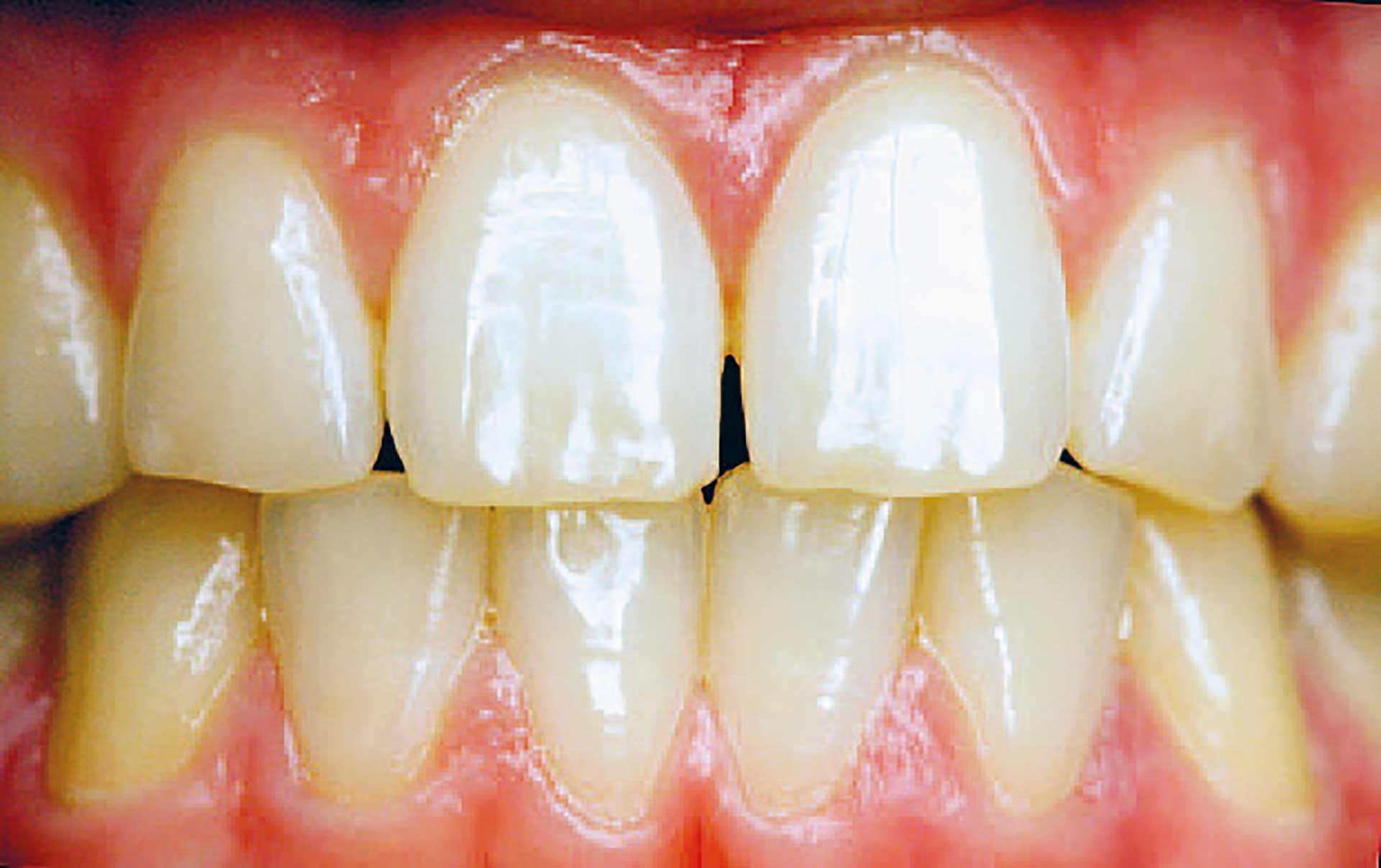
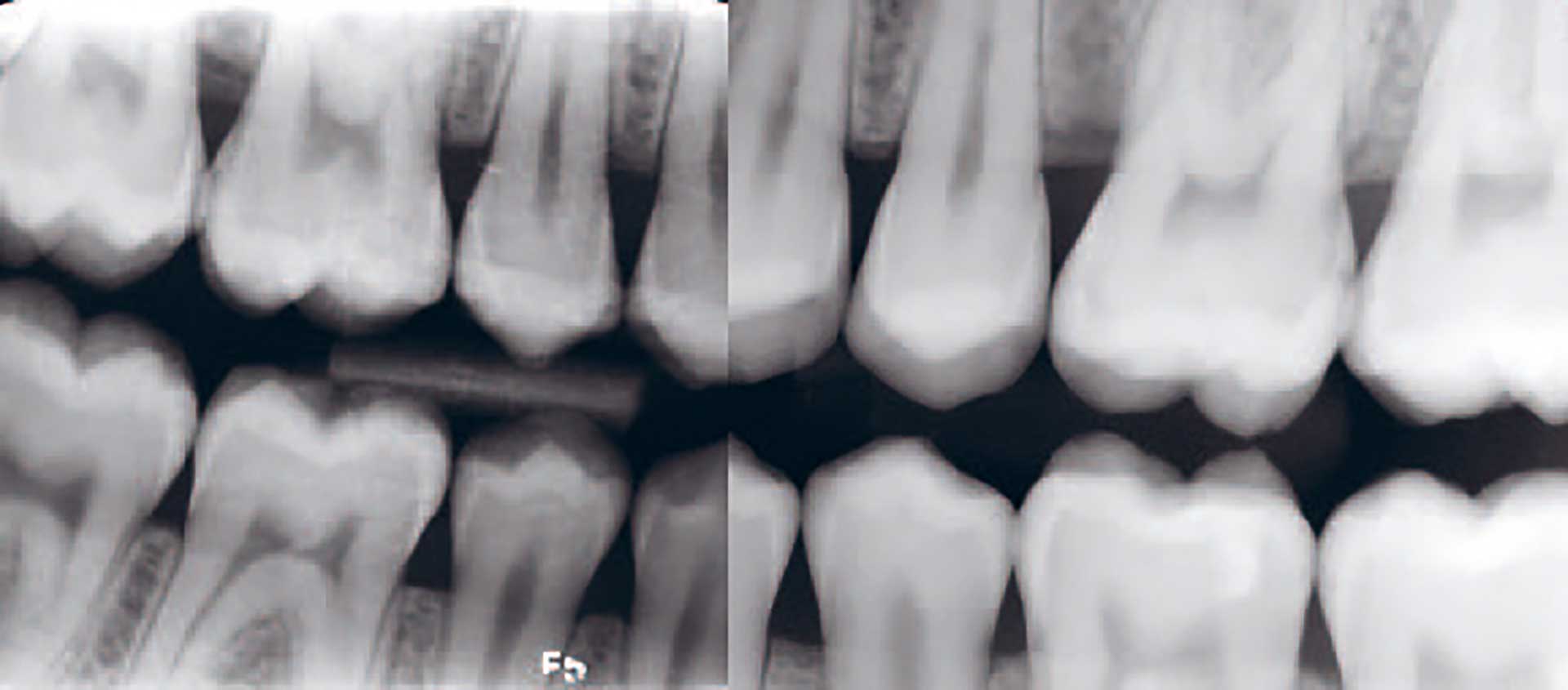
Fig. 2. 18-årig mand, ikke-ryger, diabetes type 1. 6+6 har 2 mm CAL, 5 mm pochedybde og blødning ved pochemåling. Et år tidligere var der ingen CAL. Patienten oplyser, at hans diabetes for tiden er dårligt reguleret.
Stadium: 2 mm CAL og minimalt radiologisk bedømt knogletab tyder på Stadium I; men der opgraderes til Stadium II på grund af pochedybder på 5 mm.
Udbredelse: Lokaliseret, da < 30 % af tænderne er afficerede. Grad: 2 mm CAL i løbet af et år indikerer opgradering til Grad C. Dette bekræftes af den dårlige diabetesregulering og det forhold, at CAL er større end forventet ud fra den meget fine biofilmkontrol.
Diagnose: Parodontitis Stadium II, lokaliseret, Grad C (fra (1)).
Hvordan kan implementering af den nye klassifikation blive til gavn for patienter og klinikere?
Den nye klassifikation kan ved første øjekast forekomme kompliceret; men egentlig er der bare tale om, at en række kendte elementer kombineres på en ny måde. Tandlæger er vant til at registrere gingival blødning, pochedybder, CAL, furkaturinvolveringer, løsningsgrader og manglende tænder. Der er heller ikke noget nyt i at bedømme knogletab på røntgenoptagelser, spørge ind til risikofaktorer som rygning og diabetes eller vurdere, om vævsdestruktion og mundhygiejne står i et rimeligt forhold til hinanden.
Individualisering af den parodontologiske behandlingsplan
Diagnosen er udgangspunktet for udarbejdelse af en individuel behandlingsplan og for gennemførelse af en parodontalbehandling (28). Selv om parodontitis primært diagnosticeres på baggrund af tidligere sygdomsudvikling, er der dele af diagnosen, der peger fremad. Dette gør det diagnostiske system velegnet til behandlingsplanlægning og livslang overvågning af patienter med parodontitis. Parodontitisklassifikationen kan dermed hjælpe klinikerne med at kommunikere meningsfuldt med deres patienter om parodontitissituationen i fortid, nutid og fremtid.
Vurdering af tidligere progression af parodontitis
Det er et grundlæggende princip i stadieinddelingen, at patienter ikke kan falde tilbage til et lavere alvorlighedsniveau efter behandling (14). Alvorligheden bestemmes først og fremmest af tidligere sygdomserfaringer udtrykt ved CAL og antallet af tænder, der er mistet på grund af parodontitis. De parodontale parametre, der kan ændres signifikant ved behandling, som fx BoP og PD, er ikke udslagsgivende for hverken sygdomsdefinitionen eller alvorligheden af parodontitis. Dermed retter man op på nogle forvirrende elementer i de tidligere diagnostiske systemer (34). Ekstraktion af tænder med håbløs prognose kan ikke længere formindske alvorligheden af parodontitis, og patienter med alvorligt CAL vil fortsat være patienter med svær parodontitis, selv om patologiske pocher elimineres (se eksempel i Fig. 3), og sågar også efter parodontal regeneration med fæstegevinst (30).
Eftersom CAL ikke altid registreres rutinemæssigt i klinisk praksis, kan alment praktiserende tandlæger anvende en forenklet stadieinddeling på grundlag af radiologisk dokumenteret knogletab. Alvorligheden kan let bestemmes ud fra knogletabet angivet i procent af rodlængden. Meget praktisk er det samme procentandel, der anvendes ved gradinddelingen, hvor den divideret med patientens alder giver et udtryk for sygdomsprogressionen over tid (12).
Udbredelsen af parodontitis kategoriseres som enten lokaliseret eller generaliseret ud fra, hvor mange tænder der har det højeste stadium. Sygdomsudbredelsen defineres dermed udelukkende ud fra de tænder/den tand, der bestemmer stadiet. I nogle tilfælde forekommer denne diagnostiske proces intuitivt at være utilstrækkelig. For eksempel vil en patient med 28 tænder, som har CAL svarende til Stadium I og II, og én molar med inkomplet furkaturinvolvering få diagnosen parodontitis Stadium III, lokaliseret.
Vedvarende alvorlig parodontitis
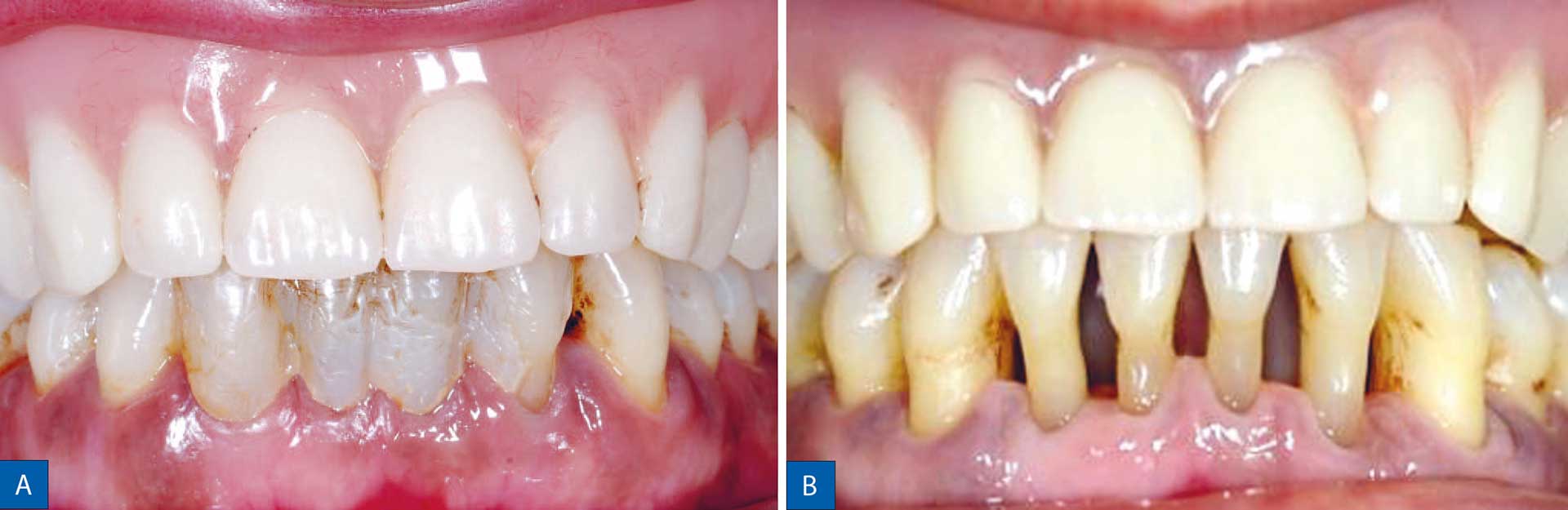
Fig. 3.
A. 59-årig kvinde, ikke-ryger og ved godt helbred, har mistet 13 tænder på grund af parodontitis. Der er knogletab i den apikale tredjedel af rodlængden ved incisiverne i underkæben, PD 6–8 mm og furkaturinvolvering af klasse II. Hun fik diagnosen Parodontitis, Stadium IV, generaliseret, Grad C.
B. Efter vellykket parodontalbehandling havde patienten ingen PD > 3 mm, og BoP var 14 %. Patientens parodontale diagnose forbliver uændret; men på grund af behandlingsresultatet klassificeres tilstanden nu som gingivitis i et reduceret parodontium.
Vurdering af aktuel parodontal status
Det er af afgørende betydning, at klinikeren er i stand til at skelne mellem sundhed og sygdom. Den nye klassifikation indeholder en klar definition på parodontal sundhed, idet den anvender den praktiske betegnelse »klinisk sund« til patienter, der har minimal eller ingen gingival inflammation (5). Parodontal sundhed kan opnås både for patienter med et normalt parodontium og for patienter med et reduceret parodontium efter vellykket parodontalbehandling. I tilfælde med få steder med gingival blødning er det vigtigt at skelne mellem gingivitis og parodontitis, men det endelige mål for behandlingen af begge sygdomme er at opnå parodontal sundhed (8). Det er vigtigt at huske, at forekomst af BoP ikke definitivt betyder parodontitis, men at fravær af BoP er tegn på stabile forhold og et klinisk sundt parodontium (35).
Selv om definitionen på parodontitis savner en direkte forbindelse til de parodontale parametre, der er tegn på aktiv sygdom, defineres stabil henholdsvis ustabil parodontitis dog ved hjælp af BoP og PD. PD-tærskelværdien på 4 mm er kritisk, fordi den betegner en stabil tilstand i områder uden gingival blødning (9,29,36).
Vurdering af fremtidig progression af parodontitis
Alvorligheden af parodontitis afhænger af sygdomserfaring tidligere i livet; men stadiet kan også anvendes til at forudsige fremtidig sygdomsmodtagelighed (37). Komplicerende faktorer, som kan give fingerpeg om suboptimale behandlingsresultater, kan modificere/forværre sygdomsstadiet. Derfor er stadieinddelingen ikke udelukkende en forståelse af tidligere sygdomserfaringer, og både stadier og grader rummer formodninger om fremtidig sygdomsprogression, selv om det kun er graden, der kan ændres i nedadgående retning.
Det primære formål med gradinddelingen er at afgøre, om en given patient vil respondere på en normal parodontalbehandling med fokus på infektionskontrol. Graden peger hen imod fremtidig sygdomsmodtagelighed ved at inddrage årsagsfaktorer som plak og rygning og en faktor som diabetes, der har indvirken på værtssvaret. En parodontitispatient, der hidtil har udvist moderat progression (Grad B), men har disse modificerbare forhold, der tyder på forøget risiko for fremtidig sygdomsprogression, vil blive diagnosticeret med parodontitis Grad C. Plak, rygning og diabetes kan bidrage til at forudsige risiko for yderligere progression, men intervention over for disse faktorer bør også indgå som mål for behandlingen (30). Gradinddelingen hjælper klinikeren med at vurdere den enkelte patients sygdomsmodtagelighed og forventelige sygdomsforløb og er et brugbart redskab i forbindelse med behandlingsplanlægning og kommunikation med patienterne.
Pochemåling er et surrogatmål for det parodontale fæsteniveau og et godt udtryk for sygdommens alvorlighed, mulighederne for effektiv behandling og stabiliteten af sygdommen. Jo dybere pocher, jo vanskeligere depuration, og PD > 5 mm peger i retning af yderligere fæstetab og tandtab (36). Tilsvarende vil forekomst af profund furkaturinvolvering og vertikalt knogletab pege i retning af forringet behandlingsresultat og progression af sygdommen (14).
Det nye system med stadier og grader inddrager faktorer, der hænger sammen med et kompliceret behandlingsforløb. Risikovurderingen er baseret på veldokumenterede risikofaktorer som rygning, dårligt reguleret diabetes, kliniske tegn på sygdomsprogression og sygdomsdebut i ung alder og omfanget af knogletab i relation til alderen. I denne sammenhæng er det vigtigt at huske, at betydelige risikofaktorer som tobaksrygning og diabetes samt andre sygdomme, der kan påvirke udviklingen af parodontitis, bør medinddrages i epidemiologiske studier, der søger at afspejle den reelle sygdomsbyrde på individ- og samfundsniveau (20).
Undersøgelser tyder på, at nogle personer er mere tilbøjelige end andre til at udvikle progredierende, alvorlig og generaliseret parodontitis og desuden responderer dårligere på sædvanlige profylaktiske og terapeutiske tiltag (14). Så længe vi ikke i praksis har adgang til biologiske markører for parodontitisrisiko, er det særligt vigtigt omhyggeligt at registrere kliniske og anamnestiske parametre og anvende det nye klassifikationssystem. Fremtidige epidemiologiske undersøgelser, der baseres på det nye klassifikationssystem, kan måske gøre det lettere at identificere personer med særlig høj modtagelighed for parodontitis. De hidtidige epidemiologiske studier af fremskreden parodontitis har anvendt forskellige kriterier, hvilket gør det vanskeligt at sammenligne studierne; men de viser i det mindste, at fremskreden parodontitis ikke er nogen sjælden tilstand (13,38,39).
Klassifikation og omfang af sygdomsbyrden på befolkningsniveau
Prævalensen af parodontitis og enhver anden sygdom kan estimeres forskelligt afhængigt af, hvordan man definerer sygdommen, hvilken population man undersøger, og hvilke screeningsmetoder man vælger at anvende (40).
På WWCP blev der fastlagt klare kriterier for alvorlig parodontitis (Tabel 2). Stadium III beskriver alvorlig parodontitis med potentiale for yderligere tandtab, og Stadium IV beskriver fremskreden parodontitis med udbredt tandtab og potentiale for total tandløshed. Sammen med angivelsen af sygdommens udbredelse i tandsættet identificerer kriterierne for Stadium III og IV personer med henholdsvis alvorlig og fremskreden parodontitis (28).
Den seneste undersøgelse (2009–2012) i den række af nationale epidemiologiske studier, der er gennemført i USA siden 1960’erne, viser, at 9 % havde alvorlig parodontitis (defineret som en kombination af PD > 5 mm og CAL > 6 mm) (38). Ud over de høje økonomiske udgifter til parodontalbehandling, der rammer både samfundet og den enkelte patient, er det påvist, at personer med alvorlig/fremskreden parodontitis har dårligere livskvalitet end personer med sunde parodontale forhold (41–43). Det er derfor vigtigt at forbedre identifikationen af personer med parodontitisrisiko for derigennem at fremme forebyggelse og behandling.
I Sverige har man hvert tiende år fra 1973 til 2013 gennemført epidemiologiske undersøgelser, der viser, at andelen af personer med alvorlig parodontitis/parodontitiserfaring (defineret som knoglesvind svarende til mellem 1/3 og 2/3 af rodlængden eller mere end 2/3 af rodlængden på de fleste af tænderne) har ligget temmelig konstant på omkring 10 % siden 1973. Til gengæld er det gennemsnitlige antal tænder steget støt, også for gruppen med udtalt parodontitiserfaring (39). Den nye klassifikation kan forhåbentlig bidrage til at forøge vores viden ved at give en mere præcis beskrivelse af sygdomsbyrden på samfundsniveau.
Resumé
Sammenlignet med klassifikationen fra 1999 er det nye system dynamisk og tillader revurdering i forbindelse med orale og systemiske forandringer. Fordelen ved den nye klassifikation er, at parodontitisdiagnosen karakteriseres ved stadier og grader i et flerdimensionalt system (14,15). Ud over at definere alvorligheden, udbredelsen/fordelingen og progressionen af sygdommen giver den en omfattende risikovurdering og hjælper med at definere en langsigtet behandlingsplan. Ved inddelingen i stadier anvendes CAL som det vigtigste kriterie sammen med andre parodontale indices og tandtab som diagnostiske kriterier, mens inddelingen i grader individualiserer diagnosen yderligere gennem inddragelse af patientens risikofaktorer (fx HbA1c-værdien og tobakseksponeringen) i den diagnostiske proces.
Udbredelsen eller den intraorale fordeling af parodontitis blev tidligere angivet som andelen af sygdomsramte tænder i tandsættet, dvs. parodontitis blev defineret som lokaliseret, hvis ≤ 30 % af tænderne var afficeret, og generaliseret, hvis > 30 % af tænderne var ramt (34). I den nye klassifikation anbefaler man i stedet klinikerne at angive den andel af tænderne, der har det stadium, der definerer diagnosen (lokaliseret, hvis < 30 % af tænderne opfylder kriterierne for Stadium III hos en patient med Stadium III; generaliseret, hvis ≥ 30 % af tænderne opfylder kriterierne) (14,33). Eftersom diagnosen »aggressiv parodontitis« ikke indgår i den nye klassifikation, definerer man nu lignende tilfælde ud fra stadiet, graden og den intraorale fordeling (dvs. molar-/incisiv-mønster) (28).
Tidligere blev en diagnose typisk angivet som fx »Lokaliseret alvorlig kronisk parodontitis«. På grund af ændringerne i sygdomsklassifikation og diagnostiske kriterier er formuleringen af diagnosen også blevet opdateret, så den nu fx kan angives som »Parodontitis, Stadium III, lokaliseret, Grad C«.
Referanser
Klausen B, Holmstrup P. Ny klassifikation af parodontal sygdom. Tandlægebladet. 2018;122:1060–7.
Bunæs DF. Ny klassifikasjon av periodontal og peri-implantat sjukdom. Nøkkelendringar. Nor Tannlegeforen Tid. 2019;129:132–7.
Suslick J. Tandläkartidningen 2020. Ny klassificering för parodontit på plats. (Set 2021 juni). Tilgængelig fra: URL: https://www.tandlakartidningen.se/arkivet/nyhet/ny-klassificering-for-parodontit-pa-plats/
Caton J, Rees T, Pack A et al. Consensus report: non-plaque-induced gingival lesions. Ann Periodontol. 1999;4:30–1.
Lang NP, Bartold PM. Periodontal health. J Periodontol. 2018;89 (Supp 1):S9–16.
Murakami S, Mealey BL, Mariotti A et al. Dental plaque-induced gingival conditions. J Periodontol. 2018;89 (Supp 1):S17–27.
Holmstrup P, Plemons J, Meyle J. Non-plaque-induced gingival diseases. J Periodontol. 2018;89 (Supp 1):S28–45.
Trombelli L, Farina R, Silva CO et al. Plaque-induced gingivitis: Case definition and diagnostic considerations. J Periodontol. 2018;89 (Supp 1):S46–73.
Chapple ILC, Mealey BL, Van Dyke TE et al. Periodontal health and gingival diseases and conditions on an intact and a reduced periodontium: Consensus report of workgroup 1 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018;89 (Supp 1):S74–84.
Herrera D, Retamal-Valdes B, Alonso B et al. Acute periodontal lesions (periodontal abscesses and necrotizing periodontal diseases) and endo-periodontal lesions. J Periodontol. 2018;89 (Supp 1):S85–102.
Fine DH, Patil AG, Loos BG. Classification and diagnosis of aggressive periodontitis. J Periodontol. 2018;89 (Supp 1):S103–19.
Needleman I, Garcia R, Gkranias N et al. Mean annual attachment, bone level, and tooth loss: A systematic review. J Periodontol. 2018;89 (Supp 1):S120–39.
Billings M, Holtfreter B, Papapanou PN et al. Age-dependent distribution of periodontitis in two countries: Findings from NHANES 2009 to 2014 and SHIP-TREND 2008 to 2012. J Periodontol. 2018;89 (Supp 1):S140–58.
Tonetti MS, Greenwell H, Kornman KS. Staging and grading of periodontitis: Framework and proposal of a new classification and case definition. J Periodontol. 2018;89 (Supp 1):S159–72.
Papapanou PN, Sanz M, Buduneli N et al. Periodontitis: Consensus report of workgroup 2 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018;89 (Supp 1):S173–82.
Albandar JM, Susin C, Hughes FJ. Manifestations of systemic diseases and conditions that affect the periodontal attachment apparatus: Case definitions and diagnostic considerations. J Periodontol. 2018;89 (Supp 1):S183–203.
Cortellini P, Bissada NF. Mucogingival conditions in the natural dentition: Narrative review, case definitions, and diagnostic considerations. J Periodontol. 2018;89 (Supp 1):S204–13.
Fan J, Caton JG. Occlusal trauma and excessive occlusal forces: Narrative review, case definitions, and diagnostic considerations. J Periodontol. 2018;89 (Supp 1):S214–22.
Ercoli C, Caton JG. Dental prostheses and tooth-related factors. J Periodontol. 2018;89 (Supp 1):S223–36.
Jepsen S, Caton JG, Albandar JM et al. Periodontal manifestations of systemic diseases and developmental and acquired conditions: Consensus report of workgroup 3 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018;89 (Supp 1):S237–48.
Araujo MG, Lindhe J. Peri-implant health. J Periodontol. 2018;89 (Supp 1):S249–56.
Heitz-Mayfield LJA, Salvi GE. Peri-implant mucositis. J Periodontol. 2018;89 (Supp 1):S257–66.
Schwarz F, Derks J, Monje A et al. Peri-implantitis. J Periodontol. 2018;89 (Supp 1):S267–90.
Hämmerle CHF, Tarnow D. The etiology of hard- and soft-tissue deficiencies at dental implants: A narrative review. J Periodontol. 2018;89 (Supp 1):S291–303.
Renvert S, Persson GR, Pirih FQ et al. Peri-implant health, peri-implant mucositis, and peri-implantitis: Case definitions and diagnostic considerations. J Periodontol. 2018;89 (Supp 1):S304–12.
Berglundh T, Armitage G, Araujo MG et al. Peri-implant diseases and conditions: Consensus report of workgroup 4 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018;89 (Supp 1):S313–8.
DUODECIM. Current Care Guidelines. Periodontitis. Working group set up by the Finnish Medical Society Duodecim and the Finnish Dental Society Apollonia 2019. (Set 2021 juni). Tilgængelig fra: URL: https://www.kaypahoito.fi/hoi50086.
Caton JG, Armitage G, Berglundh T et al. A new classification scheme for periodontal and peri-implant diseases and conditions – Introduction and key changes from the 1999 classification. J Periodontol. 2018;89 (Supp 1):S1–8.
Dietrich T, Ower P, Tank M et al. Periodontal diagnosis in the context of the 2017 classification system of periodontal diseases and conditions – implementation in clinical practice. Br Dent J. 2019;226:16–22.
Kornman KS, Papapanou PN. Clinical application of the new classification of periodontal diseases: Ground rules, clarifications and “gray zones”. J Periodontol. 2020;91:352–60.
Tonetti MS, Sanz M. Implementation of the new classification of periodontal diseases: Decision-making algorithms for clinical practice and education. J Clin Periodontol. 2019;46:398–405.
British society of periodontology. Implementing the 2017 classification of periodontal diseases to reach a diagnosis in clinical practise – flowchart. British Society of Periodontology 2018. (Set 2021 juni). Tilgængelig fra: URL: https://www.bsperio.org.uk/assets/downloads/111_153050_bsp-flowchart-implementing-the-2017-classification.pdf.
Sanz M, Del Castillo AM, Jepsen S et al. Periodontitis and cardiovascular diseases. Consensus report. Glob Heart 2020;15:1.
Armitage GC. Development of a classification system for periodontal diseases and conditions. Ann Periodontol. 1999;4:1–6.
Lang NP, Adler R, Joss A et al. Absence of bleeding on probing. An indicator of periodontal stability. J Clin Periodontol. 1990;17:714–21.
Matuliene G, Pjetursson BE, Salvi GE et al. Influence of residual pockets on progression of periodontitis and tooth loss: results after 11 years of maintenance. J Clin Periodontol. 2008;35:685–95.
Machtei EE, Hausmann E, Dunford R et al. Longitudinal study of predictive factors for periodontal disease and tooth loss. J Clin Periodontol. 1999;26:374–80.
Eke PI, Dye BA, Wei L et al. Prevalence of periodontitis in adults in the United States: 2009 and 2010. J Dent Res. 2012;91:914–20.
Norderyd O, Koch G, Papias A et al. Oral health of individuals aged 3–80 years in Jönköping, Sweden during 40 years (1973–2013). II. Review of clinical and radiographic findings. Swed Dent J. 2015;39:69–86.
Holtfreter B, Albandar JM, Dietrich T et al. Standards for reporting chronic periodontitis prevalence and severity in epidemiologic studies: Proposed standards from the Joint EU/USA Periodontal Epidemiology Working Group. J Clin Periodontol. 2015;42:407–12.
Jansson H, Wahlin Å, Johansson V et al. Impact of periodontal disease experience on oral health-related quality of life. J Periodontol. 2014;85:438–45.
Ng SK, Leung WK. Oral health-related quality of life and periodontal status. Community Dent Oral Epidemiol. 2006;34:114–22.
Cunha-Cruz J, Hujoel PP, Kressin NR. Oral health-related quality of life of periodontal patients. J Periodontal Res. 2007;42:169–76.
English summary
The new classification on periodontitis. How to apply the classification in daily clinical work
Nor Tannlegeforen Tid. 2022; 132: 10–20.
The classification of periodontal diseases has been re-organised after extensive work in expert groups followed by an international workshop arranged by the American Academy Periodontology and the European Federation of Periodontology in 2017. The international expert panel at the workshop representing countries from around the world has agreed on the definitions, which in addition to a description of periodontitis include descriptions on the intact periodontium, periodontal health, biofilm-induced gingivitis, and non-biofilm-induced gingival disease. The present article focuses on periodontitis.
Periodontitis is a condition with interdental clinical attachment loss (CAL) of at least 1 mm on at least two non-neighbouring teeth or a buccal/lingual CAL of at least 3 mm on at least two teeth. According to severity periodontitis is further subdivided in four stages (I – IV), and three grades (A, B, C) according to rate of progression and risk factors. Furthermore, the extent and distribution of the disease must be stated.
Here we describe how the new classification on periodontitis applies to every-day clinical practice, how can patients and the clinical profession benefit from implementation of the new classification, and what is the magnitude of the problem, i.e. the prevalence of severe periodontitis? The article also presents representative cases to illustrate the new concept of staging and grading.
Korrespondanceansvarlig forsteforfatter: Palle Holmstrup. E-mailadresse: pah@sund.ku.dk
Artikkelen har gjennomgatt ekstern faglig vurdering.
Holmstrup P, Bunas D, Gursoy M, Lundberg P. Den nya klassificeringen av parodontit. Nor Tannlegeforen Tid. 2022; 132: 10–20.
Emneord: Periodontitis; classification; diagnostics; bleeding on probing; clinical attachment; loss; bone loss; periodontal examination