Orale lichenoide kontaktlesjoner – en oversikt
Hovedbudskap
Orale lichenoide kontaktlesjoner er blant de vanligste bivirkningene av odontologiske biomaterialer og er oftest sett i forbindelse med amalgamfyllinger.
Utredning av orale lichenoide kontaktlesjoner krever god kunnskap om differensialdiagnostikk og baseres hovedsakelig på kliniske funn, eventuelt supplert med histologisk vurdering og allergitesting (epikutantesting).
Restaureringer som forårsaker orale lichenoide kontaktlesjoner bør fjernes og erstattes av et annet materiale etter at fordeler og ulemper er drøftet med pasienten. Ved manglende tilheling etter utskifting av restaureringsmateriale bør diagnosen revurderes.
Orale lichenoide forandringer generelt oppfattes av Verdens helseorganisasjon som potensielt maligne tilstander, på grunn av økt risiko for malignitetsutvikling. Det er omdiskutert hvorvidt dette gjelder for orale lichenoide kontaktlesjoner.
Alle mistenkte bivirkningsreaksjoner bør rapporteres til Bivirkningsgruppen.
Orale lichenoide kontaktlesjoner forårsaket av odontologiske biomaterialer forekommer relativt sjeldent, men kan gi opphav til betydelige plager hos pasienten. Hovedsakelig er det kvikksølv i amalgam som er årsak til slike lesjoner. I denne oversiktsartikkelen ønsker vi å gi en kortfattet introduksjon til orale lichenoide kontaktlesjoner, med vekt på etiopatogenese, klinisk og histologisk bilde, og differensialdiagnostisk utredning. Videre oppsummerer artikkelen behandlingsalternativer og utfall. Vi diskuterer også om orale lichenoide kontaktlesjoner har en risiko for malignitetsutvikling, og at dette innebærer et ansvar for å følge pasienten opp over tid, samt samarbeide med spesialisthelsetjenesten ved behov.
Odontologiske biomaterialer defineres som materialer som inkorporeres eller implanteres i munnhulen [1]. Utviklingen av nye og mer komplekse materialer er rask og omfattende. Det er stor oppmerksomhet rundt materialenes bruksegenskaper, og dette er helt avgjørende for at tannhelsepersonell skal kunne tilby tannhelsetjeneste av høy kvalitet. Samtidig innebærer alle materialer en risiko for bivirkninger, og vi som tannleger har et ansvar for å oppdatere vår kunnskap om disse. En av styrkene i Norge er at vi har et nasjonalt rapporteringssystem og mulighet for å henvise til «Bivirkningsgruppen for odontologiske biomaterialer» (bivirkningsgruppen.norceresearch.no). Dette er viktig for å skaffe mer informasjon om materialene på markedet og bidrar til trygg bruk. I Norge har vi også sterke fagmiljøer ved universiteter og andre institusjoner som «Nordisk Institutt for Odontologiske Materialer» (niom.no) med mye kunnskap og erfaring.
Bivirkninger fra odontologiske biomaterialer varierer fra lett ubehag til mer alvorlige symptomer som reduserer pasientenes livskvalitet [2]. Livstruende anafylaksi kan også forekomme, men oppstår svært sjelden [3] [4]. En av de vanligste bivirkningsreaksjonene fra odontologiske biomaterialer er såkalte orale lichenoide kontaktlesjoner. Disse har ofte et klinisk utseende og histologisk bilde som minner om andre sykdommer, noe som kan gi differensialdiagnostiske utfordringer. I denne artikkelen gjennomgår vi kunnskap om definisjon, etiopatogenese og klinisk/histologisk presentasjon av orale lichenoide kontaktlesjoner, samt diskuterer hvordan disse forandringene kan behandles. Artikkelen bygger på studier og oversiktsartikler i sentrale tidsskrift, samt på nasjonale retningslinjer.
Definisjon og etiopatogenese
Begrepet «lichenoid reaksjon» ble først introdusert i dermatologi for 50 år siden for å beskrive en gruppe inflammatoriske hudsykdommer som hadde felles histologiske trekk, nemlig degenerasjon av basalcellelaget og båndformet inflammatorisk infiltrat, hovedsakelig bestående av aktiverte T-lymfocytter [5]. I likhet med hud, kan også munnslimhinnen bli affisert av et spektrum av lichenoide forandringer. Disse forandringene er blitt klassifisert som enten klassisk oral lichen planus eller orale lichenoide forandringer. De sistnevnte inkluderer alle forandringer som ligner på oral lichen planus, men som mangler typiske kliniske eller histologiske trekk [6]. De omfatter ulike tilstander som, under «World Workshop of Oral Medicine» i 2006 ble delt inn i tre hovedtyper: 1) orale lichenoide kontaktlesjoner forårsaket av dentale materialer eller aromastoffer som er i kontakt med munnslimhinnen; 2) orale lichenoide legemiddelreaksjoner forårsaket av systemisk virkende legemidler; og 3) orale lichenoide forandringer som følge av transplantat-mot-vert sykdom og da vanligvis den kroniske formen av denne tilstanden [7]. Deler av fagmiljøet synes at flere sykdommer bør inkluderes i klassifiseringen av orale lichenoide forandringer på grunn av felles kliniske og/eller histologiske trekk, blant annet lichenoide forandringer av lupus erythematosus og kronisk ulcerøs stomatitt [8].
Til tross for uenighet i definisjon og inndeling, tror man at både oral lichen planus og lichenoide forandringer representerer en respons mot ulike fremmede antigener, autoantigener eller superantigener, som fører til en immunmediert destruksjon av basalcellelaget i epitelet [9]. Ved orale lichenoide kontaktlesjoner forårsaket av odontologiske biomaterialer er det hovedsakelig komponenter av materialene i kontakt med munnslimhinnen som fungerer som et antigen og som binder seg til autologt HLA-protein. Dette komplekset blir så via antigenpresenterende celler presentert for T-lymfocytter, som sensibiliseres og prolifererer i lokale lymfeknuter. T-hukommelsesceller blir dannet. Ved ny eksponering for antigenet vil slike T-hukommelsesceller utløse en kontaktallergisk reaksjon og føre til vevsskade (figur 1) [10]. Fordi det kan ta en til tre dager for en slik reaksjon å utvikle seg, kalles den en forsinket hypersensitivitetsreaksjon [10].
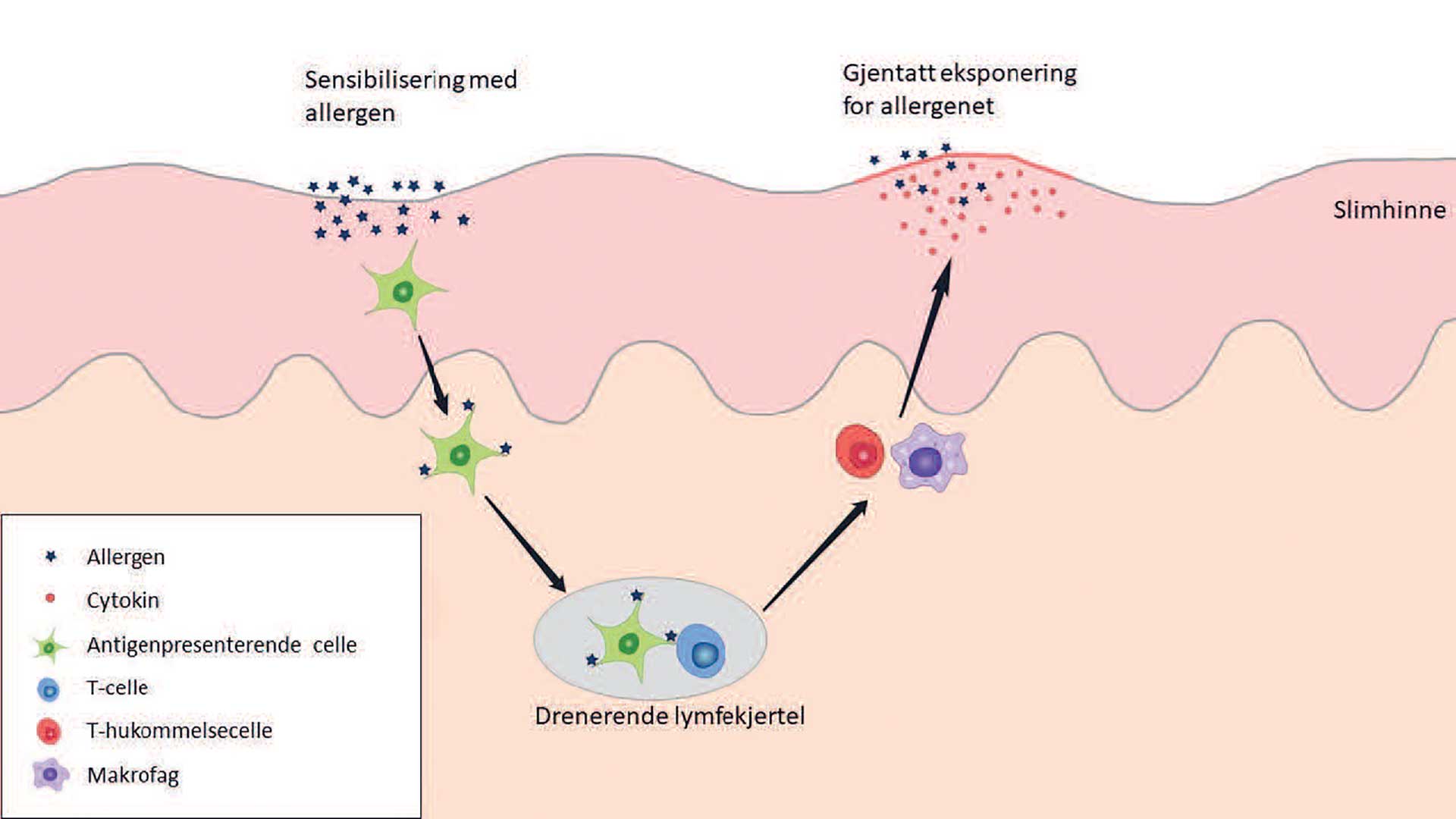
Figur 1. Forsinket/cellemediert hypersensitivitet. Allergenet (stjerner) (f.eks. kvikksølv) blir presentert for T-lymfocytter (blå celler) av antigenpresenterende celler (grønne celler). T-hukommelsesceller (røde celler) blir dannet. Ved ny eksponering for samme antigen gjenkjenner disse T-hukommelsesceller antigenet og starter en prosess med celledeling og utskillelse av cytokiner. Dette tiltrekker makrofager (lilla celler) og andre celler og resulterer i en kontaktallergisk reaksjon som kan forårsake betydelig vevskade.
Til tross for utbredt bruk av odontologiske biomaterialer er orale lichenoide kontaktlesjoner relativt sjeldne. Resultatene fra en epidemiologisk studie fra Italia viser at forekomsten av orale lichenoide forandringer i et representativt utvalg av den voksne befolkningen er 0,29%, men i studien er det ikke spesifisert hvor stor andel av disse som var kontaktlesjoner [11]. Lav forekomst kan forklares med at munnslimhinnen er mer resistent mot allergiske reaksjoner enn huden. Dette kan delvis skyldes komplekse immunologiske reguleringsmekanismer som bidrar til utvikling av munnslimhinnens toleranse overfor allergener [12]. En annen forklaring kan være at saliva stadig fornyes og skyller bort antigener fra munnhulen (clearance). Orale lichenoide kontaktlesjoner oppstår som regel mange år etter den første kontakten med restaureringsmaterialet [10], og pasientenes gjennomsnittsalder er angitt til å være omtrent 54 år [13] [14].
Orale lichenoide kontaktlesjoner er oftest sett i forbindelse med amalgamfyllinger [10] [15]. Generelt bruk av amalgam i Norge ble forbudt i 2008 av hensyn til miljøet. Fordi amalgamfyllinger har lang levetid og fremdeles er i bruk i mange andre land, er det fortsatt mange pasienter som har slike fyllinger. Dentalt amalgam er en legering av kvikksølv og andre metaller som kobber, sølv, tinn og zink [10], der kvikksølv er det mest dokumenterte allergenet. Studier viser at mellom 47% og 70% av pasientene med lichenoide kontaktlesjoner topografisk relatert til amalgamfyllinger vil være positive ved epikutantesting med kvikksølv [13] [16]. Det er derimot kun en liten andel, cirka 4%, av den generelle befolkningen som er positive ved epikutantesting med kvikksølv [17]. Dette kan tyde på at allergiske mekanismer er involvert.
Orale lichenoide kontaktlesjoner kan i sjeldne tilfeller også skyldes en allergisk reaksjon mot andre materialer enn amalgam. Slike materialer kan for eksempel være metaller som gull, palladium, nikkel og kobolt [14] [16] [18]. Orale lichenoide kontaktlesjoner forårsaket av allergi mot polymerbaserte materialer er ikke påvist. Lichenoide forandringer i kontakt med komposittfyllinger i fronten er beskrevet [19] [20], men epikutantesting er negativ i de fleste pasienter [19]. Forfatterne av studiene hevder at forandringene ikke skyldes allergi mot komposittkomponenter, men trolig utløses av mikroorganismer som fester seg til materialenes porøse overflate [2] [19] [20].
Kliniske og histologiske funn
Klinisk karakteriseres oral lichen planus og orale lichenoide forandringer av hvite retikulære og/eller papulære strukturer som ofte er asymptomatiske [8]. En plakk-variant kan også forekomme. Disse hvitlige forandringene oppstår på grunn av hyperkeratose og er epitelets svar på mild inflammasjon [2]. I tillegg kan atrofiske forandringer, erosjoner og ulcerasjoner oppstå av og til (figur 2A og 2B), noe som indikerer mer aktiv inflammasjon og som gir opphav til subjektive symptomer [2]. Pasientene klager ofte over svie, brennende følelse eller smerter, og det er ikke vanskelig å forestille seg at slike symptomer kan interferere med spising og munnhygiene, samt redusere pasientens livskvalitet. Tilstandene karakteriseres av et syklisk forløp hvor symptombildet og den kliniske presentasjonen varierer over tid [8].
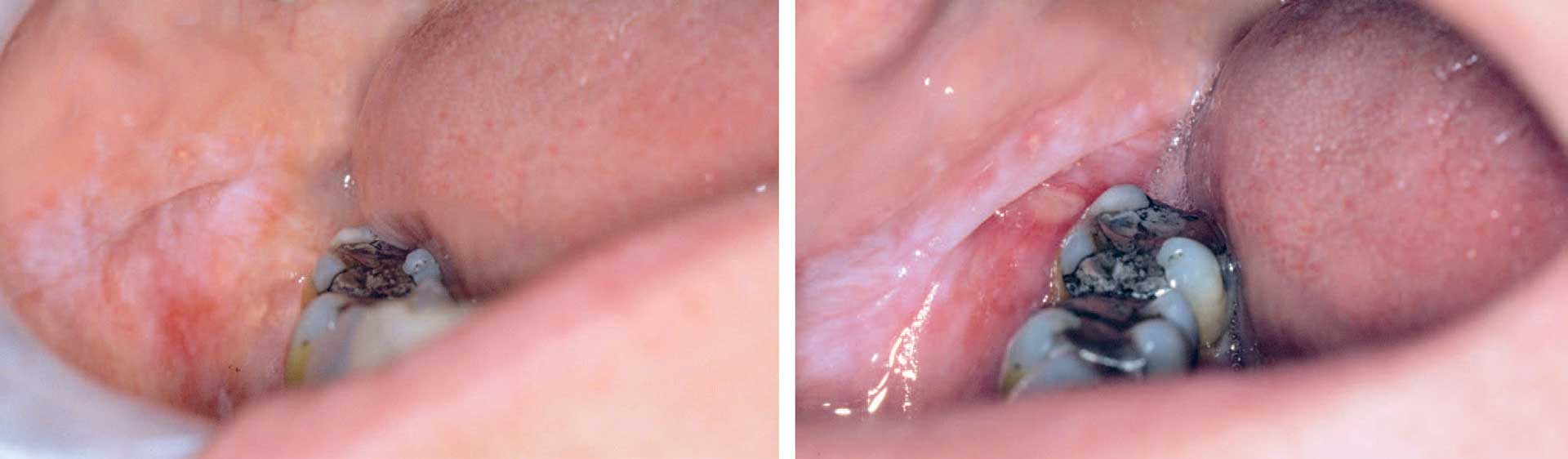
Figur 2. A) Lichenoid kontaktlesjon mot amalgam med både røde og hvite elementer på høyre kinnslimhinne. B) To uker senere oppsto ulcerasjoner i området, og pasienten hadde betydelige symptomer.
Kliniske tegn ved orale lichenoide kontaktlesjoner og oral lichen planus er svært like, men orale lichenoide kontaktlesjoner kan mangle det karakteristiske retikulære mønsteret man ser ved oral lichen planus [8]. Topografisk relasjon til tannrestaureringer, dvs. samsvar mellom hvor materialet sitter og hvor lesjonen oppstår, er kardinalfunnet ved orale lichenoide kontaktlesjoner og kan være til hjelp i det differensialdiagnostiske arbeidet (tabell 1). Kontaktlesjoner vil dermed vanligvis forekomme på den posteriore kinnslimhinnen eller på den laterale delen av tungen i direkte kontakt med tannrestaureringen. Oral lichen planus vil derimot oftest opptre bilateralt og omfatte større deler av munnslimhinnen (utover kontaktområdet), inkludert gingiva (ofte i form av deskvamativ gingivitt) [15]. Tilstedeværelse av eventuelle ekstraorale forandringer kan også være til hjelp for å skille oral lichen planus fra orale lichenoide kontaktlesjoner. Genitale slimhinneforandringer er hyppige blant kvinner med oral lichen planus og forekommer hos opptil 20% av pasientene [21]. Hudforandringer finnes hos 15% av pasientene med oral lichen planus [21]. Orale lichenoide kontaktlesjoner er derimot ikke assosiert med ekstraorale forandringer.
Orale lichenoide kontaktlesjoner |
Oral lichen planus |
|---|---|
|
Klinisk Unilateralt eller bilateralt Lesjoner i kontakt med tannrestaureringer Sjeldent gingivale lesjoner Kun lokalisert i munnslimhinnen Klinisk bilde kan variere over tid |
Bilateralt Lesjoner opptrer uavhengig av tannrestaureringer Gingivale lesjoner (ofte deskvamativ gingivitt) Kan ha ekstra-orale manifestasjoner Syklisk forløp med perioder av spontan remisjon |
|
Epikutantest med dentalserie Positiv hos de fleste |
Varierende resultat |
|
Histologisk Likt oral lichen planus, men noen ganger mer blandet, dypere og/eller mer diffust inflammasjonsinfiltrat. Germinalsenter-lignende strukturer |
Vakuolær degenerasjon av basalcellelaget og båndformet inflammasjonsinfiltrat subepitelialt som består hovedsakelig av T-lymfocytter. |
|
Respons etter fjerning av tannrestaurering Bedring/tilheling |
Ingen respons/noen ganger bedring* |
* Det kan ikke utelukkes at lesjoner av oral lichen planus forverres av en samtidig kontaktallergisk reaksjon og vil dermed vise noe bedring ved fjerning av tannrestaureringen [28].
De viktigste histologiske forandringer er karakterisert av vakuolær degenerasjon av basalcellelaget og båndformet inflammasjonsinfiltrat like subepitelialt (figur 3) [5]. Infiltratet består hovedsakelig av T-lymfocytter, men ved lichenoide kontaktlesjoner kan man iblant se et mer blandet inflammasjonsinfiltrat med plasmaceller samt noe dypere og mer diffus inflammasjon i lamina propria enn ved oral lichen planus (tabell 1) [22]. I tillegg kan en tidvis se dype perivaskulære lymfocyttinfiltrater og germinalsenter-dannelse ved kontaktlesjoner (figur 4) [23]. Det finnes dog ikke histologiske kriterier som kan skille mellom orale lichenoide kontaktlesjoner og oral lichen planus [23], og differensialdiagnosen baseres hovedsakelig på kliniske observasjoner [8]. Pasientene med orale lichenoide kontaktlesjoner og oral lichen planus utredes primært klinisk, særlig ved funn av klassiske retikulære forandringer. Det kan være aktuelt med biopsi og histologisk vurdering ved mistanke om malignitet eller ved et uklart klinisk bilde for å differensiere forandringene fra andre tilstander [7].
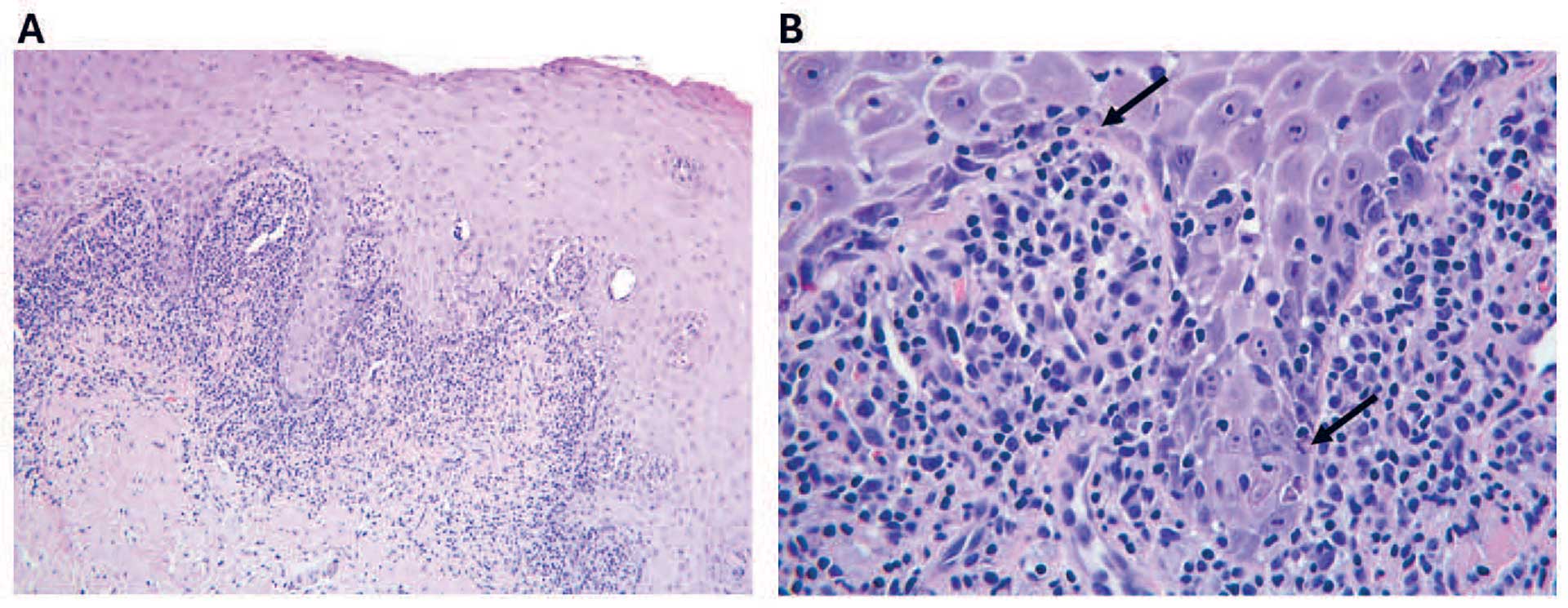
Figur 3. Lichen planus. Histopatologiske bilder fra kinnslimhinne som klinisk viste seg som retikulære hvite striper i hele kinnets utstrekning. A) Det ses et parakeratinisert overflateepitel. Like under epitelet ses et båndformet infiltrat av mononukleære betennelsesceller hvorav de fleste lymfocytter. Dypere deler av stroma er normalt. B) I et forstørret bilde ses spredte apoptotiske eosinofile celler i basalcellelaget (piler) samt intraepiteliale lymfocytter.
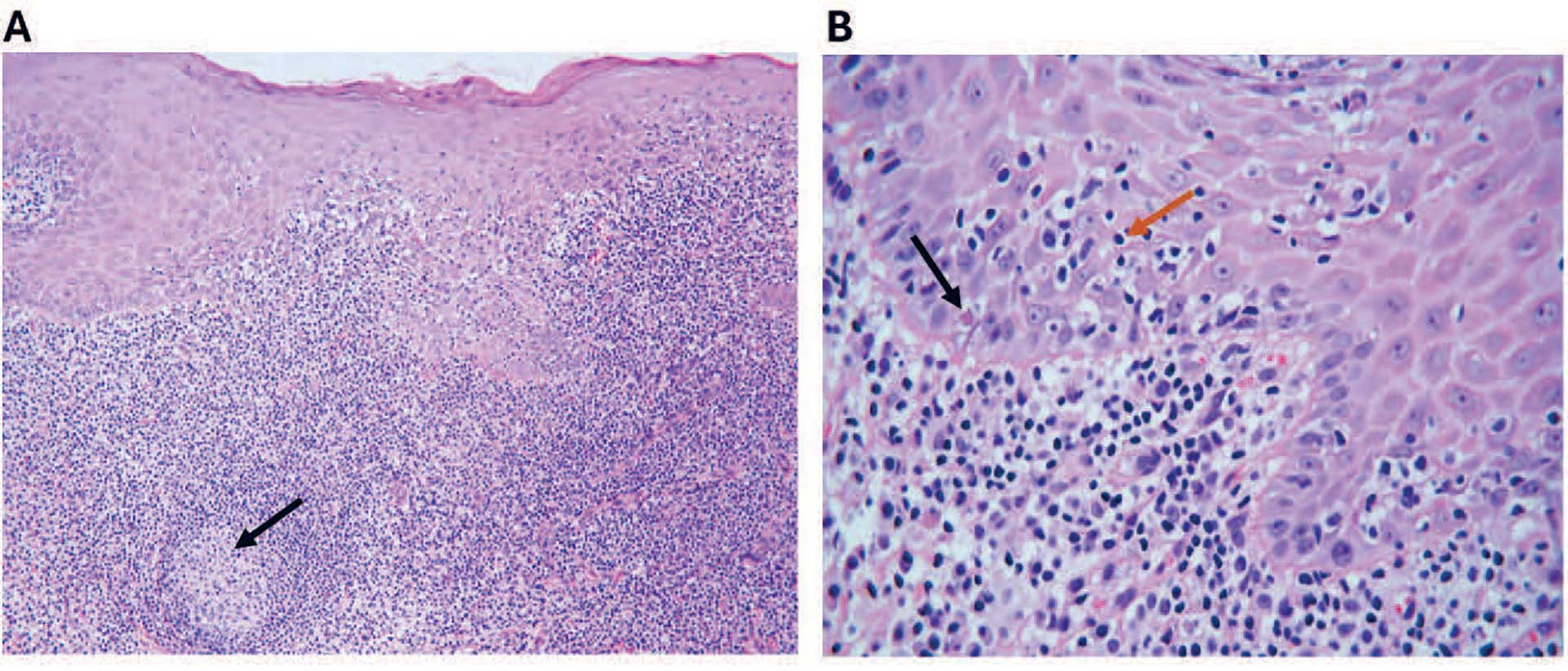
Figur 4. Lichenoid kontaktlesjon. Histopatologiske bilder fra klinisk homogen, hvitlig forandring fra kinnslimhinne med et tydelig rødt sentrum. Det opplyses om store amalgamfyllinger i kontakt med lesjonen. (A) Her ses vevsbit som på overflaten er kledd av et flerlaget plateepitel hvor det ses fortykket keratinlag superfisielt. Like under epitelet ses tett infiltrasjon av hovedsakelig mononukleære betennelsesceller (lymfocytter og plasmaceller) som også strekker seg til dypere deler av bindevesstroma. Det ses også dannelse av germinalsenter-lignende struktur (se pil). (B) I forstørret bilde ses apoptotiske eosinofile celler (svart pil) og lymfocytter i epitelet (oransje pil). Histopatologisk vurdering av forandring: Her ses et lichenoid reaksjonsmønster. Ut fra den kliniske beskrivelsen kan reaksjon på amalgamfyllinger være en mulighet. Dette kan histologisk ikke skilles fra lichen planus, men i foreliggende tilfelle ses utbredt betennelse med germinalsenter-dannelse som kan indikere at dette kan være knyttet til fyllingsmateriale heller enn lichen planus.
Tilheling av lesjonen etter utskifting av det aktuelle tannrestaureringsmaterialet er et viktig kriterium for å vurdere hvorvidt forandringen er forårsaket av restaureringsmaterialet (tabell 2) [24], og for å bekrefte diagnosen oral lichenoid kontaktlesjon. Ved manglende tilheling etter utskifting av restaureringsmateriale bør diagnosen revurderes.
Kasualitetsvurdering |
Kriterier* |
|---|---|
Sikker |
Uønsket reaksjon, med sannsynlig tidsforhold til tannbehandling Kan ikke forklares med sykdom, traume (for eksempel skarp fyllingskant) eller annen eksponering. Forbedring eller tilheling etter avbrutt eksponering (fjerning av tannrestaurering) Objektiv og spesifikk reaksjon Re-eksponering (rechallenge), om dette er forsvarlig, gir samme reaksjon. |
Sannsynlig |
Uønsket reaksjon, med rimelig tidsforhold til tannbehandling Reaksjonen kan mest sannsynlig ikke tilskrives sykdom, traume (for eksempel skarp fyllingskant) eller annen eksponering. Forbedring eller tilheling etter avbrutt eksponering (fjerning av tannrestaurering) |
Mulig |
Uønsket reaksjon, med rimelig tidsforhold til tannbehandling Kan også forklares med sykdom, traume (for eksempel skarp fyllingskant) eller annen eksponering. Informasjon om avbrutt eksponering kan være mangelfull eller uklar. |
Usannsynlig |
Uønsket reaksjon, med uklar tidsrelasjon til tannbehandling som gjør et forhold usannsynlig (men ikke umulig). Sykdom, traume eller annen eksponering gir plausible forklaringer. |
*Alle punkter (innen aktuell gruppering) bør i rimelig grad være oppfylt.
I tillegg til oral lichen planus er det viktig å være oppmerksom på flere aktuelle differensialdiagnoser med lignende klinisk bilde. Disse kan omfatte alt fra forandringer forårsaket av mekanisk traume (for eksempel en skarp fyllingskant) til lupus erythematosus, kronisk ulcerøs stomatitt og ikke-homogen leukoplaki.
Malignitetsrisiko
Det har lenge vært kjent at oral lichen planus er en potensielt malign tilstand, og malignitetsutviklingen er angitt til å være i gjennomsnitt 1,4% [25] [26]. Man er imidlertid usikker på om orale lichenoide kontaktlesjoner har risiko for malignitetsutvikling, og det er uenighet om dette. Noen studier viser at lichenoide forandringer generelt har lignende [26] eller til og med høyere risiko [25] for malignitetsutvikling sammenlignet med oral lichen planus, men definisjonen som er blitt brukt i disse studiene om lichenoide forandringer er svært vid og skiller ikke mellom orale lichenoide kontaktlesjoner og andre typer lichenoide forandringer. Disse studiene har likevel gitt grunnlag for at orale lichenoide forandringer, som en gruppe, er blitt inkludert blant de potensielt maligne tilstandene definert av Verdens helseorganisasjon (WHO) [6] [27].
Behandling
Nasjonale faglige retningslinjer fra Helsedirektoratet anbefaler at fyllinger i kontakt med orale lichenoide kontaktlesjoner fjernes og erstattes med et annet materiale [1]. Topografisk relasjon mellom munnslimhinneforandringer og restaureringsmaterialet, samt positiv epikutantest er de viktigste prediktorer for tilheling [13] [14] [28]. Forskning viser at pasienter som har positivt utslag på epikutantesting med kvikksølv har bedre prognose for tilheling etter amalgamfjerning sammenlignet med pasienter med negativ epikutantest [13] [14] [28].
Studier rapporterer likevel bedring eller tilheling av kontaktlesjonene etter fjerning av amalgam hos mange av pasientene med negativ epikutantest med kvikksølv [13] [14] [28] [29]. Grunnen kan være at andre komponenter i amalgam enn kvikksølv er årsaken til reaksjonen, eller at epikutantesting har lav sensibilitet, dvs. at sannsynligheten for falske negative resultater er stor [2]. En annen forklaring kan være at mekanismer av annen karakter enn kontaktallergi er årsaken til lesjonen, for eksempel toksiske mekanismer. Epikutantesting har dermed en begrenset diagnostisk verdi, og ifølge gjeldende retningslinjer er epikutantesting som regel ikke nødvendig hos pasienter med lichenoide kontaktlesjoner topografisk relatert til amalgamfyllinger [1]. Når det gjelder lichenoide forandringer i relasjon til andre materialer enn amalgam, er dermatologisk utredning med epikutantesting indisert [28]. Resultatet av epikutantest bør bedømmes i samarbeid med dermatolog også med tanke på klinisk relevans.
Svært få studier av pasienter som får fjernet amalgamfyllinger på grunn av orale lichenoide kontaktlesjoner har direkte sammenlignbare kontrollgrupper. Det er også viktig å være oppmerksom på at studiene mangler randomisering, noe som kan bidra til overestimering av tilheling [15]. Det sykliske forløpet av sykdommen tas sjeldent i betraktning. Studiene har ofte for kort oppfølgingstid til å kunne registrere et mulig tilbakefall av lesjoner etter amalgamfjerning [15].
Forskning støtter derfor ikke rutinemessig fjerning av amalgamfyllinger uten at disse er i kontakt med forandringene. Det skal foreligge klare indikasjoner for en slik behandling, og tannlegen bør alltid veie fordeler og ulemper [30]. Fjerning av amalgam kan føre til ytterligere tap av tannsubstans og kan by på restaureringsutfordringer. Det er også en risiko for forverring av kontaktlesjoner de nærmeste dagene etter utboring av amalgam [16] eller eksponering for innholdsstoffer med påfølgende forbigående økning i kvikksølvkonsentrasjonen i urin [31], særlig ved manglende bruk av kofferdam. Pasienten bør dermed involveres i beslutningen. Ved uttalte symptomer fra kontaktlesjonen er det enklere å ta stilling til behandlingsvalg, men i asymptomatiske tilfeller kan pasienten være mindre motivert for å skifte ut restaureringene.
Om pasienten til tross for symptomer velger å beholde tannrestaureringer som mistenkes være årsak til kontaktlesjonen, kan en forsøksvis bruke kortikosteroider lokalt etter behov for å oppnå symptomkontroll. Dette er et etablert behandlingsopplegg for oral lichen planus [32], men det finnes ikke evidens for at en slik behandling virker på pasienter med orale lichenoide kontaktlesjoner. Eliminasjon av skarpe kanter, polering av gamle fyllinger, optimalisering av munnhygiene og bruk av tannkrem uten sodium lauryl sulfate kan også bidra til å lindre symptomer [2] [15] [33].
Oppfølging med fotodokumentasjon er anbefalt pga. mulig malignitetsrisiko. Som nevnt tidligere, er det sterk uenighet om denne risikoen er reell, og det finnes ingen studier som undersøker om fjerning av tannrestaureringer reduserer risikoen for malignitetsutvikling [34]. Vi mangler evidens for oppfølgingsbehov og kontrollintervaller, men klinisk skjønn tilsier at en kan bruke samme oppfølgingsregime som for oral lichen planus, nemlig årlige kontroller eller hyppigere kontroller ved behov. Ved mistanke om malignitet skal tannlegen henvise til utredning i relevant spesialisthelsetjeneste [1]. Tannlegen bør også vurdere behovet for henvisning til spesialist ved manglende eller ufullstendig tilheling etter behandling.
Bidrag fra folketrygden
I henhold til gjeldende regler kan Folketrygden yte bidrag til utskifting av tannrestaureringsmaterialer ved «Allergiske reaksjoner mot tannrestaureringsmaterialer» på grunnlag av kontaktlesjoner i munnslimhinner [35]. Tannlegen må kunne dokumentere at munnslimhinneforandringene mest sannsynlig ikke skyldes en bakenforliggende sykdom. Oppdatert helseskjema kan benyttes som dokumentasjon for dette. I tillegg skal tannlegen rapportere til Bivirkningsgruppen for odontologiske biomaterialer ved utfylling og innsending av skjema «Rapportering av uønskede reaksjoner/bivirkninger hos brukere i forbindelse med odontologiske materialer» (bivirkningsgruppen.norceresearch.no), jf. takst 10 [35].
Konklusjon
Orale lichenoide kontaktlesjoner forårsaket av odontologiske biomaterialer forekommer relativt sjeldent, men kan gi opphav til betydelige plager hos pasienten. Ettersom det ved lichenoide forandringer kan være liknende kliniske og histologiske funn som ved oral lichen planus eller andre tilstander, bør tannlegen utrede mulige differensialdiagnoser og ha oppdatert klinisk kunnskap om oral lichen planus og orale lichenoide forandringer for å kunne gi nødvendig informasjon og veiledning til pasientene. Epikutantesting har sine begrensninger og er indisert i enkelte tilfeller. Utskifting av restaureringene som er i kontakt med lichenoide kontaktlesjoner gir bedring eller tilheling av lesjonene hos de fleste pasientene, men dette kan ta opptil flere måneder. Denne behandlingen kan være omfattende i noen tilfeller, og fordeler og ulemper bør diskuteres med pasienten i forkant. Det er også viktig å være oppmerksom på at orale lichenoide kontaktlesjoner kan ha en risiko for malignitetsutvikling. Oppfølging og tverrfaglig samarbeid mellom allmenntannleger og spesialisthelsetjenesten er dermed essensielt.
Opphavsrett og anonymisering av bildene
Figur 1 er utformet av manuskriptets forfattere. Figur 2A og 2B viser pasientbilder tatt av manuskriptets forfattere. Det er ikke mulig å kjenne igjen pasienten ut fra bilde, bildetekst eller annen tilhørende tekst. Figur 3 og 4 viser histologiske bilder tatt av manuskriptets forfattere. Det er ikke mulig å kjenne igjen pasienten ut fra bilde, bildetekst eller annen tilhørende tekst.
Referanser
Helsedirektoratet. Retningslinjer for utredning og behandling ved mistanke om bivirkninger fra odontologiske biomaterialer (IS-1481). Oslo: Helsedirektoratet 2008.
Jontell M, Dahlgren U. Allergiska reaktioner och andra biverkningar. Nor Tannlegeforen Tid. 2005; 115: 106-12.
Alnæs M, Storaas T, Björkman L, Vindenes H, Brudevoll S. Anafylaksi etter endodontisk behandling. Nor Tannlegeforen Tid. 2020; 130: 326-30.
Braun JJ, Zana H, Purohit A, Valfrey J, Scherer P, Haïkel Y, et al. Anaphylactic reactions to formaldehyde in root canal sealant after endodontic treatment: four cases of anaphylactic shock and three of generalized urticaria. Allergy. 2003; 58: 1210-5.
Pinkus H. Lichenoid tissue reactions. A speculative review of the clinical spectrum of epidermal basal cell damage with special reference to erythema dyschromicum perstans. Arch Dermatol. 1973; 107: 840-6.
Warnakulasuriya S, Kujan O, Aguirre-Urizar JM, Bagan JV, González-Moles MÁ, Kerr AR, et al. Oral potentially malignant disorders: A consensus report from an international seminar on nomenclature and classification, convened by the WHO Collaborating Centre for Oral Cancer. Oral Dis. 2021; 27: 1862-80.
Al-Hashimi I, Schifter M, Lockhart PB, Wray D, Brennan M, Migliorati CA, et al. Oral lichen planus and oral lichenoid lesions: diagnostic and therapeutic considerations. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2007; 103 Suppl:S25.e1-12.
Carrozzo M, Porter S, Mercadante V, Fedele S. Oral lichen planus: A disease or a spectrum of tissue reactions? Types, causes, diagnostic algorhythms, prognosis, management strategies Periodontol 2000. 2019; 80: 105-25.
Schlosser BJ. Lichen planus and lichenoid reactions of the oral mucosa. Dermatol Ther. 2010; 23: 251-67.
McParland H, Warnakulasuriya S. Oral lichenoid contact lesions to mercury and dental amalgam--a review. J Biomed Biotechnol. 2012; 2012:589569.
Pentenero M, Broccoletti R, Carbone M, Conrotto D, Gandolfo S. The prevalence of oral mucosal lesions in adults from the Turin area. Oral Dis. 2008;14: 356-66.
Reinhart JP, Stoopler ET, Crawford GH. Oral hypersensitivity reaction. Dermatol Clin. 2020; 38: 467-76.
Thornhill MH, Pemberton MN, Simmons RK, Theaker ED. Amalgam-contact hypersensitivity lesions and oral lichen planus. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2003; 95: 291-9.
Suter VG, Warnakulasuriya S. The role of patch testing in the management of oral lichenoid reactions. J Oral Pathol Med. 2016; 45: 48-57.
Baccaglini L, Thongprasom K, Carrozzo M, Bigby M. Urban legends series: Lichen planus. Oral Dis. 2013; 19: 128-43.
Issa Y, Duxbury AJ, Macfarlane TV, Brunton PA. Oral lichenoid lesions related to dental restorative materials. Br Dent J. 2005; 198: 361-6.
Thyssen JP, Linneberg A, Menné T, Johansen JD. The epidemiology of contact allergy in the general population – prevalence and main findings. Contact Dermatitis. 2007; 57: 287-99.
Tvinnereim HM, Lundekvam BF, Berge ME, Morken T, Björkman L. Kontaktallergisk reaksjon overfor dentalt gull – kasuspresentasjon. Nor Tannlegeforen Tid. 2004; 114: 400-1.
Blomgren J, Axell T, Sandahl O, Jontell M. Adverse reactions in the oral mucosa associated with anterior composite restorations. J Oral Pathol Med. 1996; 25: 311-3.
Bäckman K, Jontell M. Microbial-associated oral lichenoid reactions. Oral Dis. 2007; 13: 402-6.
Eisen D. The evaluation of cutaneous, genital, scalp, nail, esophageal, and ocular involvement in patients with oral lichen planus. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 1999; 88: 431-6.
Lodolo M, Gobbo M, Bussani R, Torelli L, Rupel K, Ottaviani G, Poropat A, Biasotto M. Histopathology of oral lichen planus and oral lichenoid lesions: An exploratory cross-sectional study. Oral Dis. 2023; 29: 1259-68.
Thornhill MH, Sankar V, Xu X-J, Barrett AW, High AS, Odell EW, et al. The role of histopathological characteristics in distinguishing amalgam-associated oral lichenoid reactions and oral lichen planus. J Oral Pathol Med. 2006; 35: 233-40.
World Health Organization- Uppsala Monitoring Center (WHO-UMC). The use of the WHO-UMC system for standardised case causality assessment [nettdokument] (5 juni 2013). Tilgjengelig fra https://www.who.int/publications/m/item/WHO-causality-assessment.
Iocca O, Sollecito TP, Alawi F, Weinstein GS, Newman JG, De Virgilio A, et al. Potentially malignant disorders of the oral cavity and oral dysplasia: A systematic review and meta-analysis of malignant transformation rate by subtype. Head Neck. 2020; 42: 539-55.
González-Moles MÁ, Ramos-García P. An evidence-based update on the potential for malignancy of oral lichen planus and related conditions: a systematic review and meta-analysis. Cancers (Basel). 2024; 16: 608. doi: 10.3390/cancers16030608.
Muller S, Tilakaratne WM. Update from the 5th edition of the World Health Organization classification of head and neck tumors: Tumours of the oral cavity and mobile tongue. Head Neck Pathol. 2022; 16: 54-62.
Rahat S, Kashetsky N, Bagit A, Sachdeva M, Lytvyn Y, Mufti A, et al. Can we separate oral lichen planus from allergic contact dermatitis and should we patch test? A systematic review of chronic oral lichenoid lesions. Dermatitis. 2021; 32: 144-50.
Issa Y, Brunton PA, Glenny AM, Duxbury AJ. Healing of oral lichenoid lesions after replacing amalgam restorations: a systematic review. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2004; 98: 553-65.
Fletcher R, Harrison W, Crighton A. Dental material allergies and oral soft tissue reactions. Br Dent J. 2022; 232: 620-5.
Håheim LL, Lygre GB, Dalen K, Eide R, Karlsson S, Lyngstadaas SP, et al. Effekt av utskifting av amalgamfyllinger ved symptomer og sykdom som relateres til amalgamfyllinger. Nor Tannlegeforen Tid. 2007; 117: 878-82.
Lodi G, Manfredi M, Mercadante V, Murphy R, Carrozzo M. Interventions for treating oral lichen planus: corticosteroid therapies. Cochrane Database Syst Rev. 2020; 2: CD001168.
Bankvall M, Dabelsteen E, Holmstrup P, Johannessen AC, Jontell M, Neppelberg E, et al. Common oral mucosal lesions. Nor Tannlegeforen Tid. 2024; 134: 126-38.
Kerr AR, Lodi G. Management of oral potentially malignant disorders. Oral Dis. 2021; 27: 2008-25.
Helsedirektoratet. Rundskriv til folketrygdloven § 5-6, § 5-6 a og § 5-25 – undersøkelse og behandling hos tannlege og tannpleier for sykdom og skade [nettdokument]. Oslo: Helsedirektoratet (sist faglig oppdatert 01. januar 2024). Tilgjengelig fra https://www.helsedirektoratet.no/rundskriv/folketrygdloven-kap-5/rundskriv-til-folketrygdloven--5-6--5-6-a-og--5-25--undersokelse-og-behandling-hos-tannlege-og-tannpleier-for-sykdom-og-skade.
English summary
Oral lichenoid contact lesions – an overview
Oral lichenoid contact lesions are relatively uncommon but can cause significant pain and morbidity. They are thought to be caused by a localized hypersensitivity reaction to dental restorative materials, mainly mercury released from amalgam. This overview aims to give an insight into the etiopathogenesis and clinical and histological features of oral lichenoid contact lesions, as well as suggest an approach to differential diagnosis. Management strategies and prognosis are summarized. Further, this review addresses the controversial issue of malignant potential of oral lichenoid contact lesions, and the need for patient follow-up and collaboration with specialized health care professionals.
Aliko A, Berge TLL, Skarstein K, Bergstø A, Lundekvam BF, Björkman L. Orale lichenoide kontaktlesjoner – en oversikt. Nor Tannlegeforen Tid. 2024;134:830-7. doi:10.56373/2024-10-6
Korresponderende forfatter: Ardita Aliko, e-post: aral@norceresearch.no
Akseptert for publisering 21.08.2024
Artikkelen er fagfellevurdert
Artikkelen siteres som: Aliko A, Berge TLL, Skarstein K, Bergstø A, Lundekvam BF, Björkman L. Orale lichenoide kontaktlesjoner – en oversikt. Nor Tannlegeforen Tid. 2024; 134: 830-7.
MeSH: lichenoid eruptions; oral lichen planus; dental materials; adverse effects; mouth diseases.
Artikkelen er fagfellevurdert.
Artikkelen siteres som:
Aliko A, Berge TLL, Skarstein K, Bergstø A, Lundekvam BF, Björkman L. Orale lichenoide kontaktlesjoner – en oversikt. Nor Tannlegeforen Tid. 2024;134:830-7. doi:10.56373/2024-10-6
