Xenia Hermann, Jette Daugaard-Jensen, Jakob Sonne Lempert, Marie-Louise Milvang Nørregaard, og Nuno Vibe Hermann
Emaljedysplasi eller dentinanomali?
Overtandlæge og leder, Odontologisk Landsdels- og Videncenter, Rigshospitalet, København
Tandlæge, M.S., Odontologisk Landsdels- og Videncenter, Rigshospitalet, København
Tandlæge, Tand-, Mund- og Kæbekirurgisk Klinik, Hoved-Orto-Centeret, Rigshospitalet, København
Afdelingstandlæge, studielektor, Sektion for Pædodonti, Institut for Odontologi og Oral Sundhed, Aarhus Universitet, Aarhus
Lektor, tandlæge, dr.odont. ph.d., Pædodonti og Klinisk Genetik, Odontologisk Institut, Københavns Universitet
Klinisk relevans
De hyppigst forekommende genetisk betingede afvigelser i tanddannelsen er amelogenesis imperfecta og dentinogenesis imperfecta, hvor dannelsen af henholdsvis emalje og dentin er blevet forstyrret. For afvigelser gælder, at både den primære og permanente dentition er afficeret, men med stor variation i fænotyper og behandlingsbehov. Det er bl.a. klinisk udfordrende, at kvaliteten af vævene kan være forringet, hvorved en basal egenskab som fx bindingsstyrken mellem tand og en restaurering også er nedsat. Dette betyder nedsat holdbarhed og højere omlavningsrate hos disse patienter og risiko for højere cariesprævalens. Det er derfor nødvendigt med særlig profylaktisk opmærksomhed. Det er vigtigt at kende til de forskellige typer af afvigelser for at kunne iværksætte optimal forebyggelse og relevant tandbehandling og vurdere, om henvisning til specialiseret oral rehabiliterende behandling er nødvendig.
Denne artikel omhandler genetisk betingede misdannelser af emalje eller dentin, hhv. amelogenesis imperfecta og dentinogenesis imperfecta. Ætiologi og diagnose af typiske tandforandringer, som ses ved sygdommene, gennemgås. Artiklen omhandler desuden beskrivelse af relevante dele af sundhedsloven, henvisningspraksis med relevans for området samt aktuelle anbefalinger for så vidt angår den forebyggende og rekonstruktive tandbehandling hos børn og unge med disse tilstande.
Tanddannelsesforstyrrelser kan have mangeartede udtryk og former, og de kan have såvel genetisk som miljøinduceret oprindelse eller en kombination heraf. De mest almindeligt forekommende rent genetisk betingede tanddannelsesforstyrrelser er amelogenesis imperfecta (AI) og dentinogenesis imperfecta (DI), hvor dannelsen af henholdsvis emalje og dentin er afvigende. Da der er tale om genetiske sygdomme, betyder det, at samtlige tænder er afficeret i såvel det primære som det permanente tandsæt.
Hos den enkelte patient optræder AI oftest mildest i det primære tandsæt og ses mere udtalt i den permanente dentition, mens det omvendte billede gør sig gældende for DI [1]. For begge tanddannelsessygdomme gælder det, at der ses stor variation i fænotyper og behandlingsbehov.
Da emalje er af ektodermal oprindelse, er det vigtigt at være opmærksom på, at AI-lignende emaljeforandringer kan være et symptom på mere generelle sygdomme eller syndromer i kroppens ektodermalt deriverede væv. I modsætning til emaljen dannes dentinen fra ektomesenkymet, og forandringer i dentinen kan derfor være tegn på knoglesygdommen osteogenesis imperfecta.
Forekomsten af AI i Danmark er ikke kendt, men skønnes at være 0,125 pr. 1.000 individer [2]; svenske studier fra 1980’erne finder en forekomst på 0,3 pr. 1.000 [3] i Midtsverige og 1,4 pr. 1.000 i Nordsverige [4]. Den forøgede prævalens i Nordsverige tilskrives demografiske faktorer. DI er tidligere rapporteret med en hyppighed i USA på 1 pr. 6.000 til 1 pr. 8.000 individer [5], men en nyere svensk landsdækkende registrering af DI type II, der kun medfører ændringer i tænderne, viser en langt mindre forekomst på 2,2 pr. 100.000 personer pr. år [6].
AI nedarves autosomalt dominant, autosomalt recessiv eller X-bundet, mens DI følger en autosomalt dominant arvegang. Nye mutationer kan opstå indenfor begge tanddannelsesanomalier. Den optimale behandling af AI og DI starter typisk tidligt i barnealderen og fortsætter livslangt.
Det er derfor intentionen med nærværende artikel at klæde klinikeren på til relevant diagnostik, henvisningspraksis og behandlingsmuligheder.
Tanddannelsen
Første tegn på tanddannelse ses i 7. fosteruge. I et samspil mellem slimhinden (ektodermen), grundsubstansen (ektomesenkymet) og neuroektodermen uddifferentieres de kronedannende celler (odontoblaster og ameloblaster) styret af signalmolekyler BMP, FGF, SHH og WNT og talrige transkriptionsfaktorer, herunder Pax-9, Runx2 og Msx-1, som de mest undersøgte [7] [8] (Fig. 1).

Fig. 1. Tanddannelsens forskellige stadier, og hvordan disse reguleres af forskellige signalveje (7).
Efter dentindannelsen er påbegyndt, begynder emaljedannelsen, og når kronedannelsen er afsluttet, dannes cement og parodontalmembran. Roddentinen, cementen og parodontalmembranen dannes af henholdsvis odontoblaster, cementoblaster og fibroblaster. Overordnet dannes tanden fra cuspides og mod rodspids.
Mineraliseringen af de primære tænder starter omkring 14.-16. fosteruge, og krone-/roddannelsen af de primære tænder er afsluttet omkring treårsalderen. Kort tid efter fødslen begynder mineraliseringen af permanente incisiver, hjørnetænder og førstemolarer, og alle tænder er færdigdannede i 12-14-årsalderen bortset fra 3.-molarer, der afslutter roddannelsen i 18-25-årsalderen [9].
Dentindannelsen – dentinogenesen
Dentinen dannes af odontoblaster, uddifferentieringen starter fra incisalkant eller kusptop og forløber derfra i apikal retning. Odontoblasterne secernerer organisk prædentin matrix, der omdannes til mineraliseret dentin bestående af hydroxylapatit 70 %, organisk materiale 20 % og vand 10 %. Den organiske del består hovedsageligt af type 1 kollagen 85 % og nonkollagene proteiner [10], hvor dentin sialophosphoprotein (DSPP) er dominerende og antages at have stor betydning for den tidlige dannelse og mineralisering af dentinen [11]. Efter den primære dentindannelse fortsætter odontoblasterne med dannelse af sekundær dentin ind mod pulpa, hvilket over tid resulterer i reduceret størrelse af pulpa cavum. Ved ydre påvirkninger i form af fx traumer, slid eller caries kan odontoblasterne danne reparativ dentin som beskyttelse af pulpa. Mere end 40 mutationer i DSPP er kendt, men selve dentinogenesens forløb er endnu ikke fuldstændigt belyst [12].
Emaljedannelsen – amelogenesen
Emaljedannelsen kan kort opdeles i fire faser: Sekretionsfasen, hvor organisk emaljematrix secerneres af emaljedannende ameloblaster. Emaljematrix indeholder emaljeproteiner (amelogenin 90 % og 10 % ameloblastin, enamelin og tuftelin), enzymer og 30 % mineral, der aflejres i lag, der svarer til emaljens tykkelse. I mineraliseringsfasen udskiller ameloblasterne hydroxylapatit, der erstatter det organiske materiale. Herefter følger modningsfasen, hvor emaljeproteinerne fjernes vha. enzymer, og emaljens hårdhed øges. Afslutningsvis sker hypermineralisering af emaljens overflade; tandens form er fastlagt, og emaljen opnår fuld hårdhed som kroppens hårdeste væv. Til slut ses ameloblasterne som det reducerede emaljeepitel, der forsvinder, når tanden erupterer. Emaljen kan ikke gendannes senere i livet [13].
Afhængigt af hvilken fase i amelogenesen der bliver påvirket, vil dette medføre karakteristisk forandring af emaljen i form af mindre tykkelse eller varierende hårdhed/kvalitet. Der differentieres derfor mellem såkaldte kvantitative forandringer, kvalitative forandringer og blandingstyper.
Ætiologi og diagnostik ved emaljedysplasi og dentinanomali
Amelogenesis imperfecta
AI har tidligere været klassificeret i to overordnede kliniske undergrupper, en hypoplastisk type (kvantitativ defekt) og en hypomineraliseret type (kvalitativ defekt). Den kvantitative defekt ved hypoplastisk AI kan have karakter af et generelt udtyndet, glat emaljelag – eller en meget lokaliseret udtynding, som giver pitting – eller en uensartet udtynding af emaljelaget, så tandoverfladen fremstår ujævn med sløring af normale kronekonturer. Den kvalitative defekt ved AI findes i to hovedvarianter, henholdsvis hypocalcificeret og hypomatureret type. Ved hypocalcificeret hovedgruppe ses den ringeste mineralisering af emaljen blandt de tre hovedgrupper. Ved frembrud fremstår tanden med normal mængde emalje vurderet i henhold til størrelse og form, mens farven typisk er opak, gullig-brunlig, og overfladen fremstår ru. Efter eruption ses en hurtig nedbrydning af emaljen (især okklusalt/incisalt), idet emaljen er blød pga. højt proteinindhold og reduceret grad af mineralisering, og tænderne er temperaturfølsomme. Radiologisk observeres manglende kontrast mellem emalje og dentin.
Ved hypomatureret hovedgruppe ses en reduceret, men dog bedre mineralisering sammenlignet med hypocalcificeret hovedgruppe. Ved frembrud har tanden normal størrelse og form. Efter eruption ses som ved den hypocalcificerede hovedgruppe også en nedbrydning af emaljen efter eruption (især okklusalt/incisalt). Farven af emaljen er opak, hvidlig-brunlig. Radiologisk kan der differentieres mellem emalje og dentin.
Kortlægning af genetikken for AI har imidlertid ført til beskrivelse af 15 forskellige undergrupper baseret på fænotype, kliniske særpræg og arvelighed [14]. De nyeste klassificeringer af de forskellige undertyper baserer sig mere på genetikken end på kliniske fund, og disse findes derfor mindre anvendelige i klinikken [15] [16]. Klinisk inddeles i den hypoplastiske samt de to hypomineraliserede typer; den hypomineraliserede og den hypomaturistiske samt blandingstyper med taurodonti. Denne kliniske inddeling har stor betydning for valg af behandling.
Arvegangen for AI kan være autosomalt dominant, som er den hyppigste, autosomalt recessiv eller X-bundet (5 %). Sporadiske mutationer kan ligeledes forekomme i de gener, som kontrollerer amelogenesen. I familier med X-bundet AI ses fænotypisk forskel mellem kvinder og mænd. Hos kvinder ses sund og hypoplastisk og/eller hypomineraliseret emalje veksle i lodrette striber hen over tandoverfladen. Dette kaldes »lyonization« og forklares ved, at der hos kvinder tidligt i fosterstadiet sker en inaktivering af det ene af de to X-kromosomer i alle kvindens celler [17], hvilket betyder, at nogle celler med et aktivt X-kromosom danner normal emalje, mens andre celler med et inaktivt X-kromosom danner dysplastisk emalje.
Dentinogenesis imperfecta
Arvelige dentinanomalier opdeles i dentindysplasi (DD) og dentinogenesis imperfecta (DI), Shields klassifikation fra 1973 [18]. DD opdeles i typerne DD-1 og DD-2, mens DI opdeles i tre undergrupper baseret på fænotypen: DI-I, DI-II og DI-III. Den første, DI-I, ses i forbindelse med knoglesygdommen osteogenesis imperfecta, mens DI-II og DI-III er isoleret til tandsættet (DI-III er kun fundet hos en enkeltstående amerikansk familie). Ved DI type 1 er der tale om en dentinanomali forårsaget af defekt i kollagenproteinet pga. mutation i genet COLIA1 eller COLIA2, mens DD og DI type 2 er forårsaget af defekt i sialoprotein pga.mutation i DSPP-genet. Identifikation af sialophosphorproteingenet (DSPP) har betydet, at man i dag ved, at dentindysplasi type II, DI-II og DI-III har samme genetiske baggrund og skyldes mutationer i netop dette gen. De tre anomalier kan betragtes som samme sygdom med stigende alvorlighedsgrad [19]. Den hyppigst forekommende dentinanomali, DI-II, nedarves autosomalt dominant. Emaljen i DI-II er beskrevet som værende normal i struktur og mineralindhold [20], mens den underliggende dentin er dysplastisk og irregulær, hvilket kan være medvirkende til affrakturering af emaljen og blotlæggelse af dentinen, hvorved der er risiko for udtalt slid og pulpal eksponering [12] [21].
Diagnosen for AI eller DI stilles på baggrund af anamnestiske oplysninger, kliniske og røntgenologiske fund. Spørgsmål, der kan føre til diagnosen, er fx: Er tilstanden kendt i familien? Er tandform og farve afvigende i hele tandsættet? Er tænderne følsomme for koldt/varmt? Viser røntgenbilleder afvigende roddannelse, eruptionsanomali eller retention af tænder? Se desuden skematisk gennemgang i Skema 1. Diagnosen stilles ofte af kompetente børnetandlæger eller efter henvisning til et af de to odontologiske landsdels- og videncentre, hvor et multidisciplinært team står for udredningen. Herefter vil der blive lagt en behandlingsplan, og såfremt behandlingen vurderes mulig i kommunal tandpleje, foretages der skriftlig rådgivning til denne. I tilfælde af behov for højtspecialiseret behandling varetages behandlingen enten i den højtspecialiserede behandlingsenhed på Institut for Odontologi og Oral Sundhed i Aarhus eller på Rigshospitalet i København i samarbejde med Tandlægeskolen. Selvom patienten er i højtspecialiseret behandling, er fortsatte status- og fokusundersøgelser samt sygdomsforebyggende og sundhedsfremmende tiltag i kommunal tandpleje/egen tandlæge af afgørende betydning. Derfor bliver behandlingen af denne patientgruppe ofte et samarbejde mellem videncentrene og egen tandlæge. Genetisk udredning er for nuværende ikke et standardtilbud, medmindre den dentale anomali ses som led i medicinsk grundmorbus. I fremtiden vil det givet blive mere anvendt.
Tandbehandling, behandlingsmæssige udfordringer – patienttilfredshed og sygdomsforebyggende tiltag
Hos patienten med AI er de største tandrelaterede problemer typisk dårlig æstetik, hypersensitivitet samt affrakturering eller nedslidning af emalje og deraf følgende tab af tyggefunktion [22]. Endvidere er det vigtigt at være opmærksom på, at AI i visse tilfælde er associeret med eruptionsforstyrrelser og anormal kæbevækst i form af frontalt åbent bid [23] [24]. DI-patienters hovedproblemer er dårlig æstetik og nedslidning af tænder med risiko for hæmmet tyggefunktion og reduceret ansigtshøjde.
Tandbehandlingen hos patienter med AI og DI er ofte omfangsrig og livslang, og afhængigt af de kliniske manifestationer og alderen på patienten behandles tænderne med stålkroner, kompositplast, facader, kroner eller anden rehabiliterende behandling evt. i kombination med ortodontisk og/eller kirurgisk behandling [22]. En tilbagevendende klinisk udfordring er, at holdbarheden af behandlinger, som omfatter kompositplast, generelt er nedsat. Dette skyldes, at bindingsstyrken afhænger af emaljens mineraliseringsgrad, som for de hypomineraliserede og hypomaturerede typer er forringet. Femårs overlevelsen af fyldninger kan derfor hos patienter med AI være reduceret med op til 50 % [25], dog med store inter-individuelle forskelle afhængigt af AI-type [26] [27]. Hos hypomineraliserede typer er der endvidere i mindre studier vist risiko for højere forekomst af caries [28] [29], hvorfor man bør være ekstra opmærksom vedrørende profylaktiske behandlingsstrategier i denne gruppe. Studier viser ligeledes, at personer med AI oplever en negativ indvirkning på deres livskvalitet, foruden at håndteringen og behandlingen heraf er tidkrævende og omkostningstung [30] [31] [32].
Behandling af det primære tandsæt
Allerede i tidlig barnealder er det vigtigt at være opmærksom på særlige forhold i tandsættet hos patienter med AI og DI. Hos patienter med AI er det primære tandsæt oftest lettere afficeret, evt. med behov for behandling af æstetisk og smertedækkende art.
Hos patienter med DI vil der ofte ved den første undersøgelse i 1½-2-årsalderen være behov for behandling. Mindre emaljefrakturer kan dækkes med kompositplast, så dentinen ikke er blottet, nedslidning forhindres, og bidhøjden opretholdes. Nedslidning af de primære tænder vil medføre kraftigt slid på førstemolarerne straks efter eruptionen. Det er vigtigt at være opmærksom på, at nedslidningen går ekstra hurtigt i det primære tandsæt, og manglende mulighed for retention af restaureringen kan forventes, hvis behandling udskydes for længe.
Ved behandling af den unge barnepatient er det uanset diagnose vigtigt at vægte hurtigt udførte og holdbare løsninger. Således varetages barnets tarv bedst muligt for opnåelse af optimal funktion og smertefrihed i relation til den psykiske modenhed for modtagelse af tandbehandling. Stålkroner anbefales stadig som den bedste langtidsprovisoriske behandling af primære molarer. Funktion og plads i tandbuen opretholdes, omlavningsfrekvensen er lav, og ofte fungerer stålkronen, til tanden fældes. Stålkronerne kan i de fleste tilfælde cementeres over de primære molarer uden brug af præparation/ ekskavering, lokalbedøvelse eller anden forberedelse af tanden. Metoden var oprindelig udviklet til behandling af omfattende cariesangreb i primære molarer uden forudgående ekskavering og omtales oftest i litteraturen som Hall teknik [33]. Ved tænder med lav kronehøjde, som der ofte er tale om ved AI og DI, vil der dog ofte blive behov for en modificering af den oprindelige Hall teknik. Modificeringen vil bestå i, at man tilpasser den præfabrikerede stålkrone i højden. Der vil også være tilfælde, hvor anvendelsen af konventionelle præfabrikerede stålkroner ikke er gunstig, fx hvis der i forvejen er tendens til anteriort åbent bid. I tilfælde hvor stålkroner ikke findes muligt, kan der som alternativ anvendes printede stålkroner. Disse er teknikerfremstillede efter scanning, alternativt konventionelt aftryk.
Ved behov for lindring af hypersensitivitet, mindre restaurering eller ved afvigende morfologi i form af pits eller ru/ujævn overflade kan forseglinger med flowplast være hensigtsmæssigt. Er behandlingen omfattende/langvarig, bør behovet for sedation og omfanget af denne overvejes. Behandling under anvendelse af lattergas/dinitrogenoxid (N2O) kan være en hjælp for mange patienter i denne alder.
Stålkroner og Hall teknik
Evt. separation med separationselastik ved tæt approksimal kontakt.
Udvælgelse af korrekt størrelse stålkrone.
Stålkronen cementeres med kemisk hærdende glasionomer cement.
Stålkronen trykkes helt på plads, hvorefter barnet evt. kan holde trykket ved at bide på en vatrulle.
Cementoverskud fjernes.
Evt. bidhævning efterlades (forsvinder spontant efter 2-4 uger).
Behandlingen af det unge permanente og voksne tandsæt
I det unge permanente tandsæt behandles i høj grad med de samme metoder og teknikker som i det primære tandsæt. Patienterne er endnu psykisk for umodne til meget langvarige behandlinger, og pulpa i tænderne er endnu meget stor, hvilket øger risikoen for accidentiel perforation ved omfattendepræparation. Stålkronebehandling eller opbygning i kompositplast er derfor stadig et godt klinisk valg hos disse patienter. Hypersensitive, men ikke restaureringskrævende tænder kan behandles med forsegling evt. i form af flowplast. Hos patienter med DI kan bidskinne om natten i visse tilfælde hjælpe til at reducere sliddet.
I takt med at patienten bliver ældre og dermed i stand til at samarbejde om mere behandlingstunge løsninger, kan der på individuel vurdering og indikation behandles med facader og kroner. Undersøgelser viser stor sammenhæng mellem den orale livskvalitet og holdbarhed med samtidig æstetisk tilfredsstillende løsninger [30] [31].
Betragtninger vedr. kompositplast som valg til restaurering af det især unge/yngre tandsæt
Når der ses større afvigelser i tandfarve, morfologi og/eller tandstilling samt involvering af samtlige tænder, er behandlingsplanlægningen naturligt mere omfattende og udfordrende. Behandlingsvalget er og har traditionelt været omfattende med meget præparationskrævende protetiske løsninger i form af multiple, heldækkende indirekte restaureringer, hvor der forventes god langtidsholdbarhed [22].
I disse år sker imidlertid en konstant udvidelse af kompositplasts indikationsområde, såvel i forhold til bindingsevne, slidstyrke, farvestabilitet og dækevne. En veludført kompositopbygning kan derfor være både æstetisk og langtidsholdbar og ikke mindst tandsubstansbesparende i forhold til en mere konventionel præparation. Hos unge og yngre patienter vil sidstnævnte vægte tungt, da pulpa cavum stadig er stort. Patienten forventes at skulle bruge sit tandsæt mange år endnu, og det bør derfor overvejes at vælge kompositplast, hvor dette overhovedet er muligt.
Behandlingsvalget bør altid tage udgangspunkt i en individuel samlet vurdering. Vurderingen foretages i forhold til tandsættets samlede tilstand, patientens alder, modenhed samt subjektive ønsker og behov. Det er en stor fordel, at man ved anvendelseaf kompositplast har så store reparationsmuligheder i forhold til fx metalkeramiske eller fuldkeramiske protetiske løsninger.
Overordnede mål for behandling af AI og DI
Diagnosticerer tilstanden tidligt og lægger behandlingsplaner, der både kortsigtet og langsigtet tager udgangspunkt i patientens subjektive og objektive behov.
Orienterer forældre og patient grundigt om tandsygdommen, behandlingens forløb og om vigtigheden af god mundhygiejne. Det årelange behandlingsforløb kræver et godt samarbejde med barn og familie.
Opretholder normale vertikale og horisontale dimensioner i det primære og permanente tandsæt.
Reducerer risiko for pulpakomplikationer, bevarer god tyggefunktion samt forebygger og minimerer slid.
Minimerer smerte og ubehag samt forebygger udviklingen af tandlægeangst.
Lytter til patientens skiftende ønsker og behov til tændernes udseende – det gælder også i barneårene.
Sygdomsforebyggelse og sundhedsfremme
Da AI og DI er medfødte lidelser, som i sig selv øger risikoen for omfattende behandlingsbehov og i nogle ubehandlede tilfælde forventes at føre til varig funktionsnedsættelse, er det vigtigt, at der ud over de protetiske behandlinger også varetages relevant sygdomsforebyggelse og sundhedsfremme. Der er tale om faktorer i tandsættet, der ikke kan ændres på (ej heller efter fuld protetisk behandling), hvorfor samtlige patienter bør kategoriseres med øget sygdomsrisiko (risikovurderes i rødt spor). De bør derfor tilses til fokuseret undersøgelse med professionel afpudsning hver 3. måned. Ved behov bør der modtages instruktioner for at sikre optimal mundhygiejne [4].
Når det drejer sig om barneårene, vurderes tillid og tryghed vigtigt, hvorfor det anbefales, at barnet som udgangspunkt følger samme behandler og ikke ses af mange forskellige.
Cariesforebyggelse er pga. flere faktorer hensigtsmæssig. Da tændernes overflade kan fremstå ru, og renhold kan være vanskeligt for patienten, kan der suppleres med regelmæssige fluoridpenslinger (evt. med 2 % NaF). Ved afvigende morfologi i form af pits eller ru/ujævn overflade kan forseglinger med flowplast være hensigtsmæssigt.
Forebyggelse af slid: Som tidligere nævnt er stålkroner fortsat en optimal behandling i såvel det primære som det permanente tandsæt frem til mulighed for andet kronevalg. Derudover kan det i nogle tilfælde blive nødvendigt med en form for bidskinne, såfremt der findes kooperation til dette, og at en sådan skinnebehandling ikke påvirker væksten. Ligeledes vil relevant bidhævning i form af ortodontisk behandling også i sig selv have en forebyggende effekt. Vedligeholdelse er essentielt, og såvel direkte som indirekte restaureringer vil have behov for mindre og større reparationer og genbehandlinger.
Kliniske eksempler
Patienttilfælde 1 – Fig. 2
12-årig pige med amelogenesis imperfecta, hypomineraliseret type. Patienten er henvist til Odontologisk Landsdels- og Videncenter, Rigshospitalet, som femårig, hvor de primære tænder ses gullige/brunlige og med moderat grad af slid, ikke kun okklusalt og incisalt, men også på facialfladerne pga. Markant forringet kvalitet af emaljen. Ved frembrud af de permanente tænder ses misfarvning af emaljen og kort efter posteruptivt breakdown. Plastopbygning af tænderne krævede stor grad af accept, og det foreløbige behandlingsresultat var tilfredsstillende for patienten. Der vil løbende være behov for vedligehold pga. relativt dårlig binding mellem restaurering og tand. En mere permanent og æstetisk mere tilfredsstillende behandling er indirekte teknikerfremstillede kompositkroner, der forventes at kunne fremstilles med minimal præparation, når frembruddet er afsluttet.
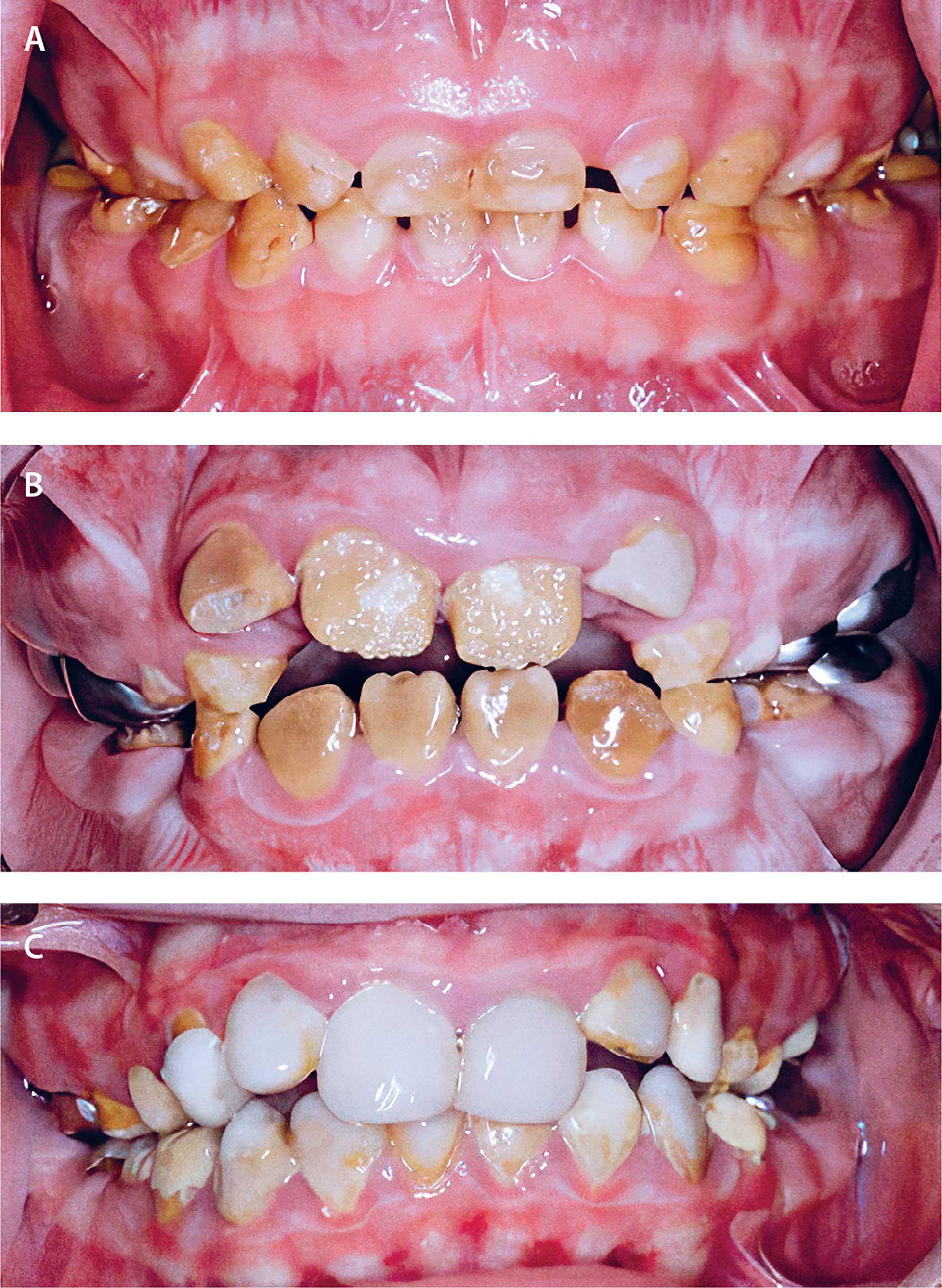
Fig. 2. A. 5 år. Det primære tandsæt ses mindre afficeret end det permanente. Der ses udtalt slid, og pt. klager over følsomme tænder.
B. 8 år. Det permanente tandsæt ses mere afficeret end det primære. Tænderne fremtræder med posteruptivt breakdown, den mørkere dentin fremtræder tydeligt. Følsomhed og farvefremtoning er til stor gene for patienten.
C. 10 år: Tænderne er beskyttet mod temperaturpåvirkninger med direkte plastopbygninger i den intermediære behandlingsfase. Når kooperation og frembrud tillader det, stiles efter heldækkende teknikerfremstillede plastkroner med ingen/minimal præparation, hvorved den ofte mere præparationskrævende behandling udskydes længst muligt.
Patienttilfælde 2 – Fig. 3
19-årig pige med amelogenesis imperfecta, blandingstype. Patienten har igennem barne- og ungdomsår kun modtaget behandling af førstemolarer. Indikationen for igangsætning af behandling er æstetik, sensibilitet og reduktion af bidhøjden. For at fastlægge okklusion, bidhøjden og tandstørrelse opbygges tandsættet i fræsede polymethylmethacrylat-kroner (PMMAkroner). Fremtidig behandling forventes at være konvertering af PMMA kroner/bro til minimalt præparerede kroner.
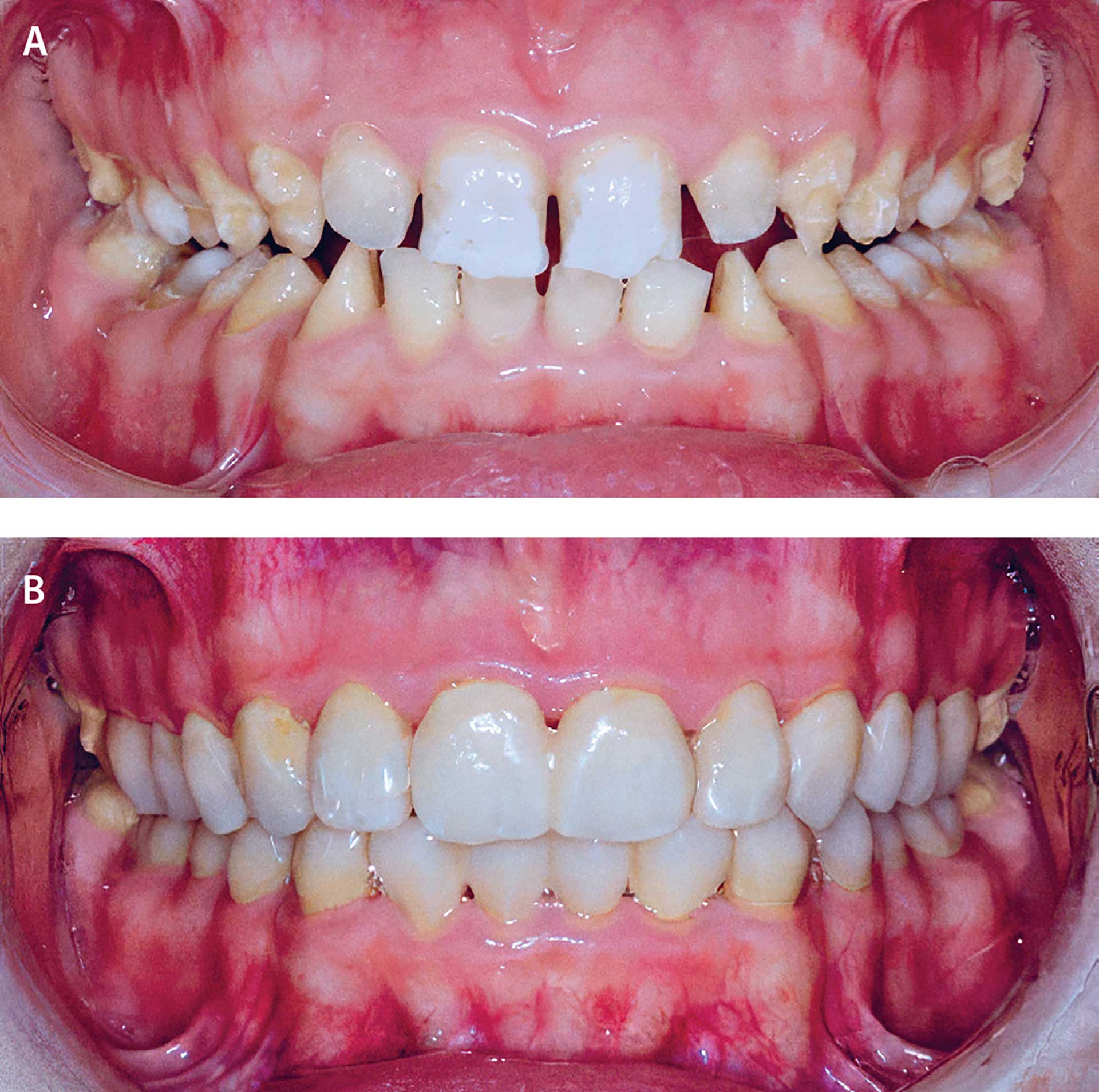
Fig. 3. A. 18 år: Tænderne er følsomme, misfarvede og malformerede, æstetisk utilfredsstillende for patienten.
B. 18 år. Langtids temporær opbygning af tandsættet med fræsede PMMA-broer uden præparation. Bemærk normalisering af tandstørrelse, facon og gode skyllerum.
Patienttilfælde 3 – Fig. 4
16-årig dreng med amelogenesis imperfecta, hypomaturationstype. Den tydelige misfarvning af tænderne har været til stor belastning for patienten. Det er kendt, at blegning af disse tænder ikke vil have den store effekt, men i visse tilfælde give øget termofølsomhed. Der er foretaget plastopbygninger forat dække misfarvninger. Fremtidig behandlingsplan er kroner posteriort og facader anteriort.
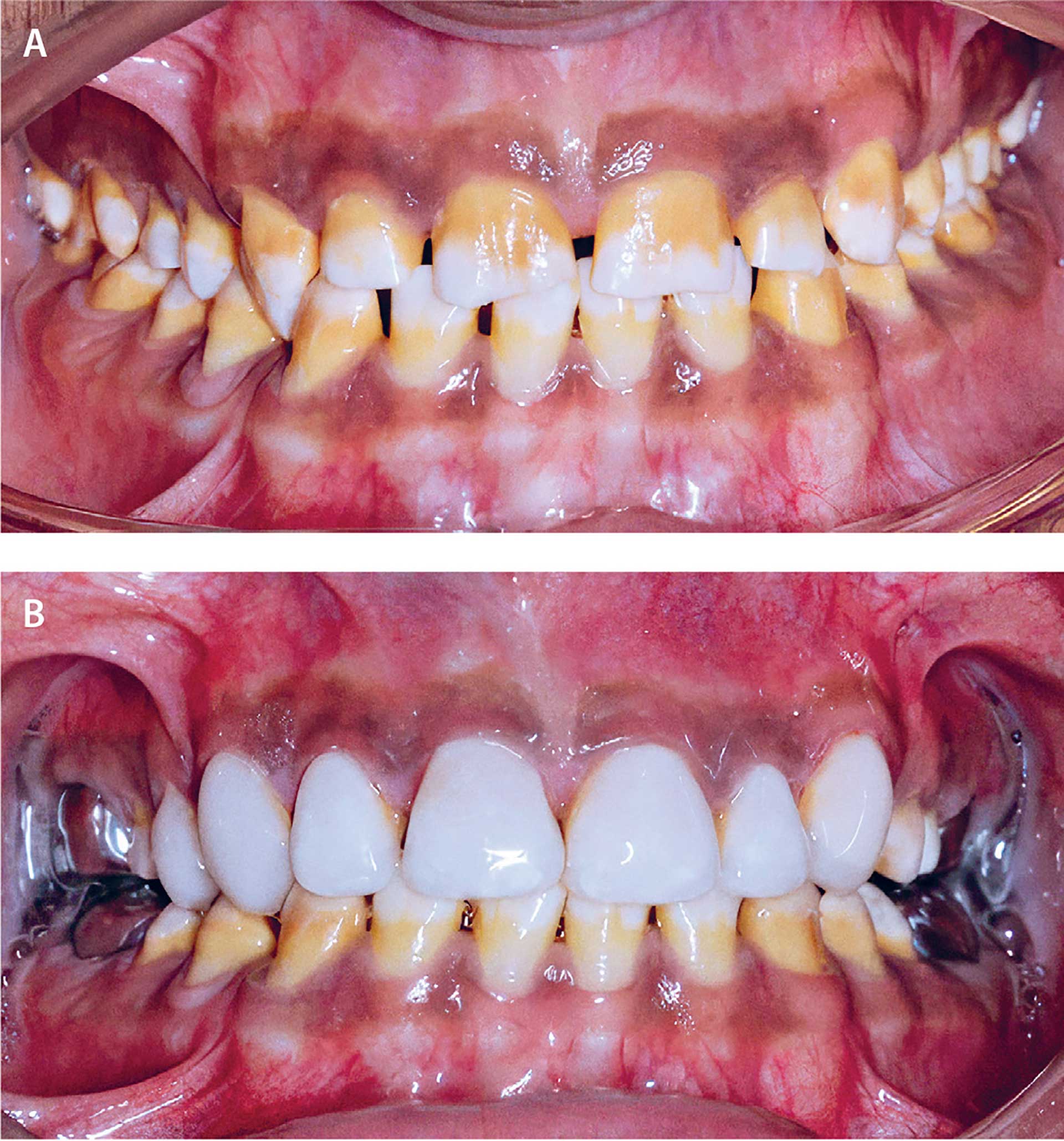
Fig. 4. A. 11 år. Emaljen ses med hvide og brunlige opaciteter. Farvefremtoningen af tænderne generer patienten.
B. 15 år. Direkte kompositopbygninger i OK, stålkroner på 6+6 og 6-6, giver for nuværende tilfredsstillende æstetik og funktion.
Patienttilfælde 4 – Fig. 5
Kvinde kendt med dentinogenesis imperfecta. Patienten blev behandlet på specialklinik for oral rehabilitering på Odontologisk Institut i København og blev i 15-årsalderen henvist til Odontologisk Landsdels- og Videncenter, Rigshospitalet. Løbende behandlet med plast og stålkroner. I 28-årsalderen behandlet med lithium dicilicat (E.max) kroner i overkæbefronten. Molarer og præmolarer er restaureret med fuldzirkonkroner og kompositopbygninger.
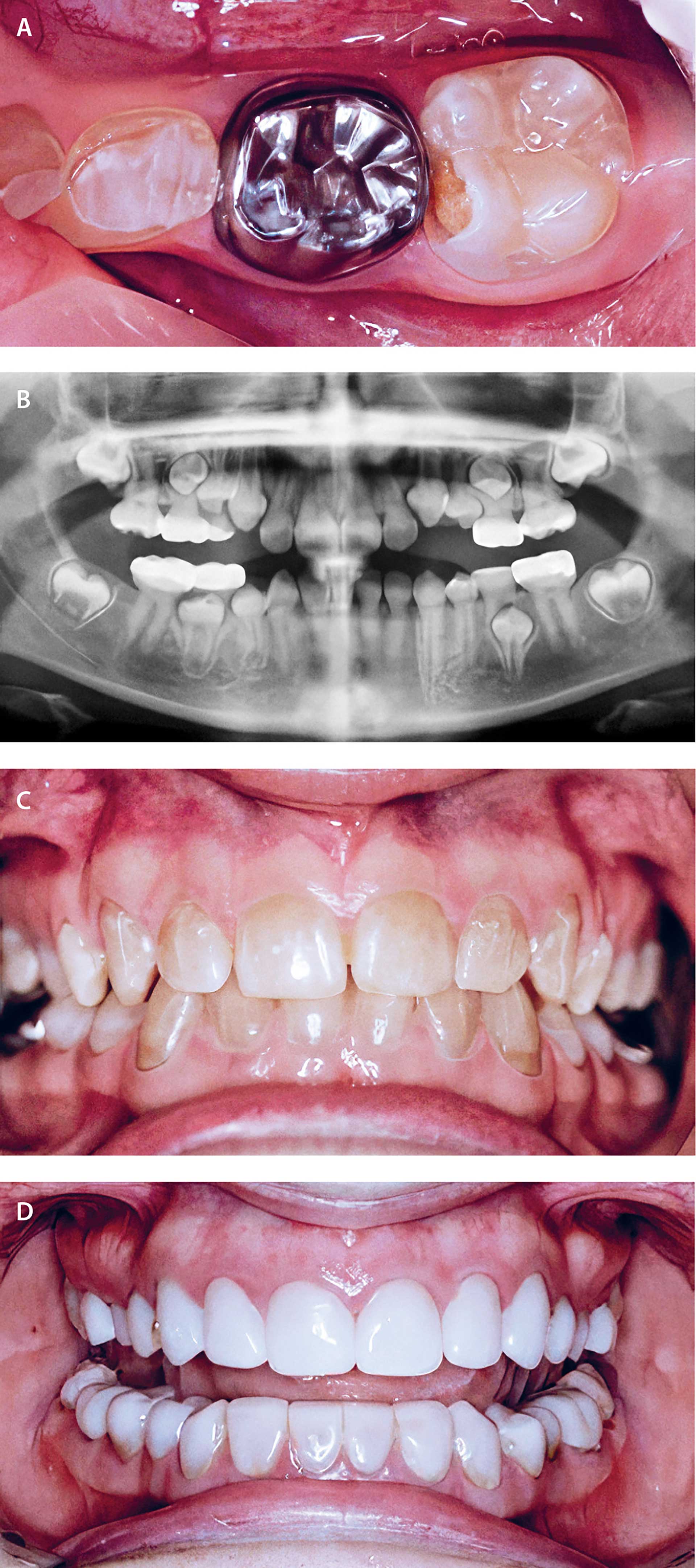
Fig. 5. A. 9 år. Der ses komposit overdækket -04, gennemslidt stålkrone -05, -6 posteruptivt breakdown.
B. 10 år. Buttede kroner med cervikal konstriktion, spinkle radices.
C. 15 år. Den mørke farve er patientens primære problem.
D. 28 år. Lithium disilicat- (E.max) kroner 321+123, monolitisk zirkonkroner molarer, plastopbygninger ved præmolarer og i underkæbefronten.
Sundhedsloven og henvisningspraksis
I 2020 udkom en ny udgave af sundhedsloven, men heri henvises fortsat til »Tillæg til vejledning om omfanget af og kravene til den kommunale og regionale tandpleje, 2012« [34], når det gælder håndtering af patienter med komplicerede former af tanddannelsesforstyrrelser. I tillægget beskrives specifikt, hvor patienter med tandproblemer relateret til AI og DI skal behandles, og hvorledes de viderehenvises ved behov. Såfremt patienten hører under børne- og ungdomstandplejen (0-21 år), skal patienten behandles i dette regi. I de tilfælde, hvor barnet eller den unge, der er omfattet af børne- og ungdomstandplejen, har behov for specialiseret tandlægelig behandlingsplanlægning og evt. behandling, skal han/hun henvises til regionstandplejen. Såfremt der ydermere er behov for højt specialiseret behandling, skal regionstandplejen viderehenvise til et af de to odontologiske landsdels- og videncentre.
Da der er tale om sjældne medfødte sygdomme og tilstande, der i henhold til bilaget i Sundhedsstyrelsens retningslinjer kan disse henvises direkte til de odontologiske landsdels- og videncentre for vurdering og/eller behandling.
For voksne patienter udskrevet af børne- og ungetandplejen gælder sundhedsloven § 166 stk. 3, som angiver, at tilskud til tandbehandling »udelukkende gives til de dele af patientens orale behandlingsbehov, som har årsagssammenhæng med sygdommen/tilstanden«.
Af positivt kan nævnes, at tilskudsordningen for patienter med omfattende odontologiske følger af medfødte lidelser i dag i langt større grad end tidligere respekterer anvendelse af plastopbygning som semipermanent løsning/langtidsprovisorium, så længe det er funktionelt og æstetisk muligt, hvilket er essentielt for behandlingsvalget og langtidsoverlevelsen af patientens tandsæt.
Tandkronen |
Farve |
Røntgen |
Pulpale forandringer |
|||
|---|---|---|---|---|---|---|
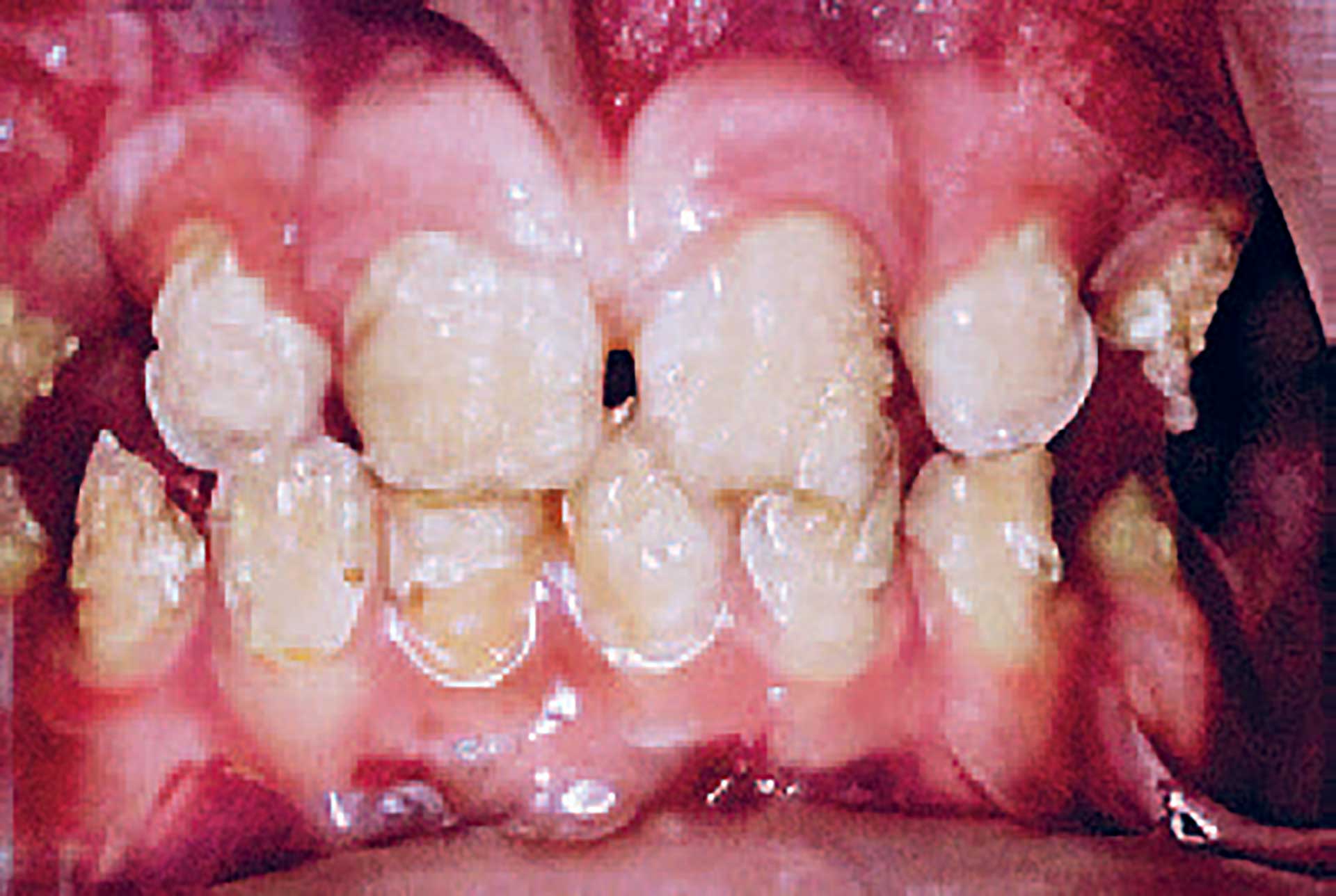 |
AI-hypoplastisk Afvigelse i sekretionsfasen Emaljetykkelsen Er reduceret Kvantitativ defekt |
Tydelig ændret morfologi i form af tynd glat emalje eller ujævn/ ru med lokale pits. Overfladen er hård ved sondering. |
Gullig idet dentinen skinner igennem den tynde emalje |
Normal kontrast. Tynd eller ujævn emalje. |
Taurodonti kan ses i visse typer |
Skeletalt åbent bid hos ca. 50 %. Termo-følsomhed Forsinket eruption eller retention |
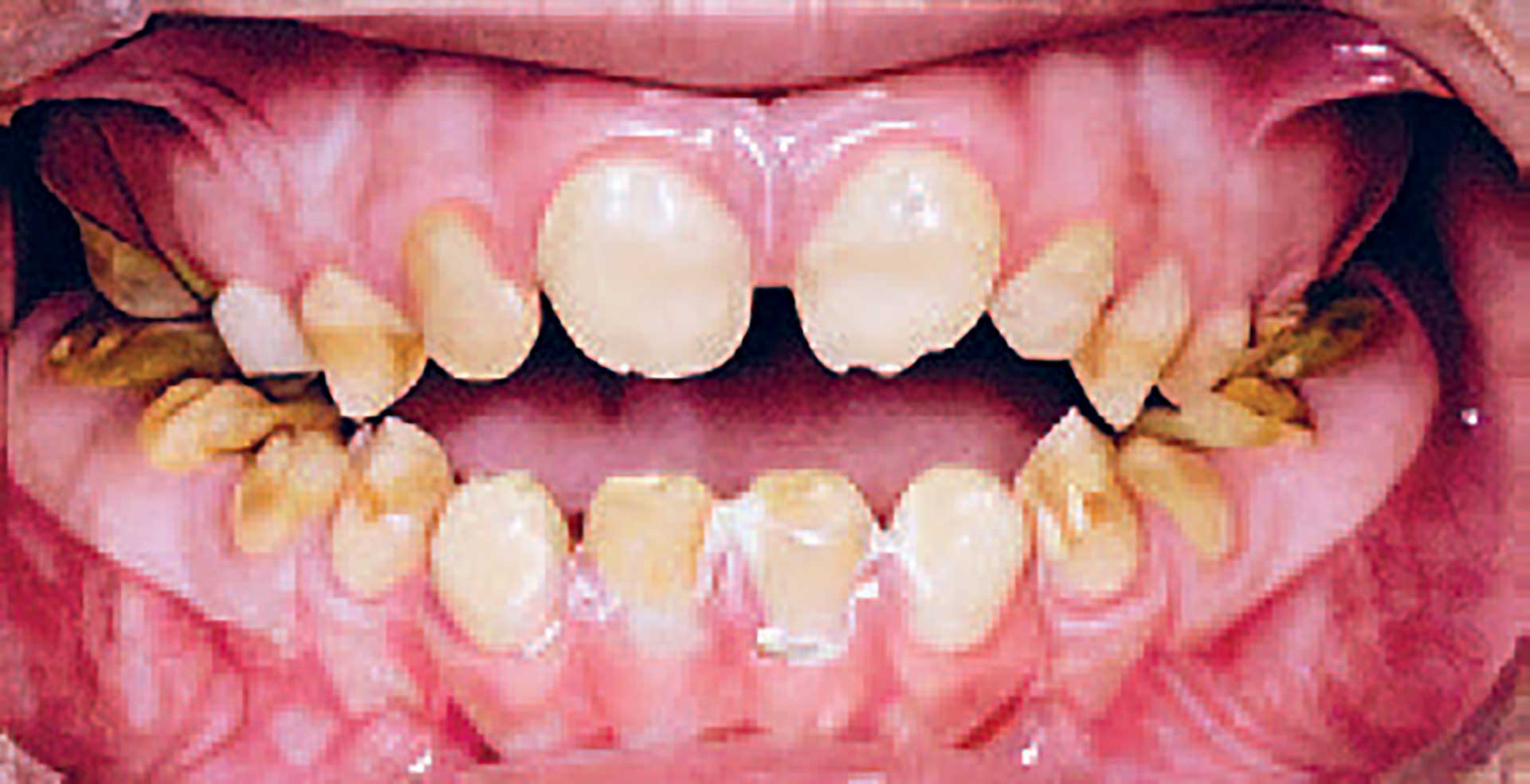 |
AI-hypomineralisation Afvigelse i mineraliseringsfasen Kvalitativ defekt |
Normal form ved eruption – blød emalje, kan nærmest »skrabes« af. |
Opak gullig-brunlig |
Ingen kontrast |
Skeletalt åbent bid. Forsinket eruption eller retention Udtalt termo-følsomhed. Calculus |
|
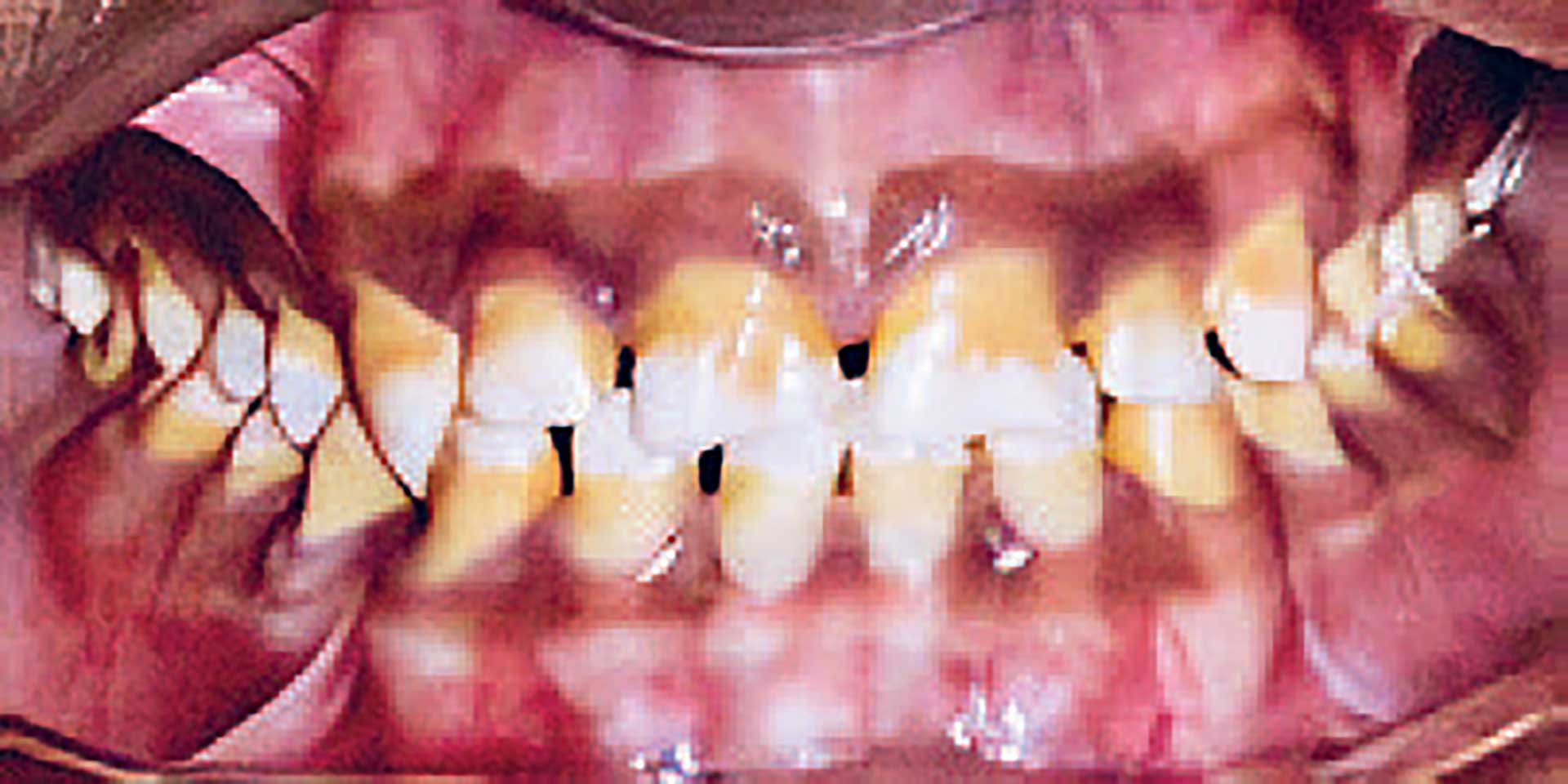 |
AI-hypomaturation Afvigelse i modningsfasen Kvalitativ defekt |
Normal form ved eruption. Hårdhed af emaljen er let reduceret, overfladen ujævn |
Opak, mere hvidlig evt. gullig-brune opaciteter |
Redu-ceret kontrast |
Termofølsomhed - Øget risiko for attrition |
|
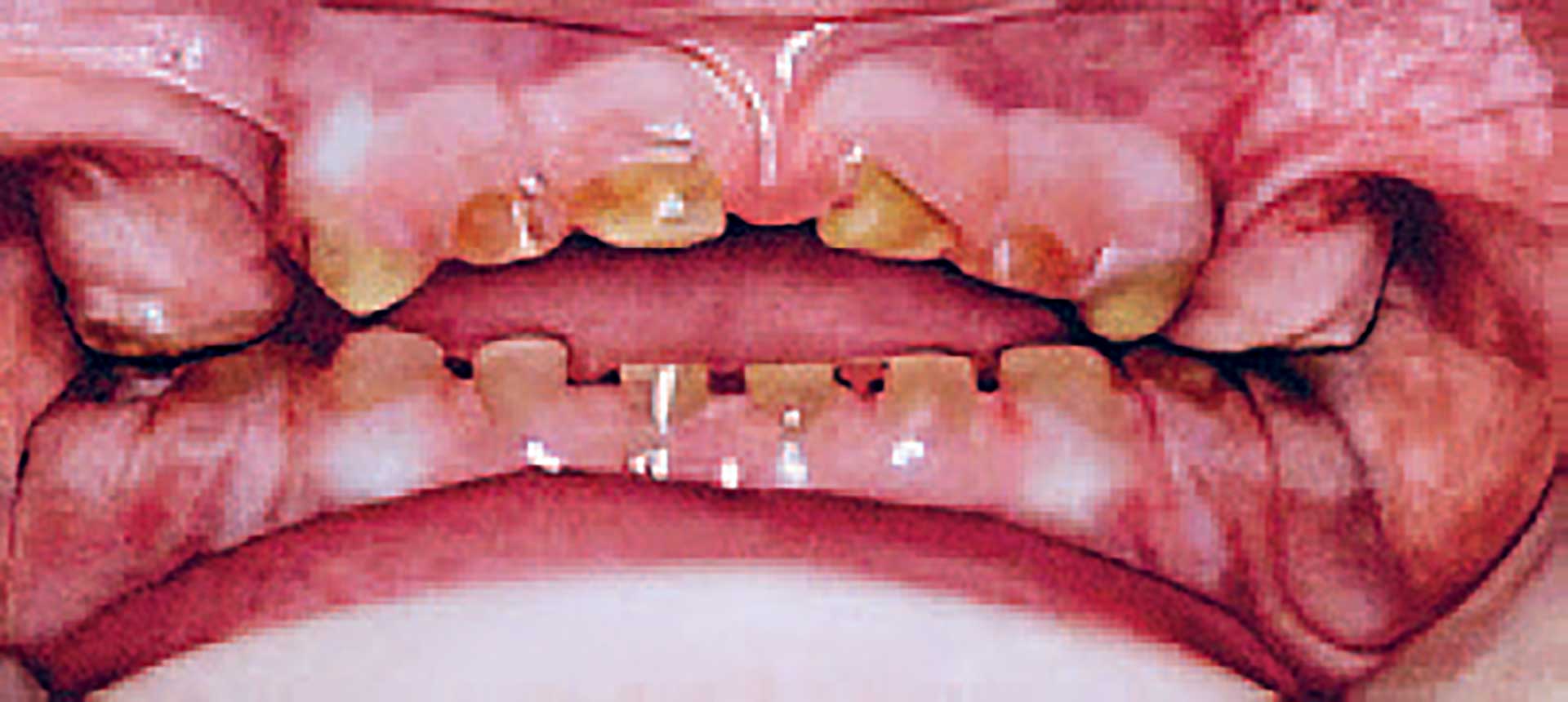 |
DI type II Abnorm dentindannelse Kvalitativ defekt |
Buttet form, med cervical indsnøring. |
Brunlig- grålig- blålig Uden emalje er tænderne gullig-brune |
Normal kontrast |
Før eruption ses store pulpae, efter eruption ses obliteration af pulpa cavum. Gracile rødder |
I nogle tilfælde tidligt tandskifte |
Sammenfatning
AI og DI er ofte omfattende og behandlingskrævende tilstande med behov for interdisciplinær håndtering samt livslangt vedligehold og behandling. Patienter med AI eller DI vil ofte kræve vurdering gennem regionstandplejen eller et af de odontologiske landsdels- og videncentre. Nogle patienter med AI eller DI vil være berettiget til behandling finansieret af regionstandplejen, andre vil have behov for højtspecialiseret behandling gennem et af de to odontologiske landsdels- og videncentre. For voksne patienter med AI eller DI vil man kunne søge tilskud gennem tilskudsordningernes § 166 stk. 3, hvis det kan dokumenteres, at et betydeligt behandlingsbehov ses som følge af den medfødte dentale anomali.
Patienterne med AI eller DI modtager ligesom alle andre patienter det almindelige basale tandplejetilbud i primærsektoren. Tandlæger i primærtandplejen har derfor behov for at kende til forebyggende tiltag, henvisningspraksis og behandlingsmuligheder.
Litteratur
Espelid I, Haubek D, Jälevik B. Developmental defects of the dental hard tissues and their treatment. In: Kock G, Poulsen S, eds. Pediatric dentistry. A clinical approach. 3rd ed. Oxford: Wiley-Blackwell, 2017;275-82.
Jakobsen C, Skou R, Hertz JM et al. Amelogenesis imperfecta: Gener, proteiner og faenotyper En oversigtsartikel. Tandlægebladet. 2013;7:574-82.
Sundell S. Hereditary amelogenesis imperfecta. An epidemiological, genetic and clinical study in a Swedish child population. Swed Dent J. (Supl.) 1986;31:1-38.
Bäckman B, Holm AK. Amelogenesis imperfecta: prevalence and incidence in a northern Swedish county. Community Dent Oral Epidemiol. 1986;14:43-7.
Witkop CJ Jr. Hereditary defects of dentin. Dent Clin North Am. 1975;19:25-45.
Andersson K, Malmgren B, Åström E et al. Dentinogenesis imperfecta type II in Swedish children and adolescents. Orphanet J Rare Dis. 2018;13:145-52.
Thesleff I. The genetic of tooth development and dental defects. Am J Med Genet Part A. 2006;140:2530-5.
Gadhia K, McDonald S, Arkutu N et al. Amelogenesis imperfecta: An introduction. Br Dent J. 2012;212:377-9.
Kock G, Kreiborg S, Andreasen JO. Erupting and shedding of teeth. In: Kock G, Poulsen S, eds. Pediatric dentistry. A clinical approach. 3rd ed. Oxford: Wiley-Blackwell, 2017;40-53.
Nancy A. Dentin-Pulp Complex. In: Ten Cate’s oral histology: development, structure and function. 9th ed. A. St. Louis, Missouri, USA: Elsevier, 2018;157-92.
Jing Z, Chen Z, Jiang Y. Effects of DSPP gene mutations on periodontal tissues. Glob Med Genet .2021;8:90-4.
Taleb K, Lauridsen E, Daugaard- Jensen J et al. Dentinogenesis imperfecta type II – genotype and phenotype analyses in three Danish families. Mol Genet Genomic Med. 2018;6:339-49.
Nancy A. Enamel: composition, formation and structure. In: Ten Cate’s oral histology: Development, structure and function. 9th ed. A. St.Louis, Missouri, USA: Elsevier, 2018;339-49.
Witkop CJ Jr. Amelogenesis imperfecta, dentinogenesis imperfecta and dentin dysplasia revisited: problems in classification. J Oral Pathol. 1988;17:547-53.
Aldred MJ, Savarirayan R, Crawford PJM. Amelogenesis imperfecta: A classification and catalogue for the 21st century. Oral Dis. 2003;9:19-23.
Crawford PJM, Aldred M, Bloch- Zupan A. Amelogenesis imperfecta. Orphanet J Rare Dis 2007;2:17-28.
Lyon MF. X-chromosome inactivation and human genetic disease. Acta Paediatr. Suppl 2002;91: 107-12.
Shields ED, Bixler D, el-Kafrawy AM. A proposed classification for heritable human dentine defects with a description of a new entity. Arch Oral Biol. 1973;18:543-53.
de La Dure-Molla M, Philippe Fournier B, Berdal A. Isolated dentinogenesis imperfecta and dentin dysplasia: Revision of the classification. Eur J Hum Genet. 2015;23:445-51.
Malmgren B, Lundberg M, Lindskog S. Dentinogenesis imperfecta in a six-generation family. A clinical, radiographic and histologic comparison of two branches through three generations. Swed Dent J. 1988;12:73-84.
Hart PS, Hart TC. Disorders of human dentin. Cells Tissues Organs. 2007;186:70-7.
Sabandal MMI, Schäfer E. Amelogenesis imperfecta: review of diagnostic findings and treatment concepts. Odontolog.y 2016;104:245-56.
Poulsen S, Gjørup H, Haubek D et al. Amelogenesis imperfecta – a systematic literature review of associated dental and oro-facial abnormalities and their impact on patients. Acta Odontol Scand. 2008;66:193-9.
Ray JG, Dutta S, Sarangi S et al. Noneruption of teeth in amelogenesis imperfecta: A report of two cases and review. J Oral Maxillofac Pathol. 2022;26:254-8.
Pousette Lundgren G, Dahllöf G. Outcome of restorative treatment in young patients with amelogenesis imperfecta. A cross-sectional, retrospective study. J Dent. 2014;42:1382-9.
Faria-e-Silva AL, De Moraes RR, Menezes Mde S et al. Hardness and microshear bond strength to enamel and dentin of permanent teeth with hypocalcified amelogenesis imperfecta. Int J Paediatr Dent. 2011;21:314-20.
Seow WK, Amaratunge A. The effects of acid-etching on enamel from different clinical variants of amelogenesis imperfects: An SEM study. Pediatr Dent. 1998;20:37-42.
Markovic D, Petrovic B, Peric T. Case series: clinical findings and oral rehabilitation of patients with amelogenesis imperfecta. Eur Arch Paediatr Dent. 2010;11:201-8.
Lindunger A, Smedberg JI. A retrospective study of the prosthodontic management of patients with amelogenesis imperfecta. Int J Prosthodont. 2005;18:189-94.
Pousette Lundgren G, Karsten A, Dahllöf G. Oral health-related quality of life before and after crown therapy in young patients with amelogenesis imperfecta. Health Qual Life Outcomes. 2015;13:197.
Lundgren GP, Wickström A, Hasselblad T et al. Amelogenesis imperfecta and early restorative crown therapy: An interview study with adolescents and young adults on their experiences. PLoS One. 2016;11:1-15.
McDonald S, Arkutu N, Malik K et al. Managing the paediatric patient with amelogenesis imperfecta. Br Dent J. 2012;212:425-8.
Innes NP, Evans DJP, Stirrups DR. The Hall Technique; A randomized controlled clinical trial of a novel method of managing carious primary molars in general dental practice: Acceptability of the technique and outcomes at 23 months. BMC Oral Health. 2007;7:18.
SUNDHEDSSTYRELSEN. Den kommunale tandpleje. Vejledning om omfanget af og kravene til den kommunale tandpleje. (Set 2023 maj). Tilgængelig fra: URL: https://www.sst.dk/da/Udgivelser/2020/Vejledningom-omfanget-af-og-kravene-til-den-kommunale-tandpleje
SUNDHEDSSTYRELSEN. Tillæg til vejledning om omfanget af og kravene til den kommunale og regionale tandpleje. (Set 2023 maj). Tilgængelig fra: URL: https://www.auh.dk/SysSiteAssets/afdelinger/tand-mund-ogkabekirurgisk-afd-o/pdf-filer/videncenter/sundhedsstyrelsenomfanget-af-og-kravene-til-denkommunale-og-regionaletandpleje-2006-vejledning/tillaegvejltandpleje.pdf.pdf
English summary
Enamel dysplasia or dentine anomaly? Aetiology, diagniostics, and treatment
Considerations of congenital, isolated tooth formation disturbancies in enamel and dentin
Nor Tannlegeforen Tid. 2024; 134: 392-401.
This paper reviews the two most frequent genetic dental anomalies, amelogenesis imperfecta (AI) and dentinogenesis imperfecta (DI). Aetiology and diagnosis of typical dental changes seen in the diseases are reviewed. The article also reviews the Health Act, referral practice with relevance to the subject, as well as current recommendations regarding preventive and reconstructive dental treatment in children and young people with these conditions.
Korrespondanceansvarlig førsteforfatter: Xenia Hermann, e-post: xenia.hermann@regionh.dk
Accepteret til publikation den 3. maj 2023 og først trykket i Tandlægebladet 2023; 127: 982-91.
Artikkelen er fagfellevurdert
Artikkelen siteres som: Hermann X, Daugaard-Jensen J, Lempert JS, Nørregaard M-LM, Hermann NV. Emaljedysplasi eller dentinanomali? Ætiologi, diagnostik og behandlingsovervejelser ved medfødte, isolerede tanddannelsesforstyrrelser i emalje og dentin. Nor Tannlegeforen Tid. 2024; 134: 392-401.
Emneord: Abnormalities, tooth formation | amelogenesis; imperfecta | dentinogenesis imperfecta; enamel dysplasia; dentin dysplasia
